đốt cháy hoàn toàn 11,5 gam hợp chất A thu được 22 gam CO2 và 13,5 gam nước biết khi hóa hơi,A có tỉ khối hơi với Hidro là 23

Những câu hỏi liên quan
Giup Anh mình bài này nha .
Đốt cháy hoàn toàn 11,5 gam hợp chất A, thu được 22 gam CO2 và 13,5 gam H2O. Biết khí hoá hơi, A có tỉ khối hơi so với hiđro bằng 23. Xác định công thức của phân tử A?
\(M_A=46\)
mC= 12 :44 . 22= 6g
mH= 2:18 . 13.5 = 1.5g
vì mC+mH < mA
=> hợp chất A có nguyên tố O.
gọi CTPT là : \(C_xH_yO_z\)
mO= 11.5-6-1.5= 4 g
mC: mH :mO = 12x : y: 16z = 6:1,5: 4
<=>x:y:z= 0,5 : 1,5 : 0,25
<=> x:y:z= 2 : 6: 1
CTTQ là : \(\left(C_2H_6O\right)_n\)
vì M_X= 46 <=> 46n=>n=1
vậy CTPT là : \(C_2H_6O\)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 1,52 gam chất X cần 0,56 lít oxi (đktc), thu được hỗn hợp khí gồm CO2, N2 và hơi nước. Sau khi ngưng tụ hơi nước hỗn hợp khí còn lại có khối lượng là 1,6 gam và có tỷ khối hơi đối với hidro là 20. Công thức đơn giản nhất của X là A. C3H8O5N2 B. C4H10O5N2 C. C2H6O5N2 D. C3H10O3N2
Đọc tiếp
Đốt cháy hoàn toàn 1,52 gam chất X cần 0,56 lít oxi (đktc), thu được hỗn hợp khí gồm CO2, N2 và hơi nước. Sau khi ngưng tụ hơi nước hỗn hợp khí còn lại có khối lượng là 1,6 gam và có tỷ khối hơi đối với hidro là 20. Công thức đơn giản nhất của X là
A. C3H8O5N2
B. C4H10O5N2
C. C2H6O5N2
D. C3H10O3N2
Đốt cháy hoàn toàn 1,52 gam chất X cần 0,56 lít oxi (đktc), thu được hỗn hợp khí gồm CO2, N2 và hơi nước. Sau khi ngưng tụ hơi nước hỗn hợp khí còn lại có khối lượng là 1,6 gam và có tỷ khối hơi đối với hidro là 20. Công thức đơn giản nhất của X là A. C3H8O5N2 B. C4H10O5N2 C. C2H6O5N2 D. C3H10O3N2
Đọc tiếp
Đốt cháy hoàn toàn 1,52 gam chất X cần 0,56 lít oxi (đktc), thu được hỗn hợp khí gồm CO2, N2 và hơi nước. Sau khi ngưng tụ hơi nước hỗn hợp khí còn lại có khối lượng là 1,6 gam và có tỷ khối hơi đối với hidro là 20. Công thức đơn giản nhất của X là
A. C3H8O5N2
B. C4H10O5N2
C. C2H6O5N2
D. C3H10O3N2
Đáp án A
Định hướng tư duy giải
Ta có:
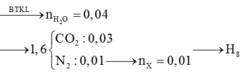
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 3,24 gam hỗn hợp X gồm hai chất hữu cơ A và B (trong đó A hơn B một nguyên tử C, MA MB), thu được m gam H2O và 9,24 gam CO2. Biết tỉ khối hơi của X so với H2 là 13,5. Giá trị m là: A. 1,26 B. 1,08 C. 2,61 D. 2,16
Đọc tiếp
Đốt cháy hoàn toàn 3,24 gam hỗn hợp X gồm hai chất hữu cơ A và B (trong đó A hơn B một nguyên tử C, MA < MB), thu được m gam H2O và 9,24 gam CO2. Biết tỉ khối hơi của X so với H2 là 13,5. Giá trị m là:
A. 1,26
B. 1,08
C. 2,61
D. 2,16
Chọn đáp án D
MX = 13,5 × 2 = 27 ⇒ nX = 3,24 ÷ 27 = 0,12 mol
nCO2 = 0,21 mol ⇒ Ctb = 0,21 ÷ 0,12 = 1,75 ⇒ A chứa 2C và B chứa 1C.
Đặt nA = x; nB = y || nX = x + y = 0,12 mol; nCO2 = 2x + y = 0,21 mol
||⇒ giải hệ có:x = 0,09 mol; y = 0,03 mol. Mặt khác:
MX = 27 và MA < MB ⇒ MA < 27 ⇒ A là C2H2.
||⇒ MB = (3,24 - 0,09 × 26) ÷ 0,03 = 30 ⇒ B là HCHO.
► m = 18 × (0,09 + 0,03) = 2,16(g) ⇒ chọn D
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 3,24 gam hỗn hợp X gồm hai chất hữu cơ A và B (trong đó A hơn B một nguyên tử cacbon, MA MB), thu được m gam H2O và 9,24 gam CO2. Biết tỉ khối hơi của X so với H2 là 13,5. Giá trị của m là: A. 1,26 B. 1,08 C. 2,61 D. 2,16
Đọc tiếp
Đốt cháy hoàn toàn 3,24 gam hỗn hợp X gồm hai chất hữu cơ A và B (trong đó A hơn B một nguyên tử cacbon, MA< MB), thu được m gam H2O và 9,24 gam CO2. Biết tỉ khối hơi của X so với H2 là 13,5. Giá trị của m là:
A. 1,26
B. 1,08
C. 2,61
D. 2,16
Đáp án D
M tb = 27g/mol
=> n hh = 0,12mol
nCO2 = 0,21
=> số nguyên tử C trung bình = 1,75
Mặt khác A, B khác dãy đồng đẳng và hơn kém nhau 1 C => 16 < M tb < 28
=> A: C2H4 và B: CH4
=> nC2H4 = 0,03mol và nCH4 = 0,15mol
=> nH2O = 0,24mol
Gọi công thức cần tìm là CxHyOz
MX = 27 => nX = 3,24/27 = 0,12 nCO2 = 9,24/44 = 0,21
=> số nguyên tử C trung bình = 0,21/0,12 = 1,75 Mtrung bình = 27
=> phải có 1 chất có khối lượng mol < 27
=> B là CH4 hoặc C2H2 => A có 2 nguyên tử C và B có 1 C => nB = 3nA a + b = 0,12 mà b = 3a => a = 0,03 mol a . MA + b . MB = 3,24 => 0,03 . MA + 0,09 . MB = 3,24 => A là CH2O và B là C2H2
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 3,24 gam hỗn hợp X gồm hai chất hữu cơ A và B (trong đó A hơn B một nguyên tử C, MA MB), thu được m gam H2O và 9,24 gam CO2. Biết tỉ khối hơi của X so với H2 là 13,5. Giá trị m là: A. 1,26 B. 1,08 C. 2,61 D. 2,16
Đọc tiếp
Đốt cháy hoàn toàn 3,24 gam hỗn hợp X gồm hai chất hữu cơ A và B (trong đó A hơn B một nguyên tử C, MA < MB), thu được m gam H2O và 9,24 gam CO2. Biết tỉ khối hơi của X so với H2 là 13,5. Giá trị m là:
A. 1,26
B. 1,08
C. 2,61
D. 2,16
Chọn đáp án D
MX = 13,5 × 2 = 27 ⇒ nX = 3,24 ÷ 27 = 0,12 mol
nCO2 = 0,21 mol ⇒ Ctb = 0,21 ÷ 0,12 = 1,75 ⇒ A chứa 2C và B chứa 1C.
Đặt nA = x; nB = y nX = x + y = 0,12 mol; nCO2 = 2x + y = 0,21 mol
⇒ giải hệ có:x = 0,09 mol; y = 0,03 mol. Mặt khác:
MX = 27 và MA < MB ⇒ MA < 27 ⇒ A là C2H2.
⇒ MB = (3,24 - 0,09 × 26) ÷ 0,03 = 30 ⇒ B là HCHO.
► m = 18 × (0,09 + 0,03) = 2,16(g) ⇒ chọn D
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 3,24 gam hỗn hợp X gồm hai chất hữu cơ A và B khác dãy đồng đẳng và cùng loại hợp chất, trong đó A hơn B một nguyên tử cacbon, người ta chỉ thu được nước và 9,24 gam CO2. Biết tỉ khối hơi của X đối với H2 là 13,5.a. Tìm công thức cấu tạo của A, B và tính thành phần trăm theo khối lượng của mỗi chất trong hỗn hợp X.b. Từ B viết sơ đồ phản ứng điều chế CH3COOCH3và
Đọc tiếp
Đốt cháy hoàn toàn 3,24 gam hỗn hợp X gồm hai chất hữu cơ A và B khác dãy đồng đẳng và cùng loại hợp chất, trong đó A hơn B một nguyên tử cacbon, người ta chỉ thu được nước và 9,24 gam CO2. Biết tỉ khối hơi của X đối với H2 là 13,5.
a. Tìm công thức cấu tạo của A, B và tính thành phần trăm theo khối lượng của mỗi chất trong hỗn hợp X.
b. Từ B viết sơ đồ phản ứng điều chế CH3COOCH3và![]()
2. Đốt cháy hoàn toàn 23 gam hợp chất A cần 33,6 lít ôxi (đktc) và thu được thể tích CO2 bằng 2/3 thể tích hơi nước . Xác định CTHH của A. Biết rằng tỉ khối hơi của A so với khí ôxi là 1,4375.
Do đốt cháy A thu được sản phẩm chứa C, H, O
=> Trong A chứa C, H và có thể có O
Gọi \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{2}{3}a\left(mol\right)\\n_{H_2O}=a\left(mol\right)\end{matrix}\right.\)
\(n_{O_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\)
Theo ĐLBTKL: \(44.\dfrac{2}{3}a+18a=23+1,5.32=71\)
=> a = 1,5 (mol)
=> \(\left\{{}\begin{matrix}n_C=n_{CO_2}=1\left(mol\right)\\n_H=2.n_{H_2O}=3\left(mol\right)\end{matrix}\right.\)
=> \(n_O=\dfrac{23-1.12-3.1}{16}=0,5\left(mol\right)\)
Xét nC : nH : nO = 1 : 3 : 0,5 = 2 : 6 : 1
=> CTPT: (C2H6O)n
Mà MA = 1,4375.32 = 46 (g/mol)
=> n = 1
=> CTPT: C2H6O
Đúng 3
Bình luận (0)
\(n_{O_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\\ m_{O_2}=1,5.32=48\left(g\right)\)
Bảo toàn khối lượng: mH2O + mCO2 = mA + mO2 = 23 + 48 = 71 (g)
Ta có:
\(\dfrac{V_{CO_2}}{V_{H_2O}}=\dfrac{2}{3}\Rightarrow\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{2}{3}\\ \Rightarrow\dfrac{m_{CO_2}}{m_{H_2O}}=\dfrac{2}{3}.\dfrac{44}{18}=\dfrac{44}{27}\\ \Rightarrow\dfrac{m_{CO_2}}{44}=\dfrac{m_{H_2O}}{27}\)
Theo t/c của dãy tỉ số bằng nhau:
\(\dfrac{m_{CO_2}}{44}=\dfrac{m_{H_2O}}{27}=\dfrac{m_{CO_2}+m_{H_2O}}{44+27}=\dfrac{71}{71}=1\)
=> \(\left\{{}\begin{matrix}m_{CO_2}=1.44=44\left(g\right)\\m_{H_2O}=1.27=27\left(g\right)\end{matrix}\right.\)
Bảo toàn C và H: \(\left\{{}\begin{matrix}n_C=n_{CO_2}=\dfrac{44}{44}=1\left(mol\right)\\n_H=2n_{H_2O}=\dfrac{2.27}{18}=3\left(mol\right)\end{matrix}\right.\)
Bảo toàn O: \(n_O=\dfrac{23-12-3}{16}=0,5\left(mol\right)\)
MA = 1,4375.32 = 46 (g/mol)
CTPT của A có dạng: CxHyOz
=> x : y : z = 1 : 3 : 0,5 = 2 : 6 : 1
=> (C2H6O)n = 46
=> n = 1
=> CTPT của A là C2H6O
Đúng 2
Bình luận (1)
Đốt cháy hoàn toàn 23 gam hợp chất A cần 33,6 lít oxi (đkt) và thu được thể tích CO2 bằng 2 phần 3 thể tích hơi nước. Xác định công thức hoá của A. Biết rằng tỉ khối hơi của A so với khí oxi là 1,4375.
Tham khảo:
Đốt cháy A chỉ tạo ra CO2 và H2O nên A chứa C;H;O
Vậy A có dạng CxHyOz
Phản ứng xảy ra:
CxHyOz+(x+y/4−z/2)O2to→xCO2+y2H2O
Ta có:
MA=1,4375MO2=1,4375.32=46
→12x+y+16z=46
Ta có:
nA=23/46=0,5 mol
nO2=33,6/22,4=1,5 mol
→x+y/4−z/2=nO2/nA=1,5/0,5=3
Ta có:
nCO2:nH2O=x:y2=2:3→x:y=2:6=1:3
Giải được: x=2;y=6;y=1
Vậy A là C2H6O
Đúng 2
Bình luận (0)

















