Khi cho 13g kẽm tác dụng với 0,3 mol HCl. Khối lượng mối ZnCl22 được tạo thành trong những phản ứng này là :
Câu 74) khi cho 13g kẽm tác dụng với 0,3 mol HCl. Khối lượng muối ZnCl2 đc tạo thành trong phản ứng này là?
Câu 69) có những chất sau: Cu(OH)2, Cu, Na2SO3, NaCl, CaO, MgO, Lần lượt tác dụng với dung dịch axit HCl, có những hiện tượng gì?
Câu 99) dung dịch chứa 7,4g canxi hiđroxit hấp thụ hoàn toàn 1,12 lít khí cacbonđioxit ( đo ở đktc) . Khối lượng CaCO3 tạo thành sau phản ứng là:
A. 5,1 g
B. 10g
C. 5g
D. 4,9g
Câu 69 :
- Cu(OH)2 tan dần, xuất hiện dung dịch xanh lam
$Cu(OH)_2 + 2HCl \to CuCl_2 + 2H_2O$
- Cu không phản ứng với HCl
- Na2SO3 tan dần, xuất hiện khí mùi hắc
$Na_2SO_3 + 2HCl \to 2NaCl + SO_2 + H_2O$
- NaCl tan dần,tạo thành dung dịch không màu
- CaO tan dần, tạo thành dung dịch không màu
$CaO + 2HCl \to CaCl_2 + H_2O$
- MgO tan dần, tạo thành dung dịch không màu
$MgO + 2HCl \to MgCl_2 + H_2O$
Câu 74 :
$n_{Zn} = \dfrac{13}{65} = 0,2(mol)$
$Zn + 2HCl \to ZnCl_2 + H_2$
Ta thấy :
$n_{Zn} : 1 > n_{HCl} : 2$ nên Zn dư
$n_{ZnCl_2} = \dfrac{1}{2}n_{HCl} = 0,15(mol)$
$m_{ZnCl_2} = 0,15.136 = 20,4(gam)$
Câu 99 :
$n_{Ca(OH)_2} = 0,1(mol) > n_{CO_2} = \dfrac{1,12}{22,4} = 0,05(mol)$
nên Ca(OH)2 dư
$Ca(OH)_2 + CO_2 \to CaCO_3 + H_2O$
$n_{CaCO_3} = n_{CO_2} = 0,05(mol)$
$m_{CaCO_3} = 0,05.100 = 5(gam)$
Đáp án C
Cho 6,5 gam kẽm tác dụng với 0,3 mol HCl, khối lượng muối clorua tạo thành trong phản ứng là
A. 15,3g
B. 5,1g
C. 13,6g
D. 10,2g
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
Xét theo tỉ lệ:
\(\dfrac{n_{Zn}}{1}=\dfrac{0,1}{1}\)
\(\dfrac{n_{HCl}}{2}=\dfrac{0,3}{2}\)
\(\Rightarrow\dfrac{n_{Zn}}{1}< \dfrac{n_{HCl}}{2}\)
Vậy HCl dư
Theo PTHH: \(n_{ZnCl_2}=n_{Zn}=0,1\left(mol\right)\)
Khối lượng muối clorua tạo thành là:
\(m_{ZnCl_2}=n_{ZnCl_2}.M_{ZnCl_2}=0,1.136=13,6\left(g\right)\)
Lập PTHH của phản ứng giữa HCl tác dụng với kẽm theo sơ đồ sau: Zn + HCl −−→ ZnCl2 + H2
Biết rằng sau phản ứng thu được 0,3 mol khí hydrogen H2. Hãy tính: a) Khối lượng kẽm đã phản ứng
b) Khối lượng axit HCl đã phản ứng
c) Khối lượng ZnCl2 tạo thành.
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
___0,3____0,6_____0,3____0,3 (mol)
a, \(m_{Zn}=0,3.65=19,5\left(g\right)\)
b, \(m_{HCl}=0,6.36,5=21,9\left(g\right)\)
c, \(m_{ZnCl_2}=0,3.136=40,8\left(g\right)\)
Bạn tham khảo nhé!
Zn+2HCl->ZnCl2+H2
0,3---0,6-----0,3----0,3 mol
=>m Zn=0,3.65=19,5g
=>m HCl=0,6.35,6=21,9g
=>m ZnCl2=0,3.136=40,8g
1.Cho 13g kẽm tác dụng với 100ml dung dịch HCl 3M
a. Chất nào còn dư trong phản ứng trên?
b. Khối lượng muối ZnCl2 được tạo thành trong phản ứng này là?
2.Trộn dung dịch có chứa 22,2g CaCl2 với dung dịch có chứa 1,7g AgNO3.
a. Chất nào còn dư trong phản ứng trên?
b. Tính khối lượng kết tủa thu được
Bài 2:
\(a.n_{CaCl_2}=\dfrac{22,2}{111}=0,2\left(mol\right)\\ n_{AgNO_3}=\dfrac{1,7}{170}=0,01\left(mol\right)\\ CaCl_2+2AgNO_3\rightarrow Ca\left(NO_3\right)_2+2AgCl\\ a.Vì:\dfrac{0,2}{1}>\dfrac{0,01}{2}\Rightarrow CaCl_2dư\\b.n_{AgCl}=n_{AgNO_3}=0,01\left(mol\right)\\ \Rightarrow m_{\downarrow}=m_{AgCl}=143,5.0,01=1,435\left(g\right)\)
Bài 1:
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\\ n_{HCl}=0,1.3=0,3\left(mol\right)\\ Zn+2HCl\rightarrow ZnCl_2+H_2\\ a,Vì:\dfrac{0,3}{2}< \dfrac{0,2}{1}\Rightarrow Zndư\\ b.n_{ZnCl_2}=\dfrac{0,3}{2}=0,15\left(mol\right)\\ m_{ZnCl_2}=136.0,15=20,4\left(g\right)\)
Cho 13g kẽm tác dụng hết với dung dịch HCL thu được ZNCL2 và khí H2 , cho toàn bộ lượng khí Hidro thu được tác dụng với 20g CuO , sản phẩm là Cu và H2O a) Viết PTHH xảy ra b) tính khối lượng ZnCl2 tạo thành c) tính khối lượng còn dư sau phản ứng khử Mn giúp mình với ạ mình sắp thi rồi
a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(H_2+CuO\underrightarrow{t^o}Cu+H_2O\)
b, Ta có: \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
Theo PT: \(n_{ZnCl_2}=n_{H_2}=n_{Zn}=0,2\left(mol\right)\Rightarrow m_{ZnCl_2}=0,2.136=27,2\left(g\right)\)
c, \(n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{1}< \dfrac{0,25}{1}\), ta được CuO dư.
Theo PT: \(n_{CuO\left(pư\right)}=n_{H_2}=0,2\left(mol\right)\Rightarrow n_{CuO\left(dư\right)}=0,25-0,2=0,05\left(mol\right)\)
\(\Rightarrow m_{CuO\left(dư\right)}=0,05.80=4\left(g\right)\)
Khi cho 13g kẽm tác dụng với 0,3 mol HCl.Khối lượng ZnCl2 được tạo thành trong phản ứng này là bao nhiêu gam?
PTHH: Zn + 2HCl \(\rightarrow\) ZnCl2 + H2\(\uparrow\)
nZn = \(\frac{13}{65}=0,2\left(mol\right)\)
Ta có tỉ lệ: \(\frac{n_{Zn}}{1}=0,2>\frac{n_{HCl}}{2}=\frac{0,3}{2}=0,15\)
=> Zn dư , HCl hết
=> Tính số mol các chất cần tìm theo HCl
Theo PT: n\(ZnCl_2\) = \(\frac{1}{2}n_{HCl}\) = \(\frac{1}{2}.0,3=0,15\left(mol\right)\)
=> m\(ZnCl_2\) = 0,15.136 = 20,4 (g)
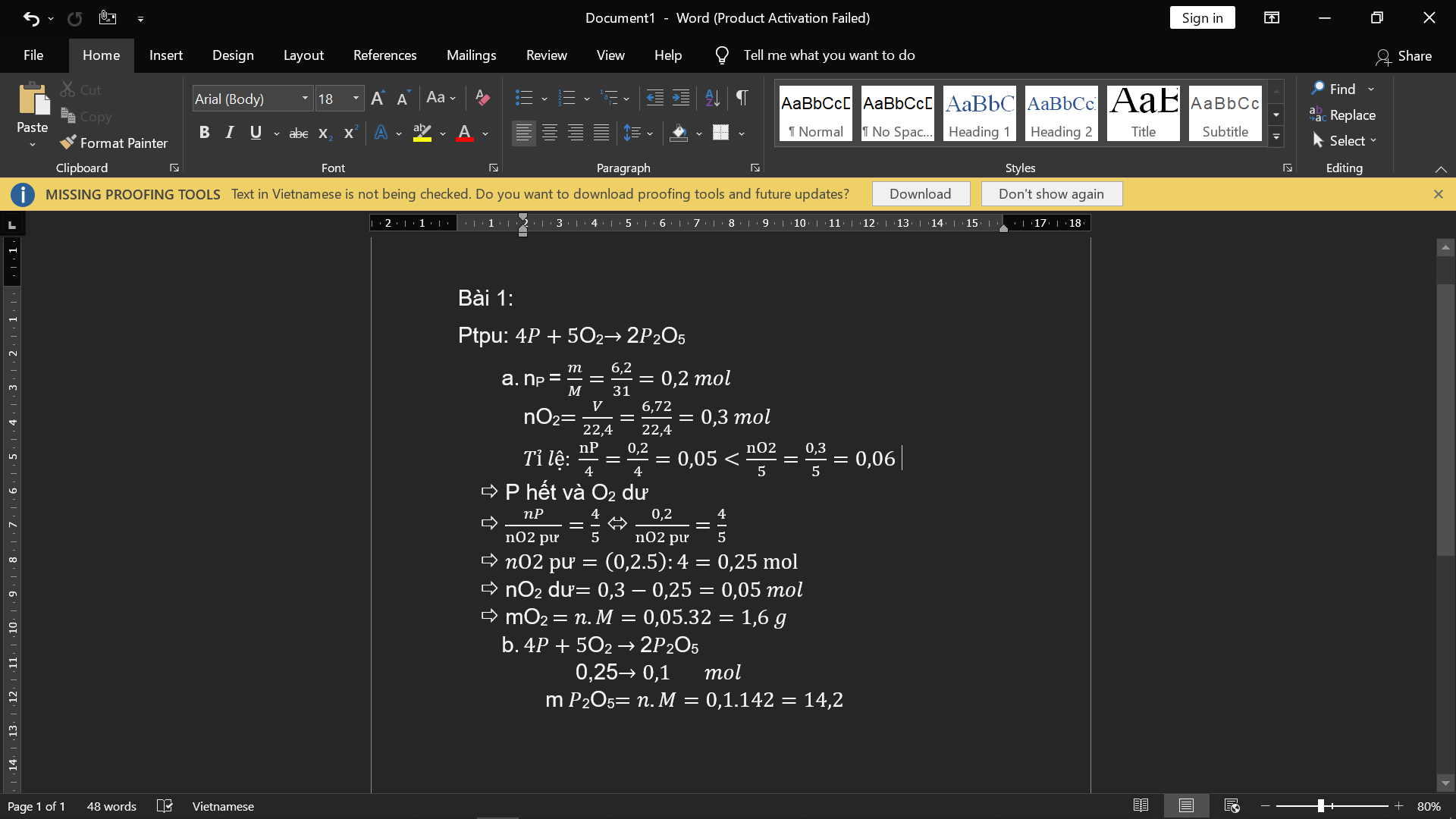
Bài 1: Đốt cháy 6,2(g) P trong bình chứa 6,72(l) khí O2 ở đktc.
a. Sau phản ứng chất nào còn dư và nếu dư thì với khối lượng bao nhiêu? b. Tính khối lượng sản phẩm thu được.
Bài 2: Cho 13g Zn tác dụng với 0,3 mol HCl sau khi kết thúc phản ứng thu được muối kẽm Clorua và khí H2.
a. Viết và cân bằng PTPƯ và cho biết sau khi kết thúc phản ứng thì chất nào còn dư và nếu dư thì dư với khối lượng bao nhiêu?.
b. Tính thể tích của H2 thu được.
Bài 3: Người ta cho 26 g kẽm tác dụng với 49 g H2SO4, sau phản ứng thu được muối ZnSO4, khí hidro và chất còn dư.
a. Viết phương trình phản ứng.
b. Tính thể tích (đktc) khí hidro sinh ra.
c. Tính khối lượng các chất còn lại sau phản ứng.
Bài 4: Nếu cho 4 gam CuO tác dụng với 2,92 g HCl.
a) Cân bằng PTHH.
b) Tính khối lượng các chất còn lại sau phản ứng.
Bài 5: Hòa tan hoàn toàn 15gam CaCO3 vào 200mL dung dịch HCl 2M.
a. Chobiếtchấtnàodưsauphảnứng.
b. Tính nồng độ mol của các chất tan có trong dung dịch thu được.
Bài 6: Hòa tan hết 4,8 gam Magie vào 200 gam dung dịch H2SO4 loãng nồng độ 20%.
a. Chobiếtchấtnàodưsauphảnứng.
b. Tính nồng độ chất tan có trong dung dịch sau phản ứng.
Bài 7: Cho 200 ml dung dịch NaOH nồng độ 2M vào 200 mL dung dịch HCl 4M.
a. Chobiếtchấtnàodưsauphảnứng.
b. Tính nồng độ mol của chất tan trong dung dịch sau phản ứng.
Bài 1:
a) nP=6,2/31=0,2(mol); nO2= 6,72/22,4=0,3(mol)
PTHH: 4P + 5 O2 -to-> 2 P2O5
Ta có: 0,2/4 < 0,3/5
=> P hết, O2 dư, tính theo nP
=> nO2(p.ứ)= 5/4. nP= 5/4. 0,2=0,25(mol)
=> mO2(dư)=0,3- 0,25=0,05(mol)
=> mO2(dư)=0,05.32=1,6(g)
b) nP2O5= nP/2= 0,2/2=0,1(mol)
=>mP2O5=0,1.142=14,2(g)
b ơi đây là bài 1 nka, tí mk làm xog sẽ gửi típ nka ![]()
Cho 13g kẽm tác dụng vừa đủ với dung dịch HCl 8%
1. Tính khối lượng dung dịch axit đã phản ứng.
2. Tính khối lượng khí hidro và muối tạo thành.
3. Tính khối lượng dung dịch sau phản ứng.
4.Tính nồng đọ % dung dịch sau phản ứng.
1) nZn=13/65=0,2(mol)
PTHH: Zn + 2 HCl -> ZnCl2 + H2
nH2=nZnCl2=nZn=0,2(mol)
nHCl=2.0,2=0,4(mol)
=> mHCl=0,4 x 36,5=14,6(g)
=> mddHCl=(14,6.100)/8=182,5(g)
2) V(H2,đktc)=0,2 x 22,4= 4,48(l)
mZnCl2=0,2.136=27,2(g)
3) mddsau=mZn+mddHCl - mH2= 13+182,5-0,2.2=195,1(g)
4) C%ddZnCl2=(27,2/195,1).100=13,941%
Cho 13g Zn tác dụng với 0,3 mol HCl sau khi kết thúc phản ứng thu được muối kẽm Clorua và khí H 2. Thể tích khí hidro thu được ở đktc là:
A.
5,6 l.
B.
22,4l.
C.
11,2 l.
D.
3,36 l.
Ta có: nZn = \(\dfrac{13}{65}\) = 0,2 mol
PTHH : Zn + 2HCl → ZnCl2 + H2
ban đầu : 0,2 0,3
phản ứng : 0,15 0,3 0,15
sau phản ứng : 0,05 0 0,15
→ nH2 = 0,15 mol
=> VH2 = 0,15 . 22,4 = 3,36 lít
Đáp án đúng là D bạn nhé