cho lượng khí CI dư đi qua 17,4 g một oxit kim loại nung nóng đến hoàn toàn thu được 12,18 g kim loại. cho lượng kim loại này vào dung dịch h2so4 loãng dư thấy sinh ra 4,872 l khí h2 ở đktc. tìm công thức hóa học của oxit trên
cho lượng khí co dư đi qua 17,4 g mỗi oxit kim loại nung nóng đến hoàn toàn thu được 12,18 g kim loại cho lượng kim loại này vào dd h2so4 loãng dư thấy sinh ra 4,82 l khí h2 ở đktc tìm cthh của oxit kim loại trên
Gọi M là kim loại
=> CT của oxit kim loại cần tìm: MxOy
PTHH: yCO + MxOy ----> xM + yCO2 (1)
Khi cho kim loại thu được qua dd H2SO4 Dư thì:
pthh: 2M + nH2SO4 ----> M2(SO4)n + nH2 (2)
nH2 thoát ra = \(\frac{4,82}{22,4}\) \(\approx\) 0,22 (mol)
theo nM = \(\frac{0,44}{n}\)(mol)
Ta có 12,18 = \(\frac{0,44}{n}\) . M
<=> 12,18n = 0,44M
<=> M = 27,7n
<lập bảng chọn>
với n = 2 thì M= 56 (nhận)
vậy M là Fe
theo (1), nFe = 0,22 mol
=> nFexOy = \(\frac{0,22}{x}\) mol
ta có 17,4 = \(\frac{0,22}{x}\) . (56x + 16y)
<=> 17,4x = 12,32x + 3,52y
<=> 5,08x = 3,52y
<=> x = 0,69y
<lập bảng chọn>
ta được: khi giá trị y = 3 thì x = 2
=> ct của Oxit Sắt là Fe2O3
Khử hoàn toàn 24 g một oxit kim loại M bằng H2 dư thu được 8,1 g nước. Hòa tan toàn bộ lượng kim loại sinh ra bằng dd H2SO4 loãng dư thu được 6,72 lít H2 ở đktc. Xác định oxit kim loại M?
Ta có: \(n_{H_2O}=\dfrac{8,1}{18}=0,45\left(mol\right)\)
⇒ n O (trong oxit) = 0,45 (mol)
Có: m oxit = mM + mO ⇒ mM = 24 - 0,45.16 = 16,8 (g)
Giả sử kim loại M có hóa trị n khi tác dụng với H2SO4.
PT: \(2M+nH_2SO_4\rightarrow M_2\left(SO_4\right)_n+nH_2\)
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_M=\dfrac{2}{n}n_{H_2}=\dfrac{0,6}{n}\left(mol\right)\)
\(\Rightarrow M_M=\dfrac{16,8}{\dfrac{0,6}{n}}=28n\)
Với n = 1 ⇒ MM = 28 (loại)
Với n = 2 ⇒ MM = 56 (nhận)
Với n = 3 ⇒ MM = 84 (loại)
⇒ M là Fe. ⇒ Oxit cần tìm là FexOy.
PT: \(Fe_xO_y+yH_2\underrightarrow{t^o}xFe+yH_2O\)
Theo PT: \(n_{Fe_xO_y}=\dfrac{1}{y}n_{H_2O}=\dfrac{0,45}{y}\left(mol\right)\)
\(\Rightarrow M_{Fe_xO_y}=\dfrac{24}{\dfrac{0,45}{y}}=\dfrac{160}{3}y\)
\(\Rightarrow56x+16y=\dfrac{160}{3}y\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
Vậy: Oxit đó là Fe2O3.
Bạn tham khảo nhé!
Khử hoàn toàn 4,06 gam một oxit kim loại bằng khí CO ở nhiệt độ cao thành kim loại. Dẫn toàn bộ khí sinh ra vào bình đựng dung dịch Ca(OH)2 (dư) tạo thành 7,00 gam kết tủa. Nếu lấy lượng kim loại sinh ra hòa tan hết vào dung dịch HCl (dư) thì thu được 1,176 lít khí H2 (đktc). Công thức của oxit kim loại là
A. FeO.
B. CrO.
C. Fe2O3.
D. Fe3O4
Gọi công thức oxit ban đầu là MxOy.
Có phản ứng khử hoàn toàn oxit MxOy thành kim loại:
![]()
Dẫn khí CO2 sinh ra hấp thụ vào dung dịch Ca(OH)2 dư:
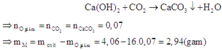
Cần lưu ý: Hóa trị của kim loại M trong oxit ban đầu và hóa trị của M trong sản phẩm của phản ứng giữa M với axit HCl có thể khác nhau.
Do đó ta gọi n là hóa trị của M thể hiện khi phản ứng với axit HCl.
![]()
Áp dụng định luật bào toàn mol electron, ta có:
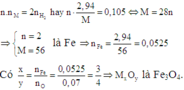
Đáp án D.
Khử hoàn toàn 12,76 gam một oxit kim loại (RxOy) bằng khí CO vừa đủ thu được kim loại R và khí CO2. Hấp thụ hết khí CO2 sinh ra vào dung dịch Ca(OH)2 dư, thu được 22 gam kết tủa trắng. Cho toàn bộ lượng kim loại R thu được ở trên tác dụng hết với dung dịch H2SO4 đặc nóng, dư thu được 5,544 lít một khí có mùi hắc (đktc). Xác định công thức của RxOy
Cho V lít khí CO đktc đi qua ống sứ chứa 2,32g oxit sắt kim loại nung nóng đến phản ứng hoàn toàn thu được m gam kim loại và hỗn hợp khí có tỉ khối so với H2 bằng 18.Dẫn toàn bộ lượng khí này vào bình chứa 2000ml dung dịch Ca(OH)2 0,015M.Kết thúc phản ứng thu được 2g kết tủa và dung dịch A.Lọc tách kết tủa rồi cho dung dịch Ba(OH)2 dư vào dung dịch A ta thu được p gam kết tủa.Cho toàn bộ lượng kim loại thi được ở trên vào bình chứa dung dịch HCl dư,phản ứng kết thúc ta thu được 0,672 lít khí H2 đktc.Viết các PTHH xảy ra.Tính C,m,p và xác định CT của oxit kim loại
Khử hoàn toàn 4,06 gam một oxit kim loại bằng CO ở nhiệt độ cao thành kim loại. Dẫn toàn bộ sản phẩm khí sinh ra vào dung dịch Ca(OH)2 dư thấy tạo thành 7 gam kết tủa. Nếu lấy lượng kim loại sinh ra hoà tan hết vào dung dịch HCl thì thu được 1,176 lít H2 (đktc). Công thức của oxit kim loại là
A. CuO.
B. Al2O3.
C. Fe3O4.
D. ZnO.
Đáp án C
nCO2 = nCaCO3 = 0,07 mol
O + CO → CO2
0,07 ← 0,07
mKL = moxit – mO
= 4,06 – 0,07.16 = 2,94 (g)
Gọi hóa trị của KL khi tác dụng với HCl là n
M → 0,5n H2
0,105/n← 0,0525 (mol)
![]()
![]()
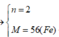
![]()
![]()
Cho 20,16 lít khí CO phản ứng với một lượng oxit MxOy nung nóng. Sau khi phản ứng xảy ra hoàn toàn, thu được 25,2 gam kim loại M và hỗn hợp khí X. Cho toàn bộ lượng hỗn hợp khí X qua bình chứa dung dịch Ca(OH)2 dư tạo ra m gam kết tủa và có 6,72 lít khí thoát ra. Hòa tan hoàn toàn lượng kim loại trên trong dung dịch HCl dư, thấy thoát ra 10,08 lít khí H2. Xác định công thức oxit và tính m. Biết thể tích các khí đo ở điều kiện tiêu chuẩn.
Dung dịch Ca(OH)2 không hấp thụ khí CO nên 6,72 lít khí thoát ra chính là khí CO dư.

Khử hoàn toàn 4,06g một oxit kim loại bằng CO ở nhiệt độ cao thành kim loại. Dẫn toàn bộ khí sinh ra vào bình đựng nước vôi trong dư, thấy tạo thành 7g kết tủa. Nếu lấy lượng kim loại sinh ra hòa tan hết vào dung dịch HCl dư thì thu được 1,176 lít khí H2 (đktc). Xác định công thức oxit kim loại.
BL
CO2+Ca(OH)2==>CaCO3+H20
0.07<= 0.07
đây là bài toán lừa đó bạn ạ . hóa trị của KL thay đổi nên gọi n m lan luot la hoa trị trong oxit và trong KL
ta gọi KL la M
M+ nHCL= MCLm+ (n/2) H2
1.76/22.4
từ PT khử thành KL áp dụng định luật BTKL ta có
mM=4.06+0.07*28-0.07*44=2.94 g
==> M=18.7n
xét từng trường hợp => M=56==> Fe . CT oxit Fe3O4
Chúc bn học tốt![]()
khử hoàn toàn 4,06 một oxit kim loại bằng CO ở nhiệt đọ cao thành kim loại .Dẫn toàn bộ khí sinh ra vào bình đựng Ca(OH)2 dư , thấy tạo thành 7g kết tủa .nếu lấy lượng kim loại sinh ra hòa tan hết vào dung dịch HCl dư thì thu được 1,176 lít khí H2 (đktc).xác định công thức phân tử oxit kim loại .
Gọi CT của oxit cần tìm là RxOy
RxOy+yCO→xR+yCO2 (1)
CO2+Ca(OH)2→CaCO3+H2O (2)
Vì Ca(OH)2 dư nên nCO2=n↓=0,07 mol
Theo PTHH (1), nO trong oxit=nCO2=0,07 mol
→mO trong oxit=0,07.16=1,12 g
→mR trong oxit=4,06−1,12=2,94 g
+) Cho kim loại R tác dụng với dung dịch HCl
PTHH: 2R+2nHCl→2RCln+nH2 (3)
Ta có: nH2=0,0525 mol
Theo (3), nR=\(\dfrac{2}{n}\)H2=\(\dfrac{0,105}{n}\)
→\(\dfrac{0,105}{n}R\)=2,94→R=28n
Chỉ có cặp nghiệm duy nhất thỏa mãn:
\(\left\{{}\begin{matrix}n=2\\R=56\left(Fe\right)\end{matrix}\right.\)
→nFe=0,0525 mol
Khi đó ta có: \(\dfrac{x}{y}:\dfrac{nFe}{nO}:\dfrac{0,0525}{0,07}=\dfrac{3}{4}\)
Vậy CT của oxit kim loại cần tìm là: Fe3O4