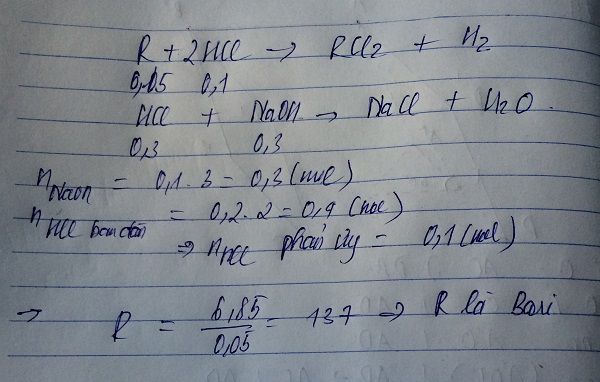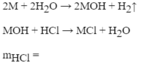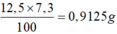hòa tan hoàn toàn một kim loại kiềm thổ R vào 200ml dung dịch HCl 2M.Để trung hòa lượng axit dư cần 100ml dung dịch NaOH 3M xác định tên kim loại đó.....trân thành cẳm ơn

Những câu hỏi liên quan
hòa tan hoàn toàn một kim loại kiềm thổ R vào 200ml dung dịch HCl 2M.Để trung hòa lượng axit dư cần 100ml dung dịch NaOH 3M xác định tên kim loại đó.....trân thành cẳm ơn
<a href="http://tchiase.info/office-2016-tai-office-2016-professional-plus-full-crack/">tải office 2016</a>
Đúng 0
Bình luận (0)
Hòa tan 1,3g một kim loại R trong 100ml dung dịch H2SO4 0,3M. Để trung hòa lượng axit dư cần 200ml dung dịch NaOH 0,1M. Xác định kim loại R?
\(n_{NaOH} =0,2.0,1 = 0,02(mol)\\ 2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O\\ n_{H_2SO_4\ dư} = \dfrac{1}{2}n_{NaOH} = 0,01(mol)\\ \Rightarrow n_{H_2SO_4\ pư} = 0,1.0,3 - 0,01 = 0,02(mol)\)
Gọi n là hóa trị của kim loại R
\(2R + nH_2SO_4\to R_2(SO_4)_3 + nH_2\\ n_R = \dfrac{2}{n}n_{H_2SO_4} = \dfrac{0,04}{n}(mol)\\ \Rightarrow \dfrac{0,04}{n}.R = 1,3\\ \Rightarrow R = \dfrac{65}{2}n\)
Với n = 2 thì R = 65(Zn)
Đúng 1
Bình luận (1)
Hòa tan hoàn toàn 6,85 g một kim loại kiềm thổ R bằng 50 ml dung dịch HCl 2 M. Xác định tên kim loại trên.
Để hòa tan hoàn toàn 7,2 gam một kim loại M hóa trị II thì cần dùng hết 200ml dung dịch axit HCl 3M. Xác định tên kim loại M đem dùng.
Hòa tan hoàn toàn 0,575 gam một kim loại kiềm vào nước. Để trung hòa dung dịch thu được cần dùng 12,5 gam dung dịch HCl 7,3% (Li=7, Na=23, K=39, Rb=85, H=1, Cl=35,5). Xác định tên kim loại kiềm.
bài 1:cho 7,2g kim loại hóa trị II phản ứng hoàn toàn 100ml dung dịch HCL 6M. Xác định tên kim loại đã dùng
baì 2: hòa tan hoàn toàn 7,56g kim loại R có hóa trị III vào dung dịch axit HCL thu được 9,408 lít H2 (đktc). Tìm kim loại R
Giúp mik vs ạ ! Cảm ơn
Bài 1:
Gọi KL cần tìm là A.
PT: \(A+2HCl\rightarrow ACl_2+H_2\)
Ta có: \(n_{HCl}=0,1.6=0,6\left(mol\right)\)
Theo PT: \(n_A=\dfrac{1}{2}n_{HCl}=0,3\left(mol\right)\)
\(\Rightarrow M_A=\dfrac{7,2}{0,3}=24\left(g/mol\right)\)
Vậy: KL cần tìm là Mg.
Đúng 1
Bình luận (0)
Bài 2:
PT: \(2R+6HCl\rightarrow2RCl_3+3H_2\)
Ta có: \(n_{H_2}=\dfrac{9,408}{22,4}=0,42\left(mol\right)\)
Theo PT: \(n_R=\dfrac{2}{3}n_{H_2}=0,28\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{7,56}{0,28}=27\left(g/mol\right)\)
Vậy: R là Al.
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 8,4 gam kim loại R (hóa trị không đổi) vào 200 ml dung dịch HCl 2,5M. Để trung hòa lượng axit dư sau phản ứng phải dùng 80gam dung dịch NaOH 10%
a) Xác định kim loại R
b) Trộn 2,1 gam MgCO3 và 8,4 gam R trên rồi cho tác dụng với H2SO4 đặc, nóng, dư thì thu được V lít hỗn hợp 2 khí (ở đktc) có tỉ khối so với H2 bằng 31. Xác định V
Mọi người giải cho tiết hai bài này giùm minh mới ạ
Bài 1: Cho 0,72 g một kim loại M tác dụng hết với dung dịch HCL dư thì thu được 672ml khí H2( đktc) . Xác định tên kim loại
Bài 2: Hoà tan hoàn toan 6,85 g một kim loại kiềm thổ R bằng 200ml dung dịch HCL 2M . Để trung hoà lượng axit dư cần 100ml dung dịch NaOH 3M. Xác định tên kim loại
1.
2M + 2xHCl -> 2MClx + xH2
nH2=0,03(mol)
Theo PTHH ta có:
nM=\(\dfrac{2}{x}\)nH2=\(\dfrac{0,06}{x}\)
MM=0,72:\(\dfrac{0,06}{x}=12x\)
Ta thấy với x=2 thì M=24 (t/m)
Vậy M là magie,KHHH là Mg
Đúng 0
Bình luận (2)
2.
R + 2HCl -> RCl2 + H2 (1)
NaOH + HCl -> NaCl + H2O (2)
nHCl=0,2.2=0,4(mol)
nNaOH=0,3(mol)
Theo PTHH 2 ta có:
nNaOH=nHCl(2)=0,3(mol)
nHCl(1)=0,4-0,3=0,1(mol)
Theo PTHH 1 ta có:
\(\dfrac{1}{2}\)nHCl=nR=0,05(mol)
MR=\(\dfrac{6,85}{0,05}=137\)
Vậy R là bari,KHHH là Ba
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 42,6 gam hỗn hợp X gồm một kim loại kiềm và một kim loại kiềm thổ có tỉ lệ mol tương ứng là 5 : 4 vào 500 ml dung dịch HCl 1M thu được dung dịch Y và 17,472 lít khí (đktc).a) Xác định thành phần % về khối lượng mỗi kim loại trong X.b) Dẫn từ từ khí CO2 vào dung dịch Y, tính thể tích khí CO2 (đktc) cần dùng để thu được lượng kết tủa lớn nhất.
Đọc tiếp
Hòa tan hoàn toàn 42,6 gam hỗn hợp X gồm một kim loại kiềm và một kim loại kiềm thổ có tỉ lệ mol tương ứng là 5 : 4 vào 500 ml dung dịch HCl 1M thu được dung dịch Y và 17,472 lít khí (đktc).
a) Xác định thành phần % về khối lượng mỗi kim loại trong X.
b) Dẫn từ từ khí CO2 vào dung dịch Y, tính thể tích khí CO2 (đktc) cần dùng để thu được lượng kết tủa lớn nhất.