Đốt cháy hoàn toàn M(gam) hợp chất B cần dùng 10,08 lít O2 (ĐKTC).Sau phản ứng thu được 13,2 gam CO2 và 7,2 gam nước.
A/ Xác định giá trị M và cho biết B cho nguyên tố nào tạo ra.
B/ Lập CT phân tử của B.
Đốt cháy hoàn toàn một hợp chất X, cần dùng hết 10,08 lít O2 (đktc). Sau phản ứng, chỉ thu được 13,2 gam khí CO2 và 7,2 gam nước.
a/ Tính khối lượng chất X đã phản ứng.
b/ Tìm công thức hoá học của X (biết công thức dạng đơn giản chính là công thức hoá học của X).
c/ Viết phương trình hoá học đốt cháy chất X ở trên.
\(n_C=\dfrac{13,2}{44}=0,3\left(mol\right)\\ n_H=2.\dfrac{7,2}{18}=0,8\left(mol\right)\\ n_O=2.\dfrac{13,2}{44}+\dfrac{7,2}{18}-\dfrac{10,08}{22,4}=0,1\left(mol\right)\\ m_X=0,3.12+0,8+0,1.16=6\left(g\right)\\ CTPT:C_xH_yO_z\\ \Rightarrow x:y:z=0,3:0,8:0,1=3:8:1\)
Mà CTHH của X là CTDGN
=> CTHH của X: C3H8O
PTHHH: 2C3H8O + 9O2 ---to---> 6CO2 + 8H2O
Đốt cháy hoàn toàn m gam một hợp chất X, cần dùng hết 10,08 lít khí oxi (ở đktc). Sau khi phản ứng kết thúc, chỉ thu được 13,2 gam khí CO2 và 7,2 gam H2O.
a. Tìm m và xác định công thức hóa học của X (biết công thức dạng đơn giản chính là công thức hóa học của X).
b. Viết phương trình hóa học của phản ứng đốt cháy X.
a, \(n_{O_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
Theo ĐLBT KL, có: mX + mO2 = mCO2 + mH2O
⇒ m = mX = 13,2 + 7,2 - 0,45.32 = 6 (g)
Ta có: \(n_{CO_2}=\dfrac{13,2}{44}=0,3\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\Rightarrow n_H=0,4.2=0,8\left(mol\right)\)
⇒ mC + mH = 0,3.12 + 0,8.1 = 4,4 (g) < mX
→ X gồm C, H và O.
⇒ mO = 6 - 4,4 = 1,6 (g) \(\Rightarrow n_O=\dfrac{1,6}{16}=0,1\left(mol\right)\)
Gọi CTPT của X là CxHyOz
⇒ x:y:z = 0,3:0,8:0,1 = 3:8:1
Vậy: CTPT của X là C3H8O
b, \(C_3H_8O+\dfrac{9}{2}O_2\underrightarrow{t^o}3CO_2+4H_2O\)
Đốt cháy hoàn toàn một hợp chất A cần dùng vừa hết 10,08 lít oxi ở đktc, sau phản ứng thu được 4,72 lít CO2 ở đktc và 7,2 gam nước.
a) Tính số nguyên tử mỗi loại trong 1 mol A.
b) Tìm CTPT của A biết MA=60g/mol.
*Sửa đề: "6,72 lít CO2"
Bảo toàn nguyên tố: \(\left\{{}\begin{matrix}n_C=n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\n_H=2n_{H_2O}=2\cdot\dfrac{7,2}{18}=0,8\left(mol\right)\end{matrix}\right.\)
Ta có: \(n_{O_2\left(p.ứ\right)}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
Ta thấy \(2n_{O_2}< 2n_{CO_2}+n_{H_2O}\) \(\Rightarrow\) Trong A có Oxi
Bảo toàn Oxi: \(n_{O\left(trong.A\right)}+2n_{O_2}=2n_{CO_2}+n_{H_2O}\) \(\Rightarrow n_O=0,1\left(mol\right)\)
Số nguyên tử C trong A là: \(0,3\cdot6\cdot10^{23}=1,8\cdot10^{23}\)
Số nguyên tử H trong A là: \(0,8\cdot6\cdot10^{23}=4,8\cdot10^{23}\)
Số nguyên tử O trong A là: \(0,1\cdot6\cdot10^{23}=6\cdot10^{22}\)
Xét tỉ lệ: \(C:H:O=0,3:0,8:0,1=3:8:1\)
\(\Rightarrow\) CTPT của A là (C3H8O)n
Mà \(M_A=60\) \(\Rightarrow n=1\)
Vậy CTPT của A là C3H8O
Hỗn hợp X gồm 1 ancol đơn chức và 1 este đơn chức (mạch hở, phân tử có cùng số nguyên tử cacbon). Đốt cháy hoàn toàn m gam X cần dùng vừa đủ V lít khí O2 ở đktc, thu được 10,08 lít CO2 (đktc) và 7,2 gam H2O. Mặt khác, m gam X phản ứng với dung dịch NaOH dư, thu được 0,15 mol hỗn hợp ancol. Giá trị của V gần nhất với
A. 11,8
B. 12,9
C. 24,6
D. 23,5
Hỗn hợp X gồm 1 ancol đơn chức và 1 este đơn chức (mạch hở, cùng số nguyên tử cacbon). Đốt cháy hoàn toàn m gam X cần dùng vừa đủ V lít khí oxi (đktc) thì thu được 10,08 lít CO2 (đktc) và 7,2 gam H2O. Mặt khác m gam X phản ứng với dung dịch NaOH dư thu được 0,15 mol hỗn hợp ancol. Giá trị gần nhất với giá trị của V là
A. 11,8
B. 12,9
C. 24,6
D. 23,5
Câu 31: Đốt cháy hoàn toàn 4,4 gam hợp chất hữu cơ A thu được 13,2 gam khí CO2 và 7,2 gam nước.
a) A có những nguyên tố nào?
b) Tìm công thức phân tử của A biết khối lượng mol của A bằng 44 gam/mol
c) Viết CTCT đầy đủ và thu gọn của A.
a, Bảo toàn C: \(n_C=\dfrac{13,2}{44}=0,3\left(mol\right)\)
Bảo toàn H: \(n_H=\dfrac{2.7,2}{18}=0,8\left(mol\right)\)
Xét mH + mC = 0,3.12 + 0,8 = 4,4 => A chỉ có C và H
b, CTPT CxHy
=> x : y = 0,3 : 0,8 = 3 : 8
=> (C3H8)n = 44
=> n = 1
CTPT: C3H8
c, CTCT:
\(CH_3-CH_2-CH_3\)
Bảo toàn C: \(n_C=n_{CO_2}=\dfrac{13,2}{44}=0,3mol\)
Bảo toàn H: \(n_H=2.n_{H_2O}=2.\dfrac{7,2}{18}=0,8mol\)
\(n_O=\dfrac{4,4-\left(0,3.12+0,8\right)}{16}=0mol\)
=> A gồm C và H
\(CTHH:C_xH_y\)
\(x:y=0,3:0,8=3:8\)
\(CTĐG:\left(C_3H_8\right)n=44\)
\(\Leftrightarrow n=1\)
\(\rightarrow CTPT:C_3H_8\)
CTCT đầy đủ:
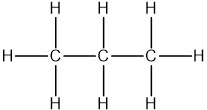
CTCT thu gọn:\(CH_3-CH_2-CH_3\)
Câu 3 :
1. Để khử hoàn toàn 47,2 gam hỗn hợp CuO , FeO, Fe3O4 cần dùng V lít khí H2 (ở đktc). Sau phản ứng thu được m gam kim loại và 14,4 gam nước.
a) Viết PTHH xảy ra?
b) Tính giá trị m và V?
2. Đốt cháy hoàn toàn 23 gam hợp chất A cần 33,6 lít ôxi (đktc) và thu được thể tích CO2 bằng 2/3 thể tích hơi nước . Xác định CTHH của A. Biết rằng tỉ khối hơi của A so với khí ôxi là 1,4375.
Hỗn hợp X gồm 1 ancol đơn chức và 1 este đơn chức ( mạch hở, cùng số nguyên tử cacbon). Đốt cháy hoàn toàn m gam X vần dùng vừa đủ V lít khí oxi (đktc) thì thu được 10,08 lít CO2 (đktc) và 7,2 gam H2O. Mặt khác m gam X phản ứng với dung dịch NaOH dư thu được 0,15 mol hỗn hợp ancol. Giá trị gần nhất với giá trị của V là
A. 11,8
B. 12,9
C. 24,6
D. 23,5
Đáp án A
Gọi CTCT của ancol: CxHyO: a (mol)
CTCT của este: CxHzO2: b (mol)
nCO2 = 0,45 (mol) ; nH2O = 0,4 (mol)
Ta có: 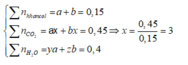
=> CTCT của ancol: C3HyO
CTCT của este: C3HzO2
Vì đốt cháy hh X cho nCO2> nH2O và hh X + NaOH → 0,15 hỗn hợp ancol
=> ancol phải không no, có 1 liên kết pi ; este phải no đơn chức
Ancol: C3H4O: 0, 05 (mol) ( nancol = nCO2 – nH2O)
Este: C3H6O2: 0,1 (mol)
BTNT O:
nO2 = (2nCO2 + nH2O – nO( trong X))/2 = [2.0,45 + 0,4 – (0,05 .1 + 0,1.2)]/2 = 0,525 (mol)
=> VO2 = 0,525.22,4= 11,76(lít) ≈ 11,8 (lít)
Đốt cháy hoàn toàn hợp chất hữu cơ A cần dùng 6,72 lít O 2 (đktc). Sau khi kết thúc phản ứng thu được 13,2 gam C O 2 và 5,4 gam H 2 O . Xác định CTPT của A biết d A / H e = 15
A. C 2 H 4 O
B. C 2 H 4 O 2
C. C 2 H 4
D. C 4 H 8 O
n C O 2 = 13,2 44 = 0,3 m o l → n C = 0,3 m o l ; m C = 3,6 g a m . n H 2 O = 5,4 18 = 0,3 m o l → n H = 0,6 m o l ; m H = 0,6 g a m .


Vậy A có công thức đơn giản nhất là C H 2 O n .
Lại có M A = 15 . 4 = 60 ( g / m o l ) → n = 2 thỏa mãn.
A là C 2 H 4 O 2 .
⇒ Chọn B.