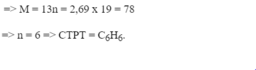Hãy thiết lập công thức phân tử hợp chất hữu cơ biết rằng khi đốt cháy hoàn toàn 10 mg hợp chất hữu cơ đó sinh ra 33,85 mg CO2 và 6,95 mg H2O. Tỉ khối hơi của hợp chất đó đối với không khí là 2,69.

Những câu hỏi liên quan
Đốt cháy hoàn toàn hợp chất hữu cơ gồm C,H, Cl sinh ra 112 cm3 CO2 (do đktc) và 0,09 gam H2O cũng được chất hữu cơ đó cho tác dụng AgNO3 thì thu được 1,435 g AgCl lập công thức phân tử chất hữu cơ biết rằng tỉ khối hơi so với he là 21,35
Giúp em vs ạ em cảm ơn
Gọi CTHH là \(C_xH_yCl_z\)
\(V=112cm^2=0,112l\Rightarrow n_{CO_2}=0,005mol\Rightarrow n_C=0,005mol\)
\(n_{H_2O}=\dfrac{0,09}{18}=0,005mol\Rightarrow n_H=0,01mol\)
\(n_{AgCl}=\dfrac{1,435}{143,5}=0,01mol\Rightarrow n_{Cl}=0,01mol\)
\(x:y:z=n_C:n_H:n_{Cl}=0,005:0,01:0,01=1:2:2\)
\(\Rightarrow\)CTĐGN: \((CH_2Cl_2)_n\)
Mà \(M=21,35\cdot4=85đvC\)
\(\Rightarrow\left(12+2+2\cdot35,5\right)\cdot n=85\)
\(\Rightarrow n=1\)
Vậy CTPT tìm được là \(CH_2Cl_2\)
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn 7,8 g hợp chất hữu cơ X thu được 26,4 g C O 2 và 5,4 g H 2 O . Tỉ khối hơi của X so với không khí là 2,69 ( M k k = 29). Lập công thức phân tử cúa X (H=1, C=12, O=16)
Đốt cháy hoàn toàn m gam hỗn hợp chất hữu cơ A chỉ thu được a gam CO2 và b gam H2O. Biết 11b 3a và 7m 3(a+b). Mặt khác ta có tỉ khối hơi của chất A đối với không khí nhỏ hơn 3. Công thức phân tử của chất hữu cơ A là: A. C3H8 B. C2H6 C. C3H4O2 D. C3H6O2
Đọc tiếp
Đốt cháy hoàn toàn m gam hỗn hợp chất hữu cơ A chỉ thu được a gam CO2 và b gam H2O. Biết 11b = 3a và 7m = 3(a+b). Mặt khác ta có tỉ khối hơi của chất A đối với không khí nhỏ hơn 3. Công thức phân tử của chất hữu cơ A là:
A. C3H8
B. C2H6
C. C3H4O2
D. C3H6O2
Đáp án C
Vì đốt cháy A thu được CO2 và H2O nên A chứa C, H, có thể có O.
Khi đó gọi công thức phân tử của A là CxHyOz
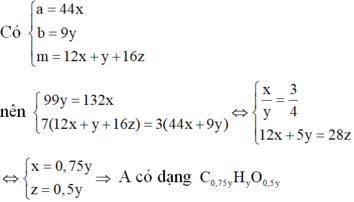
![]()
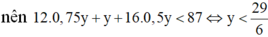
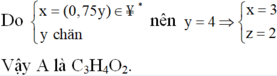
Nhận xét: Khi làm đến bước x : y = 3 :4 và kết hợp với quan sát 4 đáp án, ta có thể kết luận ngay A là C3H4O2.
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 2,2g hợp chất hữu cơ A thu được 6,6g CO2 và 3,6g H2O. Biết A có tỉ khối so với khí H2 là 22. Xác định công thức phân tử của hợp chất hữu cơ.
\(n_{CO_2}=\dfrac{6,6}{44}=0,15\left(mol\right)\)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
Bảo toán C: nC(A) = 0,15 (mol)
Bảo toàn H: nH(A) = 0,2.2 = 0,4 (mol)
=> \(n_O=\dfrac{2,2-0,15.12-0,4.1}{16}=0\left(mol\right)\)
Xét nC : nH = 0,15 : 0,4 = 3:8
=> CTPT: (C3H8)n
Mà MA = 22.2 = 44(g/mol)
=> n = 1
=> CTPT: C3H8
Đúng 4
Bình luận (0)
giúp em câu này với mn ;
Tìm CTĐGN và CTPT cua mỗi chất trong từng trường hợp a) đốt cháy hoàn toàn 7,8gam chất hữu cơ Y sinh ra 26,4g CO2 và 5,4gam h2o tỉ khối hơi của Y đối với không khí 2,69. b) kết quả phân tích các nguyên tố trong nicotin nhu sau 74%C 8,65 %H ,17,35 % N xác định CTĐGN VÀ CTPT của nicotin . biết nicotin có khối lượng mol phân tử là 162
Đốt cháy hoàn toàn 9 gam một hh chất hữu cơ A thì thu được 13,2 gam khí cacboic và 5,4 gam nước .Phân tử khối của hợp chất hữu cơ là 180.Hãy xác định công thức phân tử của hợp chất hữu cơ đó
Xem chi tiết
Ta có: \(n_{CO_2}=\dfrac{13,2}{44}=0,3\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\Rightarrow n_H=0,3.2=0,6\left(mol\right)\)
⇒ mC + mH = 0,3.12 + 0,6.1 = 4,2 (g) < mA
⇒ A có các nguyên tố C, H và O.
⇒ mO = 9 - 4,2 = 4,8 (g)
\(\Rightarrow n_O=\dfrac{4,8}{16}=0,3\left(mol\right)\)
Giả sử CTPT của A là CxHyOz. (x, y, z nguyên dương)
⇒ x : y : z = 0,3 : 0,6 : 0,3 = 1: 2 : 1
⇒ CTĐGN của A là (CH2O)n (n nguyên dương)
Mà: MA = 180 (g/mol)
\(\Rightarrow n=\dfrac{180}{12+2+16}=6\left(tm\right)\)
Vậy: A là C6H12O6.
Bạn tham khảo nhé!
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 4,8 gam một hợp chất hữu cơ A sau phản ứng thu được 6,6 gam CO2 và 5,4 gam H2O. Biết rằng khi hóa hơi ở điều kiện tiêu chuẩn 2,24 lít khí A nặng 3,2 gam. a) Xác định công thức phân tử của hợp chất hữu cơ A. b) Biết rằng A có phản ứng với Na. Tính thể tích khí hidro (đktc) thoát ra khi cho lượng chất A ở trên phản ứng hoàn toàn với Na dư. (Na = 23, O = 16, C = 16, H = 1)
a)
n CO2 = 6,6/44 = 0,15(mol) => n C = n CO2 = 0,15(mol)
n H2O = 5,4/18 = 0,3(mol) => n H = 2n H2O = 0,6(mol)
=> n O = (4,8 - 0,15.12 - 0,6)/16 = 0,15(mol)
Ta có :
n C : n H : n O = 0,15: 0,6 : 0,15 = 1 : 4 : 1
=> CTP của A là (CH4O)n
M A = (12 + 4 + 16)n = 3,2/(2,24/22,4) = 32
=> n = 1
Vậy CTPT của A là CH4O
b)
$2CH_3OH + 2Na \to 2CH_3ONa + H_2$
n CH3OH = n CO2 = 0,15(mol)
=> n H2 = 1/2 n CH3OH = 0,075(mol)
=> V H2 = 0,075.22,4 = 1,68(lít)
Đúng 2
Bình luận (0)
Một hợp chất hữu cơ X có tỉ khối so với không khí bằng bằng 2. Đốt cháy hoàn toàn A bằng khí O2 thu được CO2 và H2O. Có bao nhiêu công thức phân tử phù hợp với X A. 1 B. 4 C. 2 D. 3
Đọc tiếp
Một hợp chất hữu cơ X có tỉ khối so với không khí bằng bằng 2. Đốt cháy hoàn toàn A bằng khí O2 thu được CO2 và H2O. Có bao nhiêu công thức phân tử phù hợp với X
A. 1
B. 4
C. 2
D. 3
Đốt cháy hoàn toàn 6g hợp chất hữu cơ X thì thu được 4,48 lit khí CO2 (đktc) và 3,6g H20, biết tỉ khối hơi của X so với hidro là 30. Công thức phân tử của X là ?
PTPƯ: \(X+O_2\underrightarrow{t^o}CO_2+H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_C=0,2mol\\n_H=0,4mol\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_C=0,2\cdot12=2,4\left(g\right)\\m_H=0,4\cdot1=0,4\left(g\right)\end{matrix}\right.\)
Ta thấy \(m_C+m_H=2,4+0,4< m_X=6\)
\(\Rightarrow\) Trong X có Oxi
\(\Rightarrow m_O=6-2,4-0,4=3,2\left(g\right)\) \(\Rightarrow n_O=\dfrac{3,2}{16}=0,2\left(mol\right)\)
Xét tỉ lệ \(C:H:O=0,2:0,4:0,2=1:2:1\)
\(\Rightarrow\) CTPT của X là \(\left(CH_2O\right)_n\)
Mà \(M_X=30\cdot2=60\)
\(\Rightarrow n=\dfrac{60}{30}=2\) \(\Rightarrow\) X là C2H4O2
Đúng 1
Bình luận (0)