Thực phẩm bảo quản trong tủ lạnh sẽ giữ được lâu hơn (a), khi nấu một loại thực phẩm bằng nồi áp suất sẽ nhanh chín hơn (b), bệnh nhân sẽ dễ hô hấp hơn khi dùng oxygen từ bình chứa khí oxygen so với từ không khí(c),…
Những yếu tố nào ảnh hưởng đến tốc độ của các quá trình biến đổi trên?



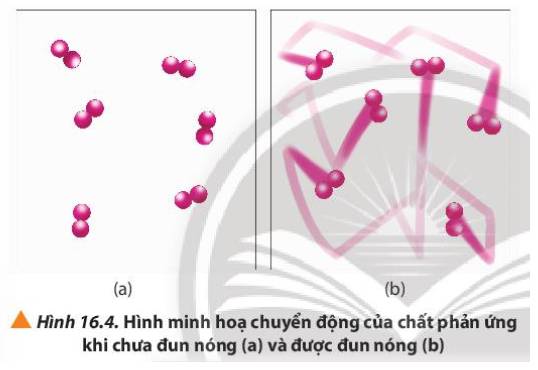


(a) Ảnh hưởng của nhiệt độ
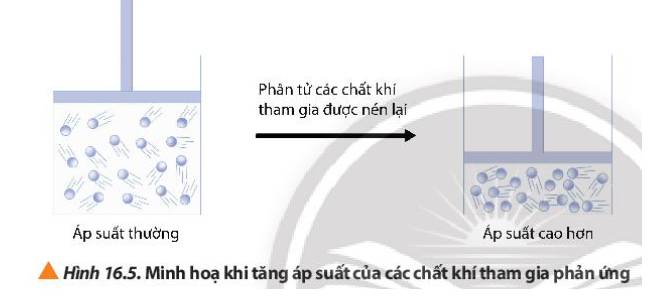
(b) Ảnh hưởng của áp suất
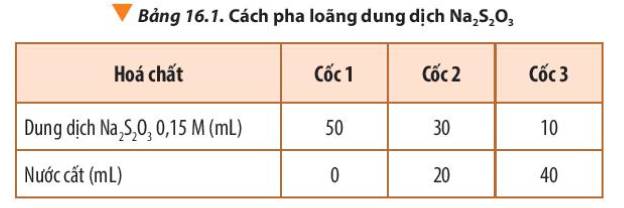
(c) Ảnh hưởng của nồng độ