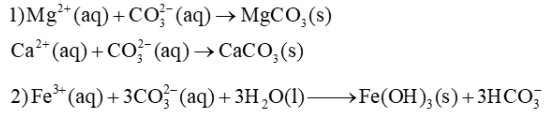Viết các phương trình hoá học để giải thích cơ sở các ứng dụng sau:
a) Viên sủi chứa NaHCO3 và acid hữu cơ (viết gọn là HX) có khả năng tạo bọt khí khi hoà tan vào nước.
b) Trong kĩ thuật xử lí nước, NaHCO3 được sử dụng để điều chỉnh pH khi nước dư acid (H+).