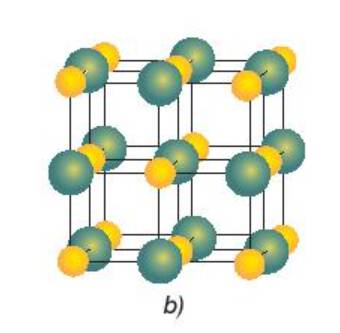
Hợp chất NaCl nóng chảy ở nhiệt độ cao và có khả năng dẫn điện khi nóng chảy hoặc khi hòa tan trong dung dịch. Yếu tố nào trong phân tử NaCl gây ra các tính chất trên?
Bài 11: Liên kết ion
Mở đầu (SGK Kết nối tri thức và cuộc sống trang 51)
Thảo luận (1)
Câu hỏi 1 (SGK Kết nối tri thức và cuộc sống trang 52)
Hoàn thành các sơ đồ tạo thành ion sau:
a) Li → Li+ + ?
b) Be → ? + 2e
c) Br + ? → Br-
d) O + 2e → ?
Thảo luận (1)Hướng dẫn giải`a)Li -> Li^[+] + 1e`
`b)Be -> Be^[2+] + 2e`
`c)Br + 1e -> Br^[-]`
`d)O+2e -> O^[2-]`
(Trả lời bởi 2611)
Câu hỏi 2 (SGK Kết nối tri thức và cuộc sống trang 52)
Viết cấu hình electron của các ion K+, Mg2+, F-, S2-. Mỗi cấu hình đó giống với cấu hình electron của nguyên tử khí hiếm nào?
Thảo luận (1)Hướng dẫn giảiK+( e = 18): 1s22s22p63s23p6 => Cấu hình electron giống nguyên tử Ar.
Mg2+(e =10): 1s22s22p6 => Cấu hình electron giống nguyên tử Ne.
F- (e =10): 1s22s22p6 => Cấu hình electron giống nguyên tử Ne.
S2- (e = 18): 1s22s22p63s23p6 => Cấu hình electron giống nguyên tử Ar.
(Trả lời bởi Mai Trung Hải Phong)
Câu hỏi 3 (SGK Kết nối tri thức và cuộc sống trang 52)
Vì sao một ion O2- kết hợp được với hai ion Li+?
Thảo luận (1)Hướng dẫn giảiQuá trình tạo thành ion của O và Li:
O + 2e → O2-
Li → Li+ + 1e
Tổng điện tích của các ion hình thành nên hợp chất luôn bằng 0.
(Trả lời bởi Mai Trung Hải Phong)
Câu hỏi 4 (SGK Kết nối tri thức và cuộc sống trang 52)
Cho các ion: Na+ , Mg2+, O2-, Cl-. Những ion nào có thể kết hợp với nhau tạo thành liên kết ion?
Thảo luận (1)Hướng dẫn giảiNhững ion có thể kết hợp với nhau là:
`@ Na^[+]` và `O^[2-]`
`@Na^[+]` và `Cl^[-]`
`@Mg^[2+]` và `O^[2-]`
`@Mg^[2+]` và `Cl^[-]`
(Trả lời bởi 2611)
Câu hỏi 5 (SGK Kết nối tri thức và cuộc sống trang 52)
Mô tả sự tạo thành liên kết ion trong:
a) Calcium oxide
b) Magnesium chloride.
Thảo luận (1)Hướng dẫn giải
Hoạt động 1 (SGK Kết nối tri thức và cuộc sống trang 53)
Lắp ráp mô hình tinh thể NaClChuẩn bị: bộ mô hình tinh thể NaCl.Tiến hành:- Chọn hình cầu có màu sắc khác nhau đại diện cho ion Na+ và ion Cl-.- Lắp các hình cầu và que nối theo mẫu (Hình 11.1b).Quan sát mô hình và xác định số ion gần nhất bao quanh một ion trái dấu ở giữa mô hình.
Đọc tiếp
Lắp ráp mô hình tinh thể NaCl
Chuẩn bị: bộ mô hình tinh thể NaCl.
Tiến hành:
- Chọn hình cầu có màu sắc khác nhau đại diện cho ion Na+ và ion Cl-.
- Lắp các hình cầu và que nối theo mẫu (Hình 11.1b).
Quan sát mô hình và xác định số ion gần nhất bao quanh một ion trái dấu ở giữa mô hình.
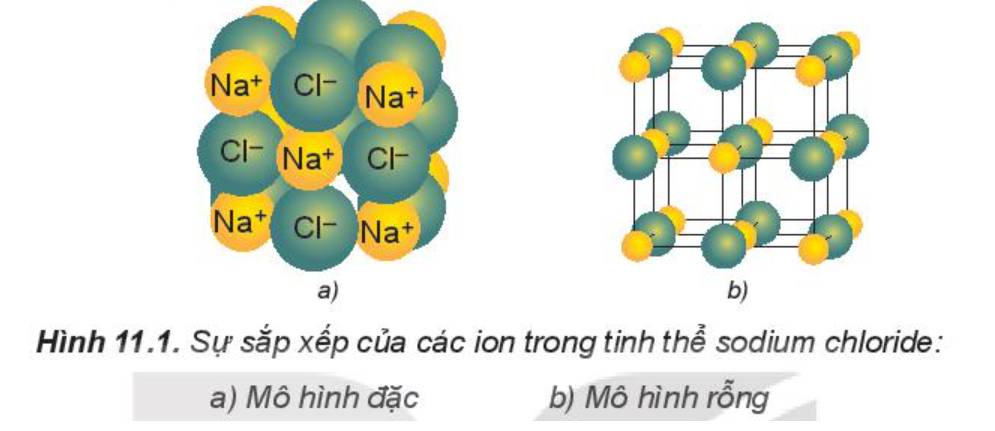
Thảo luận (1)Hướng dẫn giảiMô hình thu được tương tự hình
- Trong tinh thể sodium chloride, mỗi ion sodium được bao quanh bởi 6 ion chloride gần nhất và mỗi ion chloride cũng được bao quanh bởi 6 ion sodium gần nhất.
(Trả lời bởi Mai Trung Hải Phong)
Hoạt động 2 (SGK Kết nối tri thức và cuộc sống trang 54)
Thử tính dẫn điện của hợp chấtChuẩn bị: muối ăn dạng hạt, dung dịch muối ăn bão hòa, dung dịch nước đường, dụng cụ thử tính dẫn điện, cốc thủy tinh.Tiến hành: Sử dụng dụng cụ thử tính dẫn điện như Hình 11.3, lần lượt cho chân kim loại của dụng cụ thử tính dẫn điện tiếp xúc với:- Dung dịch nước đường- Muối ăn khan.- Dung dịch muối ăn bão hòa.Nếu đèn sáng thì chất dẫn điện nếu đèn không sáng thì chất không dẫn điện.Quan sát hiện tượng và cho biết trường hợp nào dẫn điện, trường hợp nào không dẫn đ...
Đọc tiếp
Thử tính dẫn điện của hợp chất
Chuẩn bị: muối ăn dạng hạt, dung dịch muối ăn bão hòa, dung dịch nước đường, dụng cụ thử tính dẫn điện, cốc thủy tinh.
Tiến hành: Sử dụng dụng cụ thử tính dẫn điện như Hình 11.3, lần lượt cho chân kim loại của dụng cụ thử tính dẫn điện tiếp xúc với:
- Dung dịch nước đường
- Muối ăn khan.
- Dung dịch muối ăn bão hòa.
Nếu đèn sáng thì chất dẫn điện nếu đèn không sáng thì chất không dẫn điện.
Quan sát hiện tượng và cho biết trường hợp nào dẫn điện, trường hợp nào không dẫn điện. Giải thích.

Thảo luận (1)Hướng dẫn giảiHiện tượng:- Dung dịch nước đường: đèn tín hiệu không sáng. Do khi hòa tan đường trong nước không tạo ra các ion.
- Muối ăn khan: đèn tín hiệu không sáng. Do ở trạng thái rắn, các ion không di chuyển tự do được nên hợp chất ion không dẫn điện.
- Dung dịch muối ăn bão hòa: đèn tín hiệu phát sáng. Do khi muối được hòa tan vào nước, các ion chuyển động khá tự do và là tác nhân dẫn điện.
(Trả lời bởi Mai Trung Hải Phong)
Câu hỏi 6 (SGK Kết nối tri thức với cuộc sống trang 54)
a) Vì sao muối ăn có nhiệt độ nóng chảy cao (801oC)?
b) Hợp chất ion dẫn điện trong trường hợp nào? Vì sao?
Thảo luận (1)Hướng dẫn giảia) Muối ăn (NaCl) là tinh thể ion, giữa các ion Na+ và Cl- có lực hút tĩnh điện rất mạnh nên muối ăn khó nóng chảy hay có nhiệt độ nóng chảy cao.
b) Các hợp chất ion ở trạng thái nóng chảy hoặc dung dịch sẽ dẫn điện, vì:
- Khi nóng chảy hoặc tan trong nước, các ion bị tách khỏi mạng lưới tinh thể, chuyển động khá tự do và là tác nhân dẫn điện.
- Ở trạng thái rắn, các ion không di chuyển tự do được nên hợp chất ion không dẫn điện.
(Trả lời bởi Hà Quang Minh)
Em có thể? (SGK Kết nối tri thức với cuộc sống trang 54)
Giải thích một số tính chất đặc trưng của hợp chất ion và một số ứng dụng phổ biến của chúng trong đời sống.
Thảo luận (1)Hướng dẫn giải- Trong tinh thể ion, giữa các ion có lực hút tĩnh điện rất mạnh nên các hợp chất ion thường là chất rắn, khó nóng chảy, khó bay hơi ở điều kiện thường.
Ví dụ: Nhiệt độ nóng chảy của MgO là 2800°C.
- Các hợp chất ion thường tan nhiều trong nước. Khi tan trong nước, các ion bị tách khỏi mạng lưới tinh thể, chuyển động khá tự do và là tác nhân dẫn điện. Ở trạng thái nóng chảy, hợp chất ion dẫn điện.
- Do lực hút tĩnh điện rất mạnh giữa các ion nên các tinh thể ion khá rắn chắc, nhưng khá giòn.
⇒ Đây là tính chất đặc trưng của tinh thể ion.
Một số ứng dụng phổ biến của hợp chất ion trong đời sống:
- Potassium hydroxide là hợp chất ion được dùng làm chất dẫn điện trong pin alkaline (pin kiềm).
- Máy lọc không khí tạo ion âm.
(Trả lời bởi Hà Quang Minh)