a)
- Kim loại có xu hướng nhường electron, phi kim có xu hướng nhận electron
=> Phi kim sẽ lấy electron của kim loại để cả phi kim và kim loại đạt cấu hình electron bền vững của khí hiếm
- Ví dụ: NaCl
+ Na: có 1 electron ở lớp ngoài cùng
+ Cl: có 7 electron ở lớp ngoài cùng
=> Na sẽ nhường 1 electron và Cl sẽ nhận 1 electron của Na để đạt cấu hình có 8 electron ở lớp vỏ ngoài cùng
b)
- Hai phi kim đều có xu hướng nhận thêm electron
=> Cả 2 phi kim sẽ bỏ ra electron để góp chung
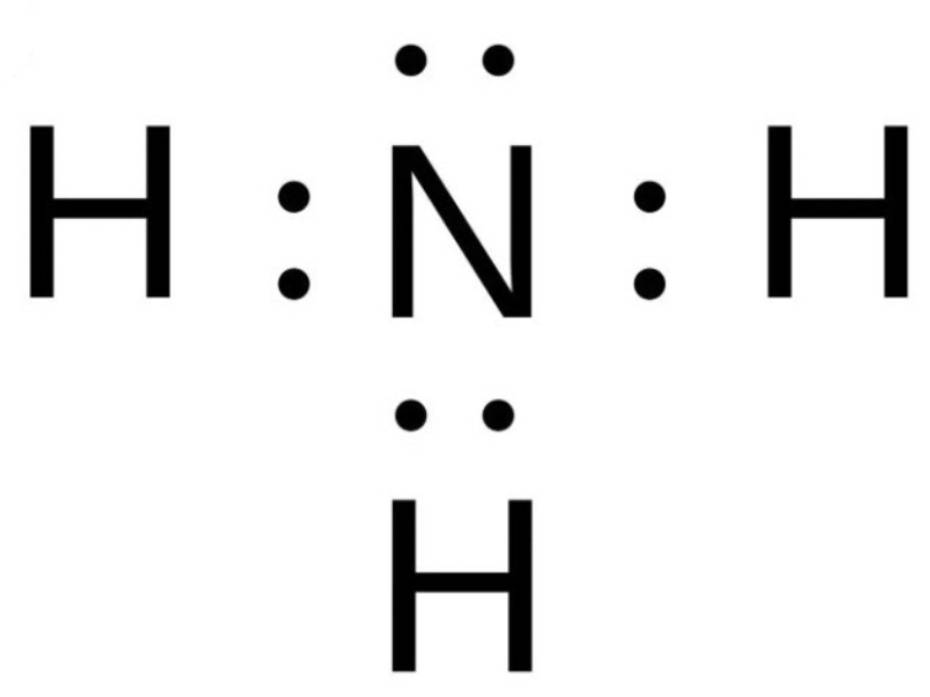
Ví dụ: N2 tác dụng với H2 tạo thành NH3
+ N: có 5 electron ở lớp ngoài cùng => Cần nhận thêm 3 electron
+ H: có 1 electron ở lớp ngoài cùng => Cần nhận thêm 1 electron
=> N sẽ bỏ ra 3 electron và 3H mỗi H bỏ ra 1 electron để góp chung