Bài 3. Đơn chất nitrogen
Các câu hỏi tương tự
Viết phương trình hoá học chứng minh tính oxi hoá và tính khử của nitrogen. Cho biết số oxi hoá của nitrogen thay đổi như thế nào trong các phản ứng hoá học đó.
Quan sát Hình 3.3 và từ dữ kiện năng lượng liên kết trong phân tử N2 dự đoán về độ bền phân tử và khả năng phản ứng của nitrogen ở nhiệt độ thường.

Nitrogen là khí có hàm lượng lớn nhất trong không khí, có vai trò cung cấp đạm tự nhiên cho cây trồng. Nitrogen có tính chất gì và có những ứng dụng nào trong cuộc sống?
Quan sát Hình 3.5 và dựa vào các tính chất của nitrogen, hãy giải thích vì sao nitrogen có những ứng dụng đó.

Nitrogen nặng hơn hay nhẹ hơn không khí. Tại sao?
Người ta có thể thu khí nitrogen trong phòng thí nghiệm bằng phương pháp đẩy nước. Hãy giải thích điều này.
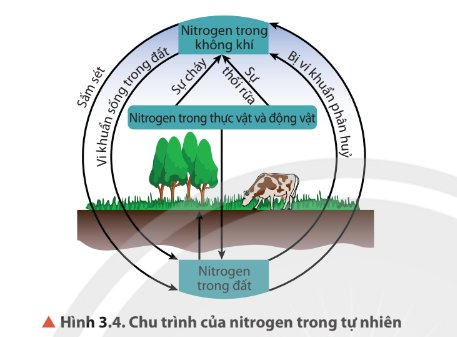
Quan sát Hình 3.4, cho biết con người có thể can thiệp vào chu trình của nitrogen trong tự nhiên bằng cách nào. Nếu sự can thiệp đó vượt ngưỡng cho phép thì ảnh hưởng gì đến môi trường?
Dựa vào giá trị năng lượng liên kết (Eb), hãy dự đoán ở điều kiện thường, chất nào (nitrogen, hydrogen, oxygen, chlorine) khó và dễ tham gia phản ứng hoá học nhất. Vì sao?begin{array}{l}{rm{a) }}{{rm{N}}_{rm{2}}}{rm{ (g) }} to {rm{ 2N (g) }}{{rm{E}}_{rm{b}}}{rm{ 945 kJ/mol}}{rm{b) }}{{rm{H}}_{rm{2}}}{rm{ (g) }} to {rm{ 2H (g) }}{{rm{E}}_{rm{b}}}{rm{ 432 kJ/mol}}{rm{c) }}{{rm{O}}_{rm{2}}}{rm{ (g) }} to {rm{ 2O (g) }}{{rm{E}}_{rm{b}}}{rm{ 498 kJ/mol}...
Đọc tiếp
Dựa vào giá trị năng lượng liên kết (Eb), hãy dự đoán ở điều kiện thường, chất nào (nitrogen, hydrogen, oxygen, chlorine) khó và dễ tham gia phản ứng hoá học nhất. Vì sao?
\[\begin{array}{l}{\rm{a) }}{{\rm{N}}_{\rm{2}}}{\rm{ (g) }} \to {\rm{ 2N (g) }}{{\rm{E}}_{\rm{b}}}{\rm{ = 945 kJ/mol}}\\{\rm{b) }}{{\rm{H}}_{\rm{2}}}{\rm{ (g) }} \to {\rm{ 2H (g) }}{{\rm{E}}_{\rm{b}}}{\rm{ = 432 kJ/mol}}\\{\rm{c) }}{{\rm{O}}_{\rm{2}}}{\rm{ (g) }} \to {\rm{ 2O (g) }}{{\rm{E}}_{\rm{b}}}{\rm{ = 498 kJ/mol}}\\{\rm{d) C}}{{\rm{l}}_{\rm{2}}}{\rm{ (g) }} \to {\rm{ 2Cl (g) }}{{\rm{E}}_{\rm{b}}}{\rm{ = 243 kJ/mol}}\end{array}\]
Câu hỏi 2: Ngoài đơn chất nitrogen, thì nguyên tố nitrogen còn tồn tại dưới dạng nào? Lấy ví dụ.





