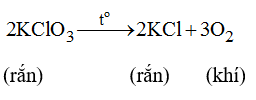\(a.2KClO_3-^{t^o}\rightarrow2KCl+3O_2\\ n_{O_2}=\dfrac{3}{2}n_{KClO_3}=0,6\left(mol\right)\\ \Rightarrow V_{O_2}=0,6.22,4=13,44\left(l\right)\\ n_{KCl}=n_{KClO_3}=0,4\left(mol\right)\\ \Rightarrow m_{KCl}=0,4.74,5=29,8\left(g\right)\)
Bài 21: Tính theo công thức hóa học
Đúng 3
Bình luận (0)
Các câu hỏi tương tự
Trong phòng thí nghiệm người ta có thể điều chế oxi bằng cách đốt nóng kali clorat: Hãy dùng phương trình hóa học trên nên trả lời những câu hỏi sau: a) Muốn điều chế được 4,48 lit khí oxi (đktc) cần dùng bao nhiêu gam KClO3 ? b) Nếu có 1,5 mol KClO3 tham gia phản ứng, sẽ được bao nhiêu gam khí oxi? c) Nếu có 0,1 mol KClO3 tham gia phản ứng, sẽ được bao nhiêu mol chất rắn và chất khí?
Đọc tiếp
Trong phòng thí nghiệm người ta có thể điều chế oxi bằng cách đốt nóng kali clorat:
Hãy dùng phương trình hóa học trên nên trả lời những câu hỏi sau:
a) Muốn điều chế được 4,48 lit khí oxi (đktc) cần dùng bao nhiêu gam KClO3 ?
b) Nếu có 1,5 mol KClO3 tham gia phản ứng, sẽ được bao nhiêu gam khí oxi?
c) Nếu có 0,1 mol KClO3 tham gia phản ứng, sẽ được bao nhiêu mol chất rắn và chất khí?
Đốt cháy 7,8 g kim loại Kali trong khí Oxi sinh ra Kali oxit. Viết phương trình hóa học của phản ứng. Tính khối lượng Kali oxit sinh ra. Tính thể tích của khí Oxi đã phản ứng ở điều kiện tiêu chuẩn. Tính thể tích không khí cần dùng biết khí oxi chiếm...
để điều chế khí O2 người ta nung nóng hỗn hợp KClO3 với MnO2 là chất xúc tác thu dược 14.9g KCl và 9.6g khí O2 theo sơ đồ sau : KClO3---- KCl+O2a) viết cong thức về khối lượng của phản ứng và viết sơ đồ trên thành phương trình hoá học b) tính khối lương KClO3 đã phản ứng c) xác định tỷ lệ phần trăm của muối kaliclorat có trong hỗn hợp
Đọc tiếp
để điều chế khí O2 người ta nung nóng hỗn hợp KClO3 với MnO2 là chất xúc tác thu dược 14.9g KCl và 9.6g khí O2 theo sơ đồ sau : KClO3----> KCl+O2
a) viết cong thức về khối lượng của phản ứng và viết sơ đồ trên thành phương trình hoá học
b) tính khối lương KClO3 đã phản ứng
c) xác định tỷ lệ phần trăm của muối kaliclorat có trong hỗn hợp
1)Tính theo công thức hóa họca) tính % khối lượng của các nguyên tố trong hợp chất:NANO3,K2CO3,AL(OH)3,SO3,FE2O3b)Một hợp chất khí X có tỉ khối đối với hidro là 8,5.Hãy xác định công thức hóa học của X biết hợp chất khí X có thành phần theo khối lượng là 82,35%N và 17,65%H2) Cho 11,2 gam Fe tác dụng với dung dịch HCL. Sản phẩm tạo thành là sắt (II) clorua và khí hidro.a) Viết phương trình hóa học xảy rab) tính thể tích khí H2 thu được ở điều kiện tiêu chuẩnc) tính khối lượng HCL đã phản ứngd) kh...
Đọc tiếp
1)Tính theo công thức hóa học
a) tính % khối lượng của các nguyên tố trong hợp chất:NANO3,K2CO3,AL(OH)3,SO3,FE2O3
b)Một hợp chất khí X có tỉ khối đối với hidro là 8,5.Hãy xác định công thức hóa học của X biết hợp chất khí X có thành phần theo khối lượng là 82,35%N và 17,65%H
2) Cho 11,2 gam Fe tác dụng với dung dịch HCL. Sản phẩm tạo thành là sắt (II) clorua và khí hidro.
a) Viết phương trình hóa học xảy ra
b) tính thể tích khí H2 thu được ở điều kiện tiêu chuẩn
c) tính khối lượng HCL đã phản ứng
d) khối lượng FeCl2 tạo thành
3) Cho 6 gam Mg phản ứng 2,24 lít khí oxi(đktc).Sau phản ứng thu được magie oxit(MgO)
a) viết phườn trình hóa học
b) tính khối lượng MgO được tạo thành
4) Cho phản ứng: 4Al+3O2-)2Al2O3. Biết cos,4.10^23 nguyên tử Al phản ứng.
a) Tính thể tích khí O2 đã tham gia phản ứng ở đktc. Từ đó tính thể tích không khí cần dùng. Biết khí oxi chiếm 1/5 thể tích của không khí.
b) Tính khối lượng Al2O3 tạo thành
#m.n_giúp_mk_nha_mk_đang_cần_gấp
Đốt cháy hoàn toàn một lượng magie trong khí oxi thì thu được 10 gam magie oxit (MgO).
a. Viết phương trình phản ứng xảy ra?
b. Tính khối lượng magie tham gia phản ứng?
c. Tính thể tích khí oxi tham gia phản ứng (ở điều kiện tiêu chuẩn)?
d. Tính khối lượng Kali pemanganat (KMnO4) cần dùng để điều chế lượng oxi ở trên?
Câu 1: Đốt cháy hoàn toàn 24,7g Bari trong không khí thu được Bari oxit.
a. Viết PTHH
b. Tính khối lượng sản phẩm tạo thành
c. Tính thể tích không khí cần dùng để đốt cháy hết lượng Bari trên ( Biết rằng thể tích khí oxi bằng 1/5 thể tích không khí )
d. Tính khối lượng Kali Clorat cần để điều chế vừa đủ lượng khí oxi dùng cho phản ứng trên
( Ba 137, O 16, K 39, C 12, Cl 35,5 )
Câu 2: Đốt cháy hoàn toàn 3,45g Natri trong không khí thu được Natri oxit.
a. Viết PTHH
b. Tính khối lượng...
Đọc tiếp
Câu 1: Đốt cháy hoàn toàn 24,7g Bari trong không khí thu được Bari oxit.
a. Viết PTHH
b. Tính khối lượng sản phẩm tạo thành
c. Tính thể tích không khí cần dùng để đốt cháy hết lượng Bari trên ( Biết rằng thể tích khí oxi bằng 1/5 thể tích không khí )
d. Tính khối lượng Kali Clorat cần để điều chế vừa đủ lượng khí oxi dùng cho phản ứng trên
( Ba = 137, O = 16, K = 39, C = 12, Cl = 35,5 )
Câu 2: Đốt cháy hoàn toàn 3,45g Natri trong không khí thu được Natri oxit.
a. Viết PTHH
b. Tính khối lượng sản phẩm tạo thành
c. Tính thể tích không khí cần dùng để đốt cháy hết lượng Natri trên ( Biết rằng thể tích khí oxi bằng 1/5 thể tích không khí )
d. Tính khối lượng Kali pemanganat cần để điều chế vừa đủ lượng khí oxi dùng cho phản ứng trên
( Na = 23, O = 16, K = 39, Mn = 55 )
Câu 3: Đốt cháy hoàn toàn 25,2g sắt trong bình chứa khí.
a. Hãy viết phương trình phản ứng xảy ra
b. Tính thể tích không khí cần dùng để đốt cháy hết lượng sắt trên ( Biết rằng thể tích khí oxi bằng 20% thể tích không khí )
c. Tính khối lượng KClO3 cần dùng để khi phân hủy thì thu được một thể tích khí O2 (ở đktc) bằng với thể tích khí O2 đã sử dụng ở phản ứng trên
Câu 4: Đốt cháy hoàn toàn 6,2g photpho trong bình chứa khí oxi tạo sản phẩm là điphotpho pentaoxit.
a. Viết phương trình hóa học của phản ứng xảy ra
b. Tính khối lượng sản phẩm thu được
c. Tính thể tích không khí cần dùng để đốt cháy hết lượng sắt trên ( Biết rằng thể tích khí oxi bằng 20% thể tích không khí )
d. Để có lượng oxi nói trên thì cần phân hủy bao nhiêu gam điphotpho pentaoxit ?
Câu 5: Đốt cháy hoàn toàn 4,8g bột lưu huỳnh trong bình chứa khí oxi tạo sản phẩm là lưu huỳnh đioxit
a. Viết phương trình hóa học của phản ứng xảy ra
b. Tính khối lượng sản phẩm thu được
c. Tính thể tích không khí cần dùng để đốt cháy hết lượng lưu huỳnh trên ( Biết rằng thể tích khí oxi bằng 20% thể tích không khí )
d. Để có lượng oxi nói trên thì cần phân hủy bao nhiêu gam kali clorat ?
* Mng bt câu nào thì help mk vs _ Thank you !!
Cho 11.2g sắt tác dụng với dung dịch HCl . khí hiđrô sinh ra được dẫn qua bột đồng 2 oxit nung nóng . Viết phương trình hóa học. b: tính thể tích khí Hiđro thu được ở điều kiện tiêu chuẩn. C: tính khối lượng đồng thu được sau phản ứng. ( Fe 56; h 1 ; cl 35,5; cu 64; O 16)
Đọc tiếp
Cho 11.2g sắt tác dụng với dung dịch HCl . khí hiđrô sinh ra được dẫn qua bột đồng 2 oxit nung nóng . Viết phương trình hóa học. b: tính thể tích khí Hiđro thu được ở điều kiện tiêu chuẩn. C: tính khối lượng đồng thu được sau phản ứng. ( Fe = 56; h = 1 ; cl= 35,5; cu = 64; O = 16)
Đốt cháy hoàn toàn 16,8 gam sắt trong bình chứa khí oxi, sau phản ứng thu được chất rắn màu nâu đỏ.
a) Viết phương trình hoá học xảy ra.
b) Tính thể tích khí oxi đã tham gia phản ứng (ở đktc).
c) Tính khối lượng sản phẩm tạo thành.
Cho 6,2 gam Na2O tác dụng với H2O thu được 0.5 lít dung dịch NaOH . a. Tính nồng độ mol của dung dịch NaOH thu được ? b. Tính khối lượng HCl dùng để trung hoà lượng NaOH trên ? ( Cho biết : Na = 23 ; O = 16 ; H = 1 ; Cl = 35,5 ) . .