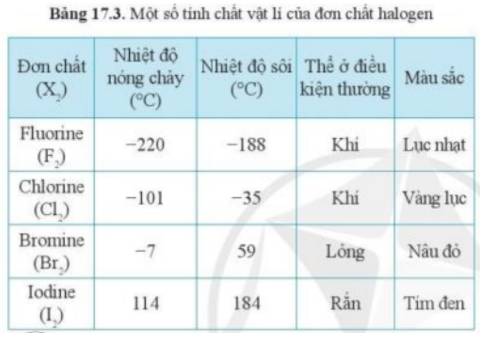
- Quan sát Bảng 17.3, nhận thấy trong điều kiện thường có Iodine (I2) là ở thể rắn
- Giải thích:
+ Khối lượng phân tử cao
+ Lực tương tác van der Waals giữa phân tử iodine mạnh
- Quan sát Bảng 17.3, nhận thấy trong điều kiện thường có Iodine (I2) là ở thể rắn
- Giải thích:
+ Khối lượng phân tử cao
+ Lực tương tác van der Waals giữa phân tử iodine mạnh
Dựa vào xu hướng biến đổi tính chất của các đơn chất halogen trong bảng 17.3, hãy dự đoán về thể (trạng thái) của đơn chất astatine ở điều kiện thường. Giải thích.
Hãy giải thích vì sao các halogen không tồn tại tự do trong tự nhiên.
Giả sử có thí nghiệm sau: Nhỏ nhanh vài giọt bromine màu nâu đỏ vào ống nghiệm chứa nước, đậy kín, lắc đều. Trong dung dịch bromine có những chất nào? Vì sao?
Vì sao nước chlorine được sử dụng phổ biến để khử trùng, sát khuẩn?
Calcium và fluorine kết hợp thành phân tử calcium fluorine, CaF2. Trong đó, nguyên tử nào đã nhường và nhường bao nhiêu electron? Nguyên tử nào đã nhận và nhận bao nhiêu electron?
Tra cứu các giá trị năng lượng liên kết ở phụ lục 2
a) Hãy tính biến thiên enthalpy chuẩn ∆rH0298 của 2 phản ứng dưới đây:
F2(g) + H2(g) → 2HF (g)
O2(g) + 2H2(g) → 2H2O(g)
b) Ở hai phản ứng trên, fluorine và oxygen đều đóng vai trò là chất oxi hóa. Dựa vào giá trị ∆rH0298, cho biết phản ứng oxi hóa – khử nào thuận lợi hơn.
- Thí nghiệm 1:
+ Nhỏ vào ống nghiệm khoảng 2 mL dung dịch sodium bromide hoặc potassium bromide loãng.
+ Nhỏ tiếp vào ống nghiệm vài giọt nước chlorine và lắc nhẹ
+ Có thể tiếp tục nhỏ vào ống nghiệm khoảng 2 mL cyclohexane
- Thí nghiệm 2:
+ Nhỏ vào ống nghiệm khoảng 2 mL dung dịch sodium iodide hoặc potassium iodide loãng
+ Nhỏ tiếp vào ống nghiệm vài giọt nước bromine loãng và lắc nhẹ. Có thể thêm tiếp vào ống nghiệm khoảng 2 mL cyclohexane
+ Thêm tiếp vào ống nghiệm vài giọt hồ tinh bột
Giải thích các hiện tượng xảy ra và minh họa bằng phương trình hóa học
Một trong những ứng dụng của chlorine trong đời sống là khử trùng nước sinh hoạt tại các nhà máy xử lí và cấp nước. Trong quá trình khử trùng, người ta phải cho một lượng chlorine dư vào nước sinh hoạt. Lượng chlorine dư trong nước sinh hoạt còn có tác dụng ngăn ngừa sự tái nhiễm của vi khuẩn trong quá trình phân phối trong đường ống dẫn nước và trữ nước tại nhà.
Theo quy chuẩn kĩ thuật quốc gia (QCVN 01 – 1: 2018/BYT), hàm lượng chlorine tự do đối với nước sạch sử dụng cho mục đích sinh hoạt từ 0,2 – 1 mgL-1. Nếu hàm lượng chlorine nhỏ hơn 0,2 – 1 mgL-1 thì không tiêu diệt hết vi khuẩn và không xử lí được hết chất hữu cơ. Ngược lại, lượng chlorine trong nước lớn hơn 1,0 mgL-1 sẽ gây dị ứng
Carbon trong than hoạt tính sẽ tương tác trực tiếp với chlorine, giúp loại bỏ chlorine và các hợp chất chlorine và các hợp chất chlorine bằng cơ chế hấp thụ bề mặt. Khi chiếu tia cực tím với cường độ cao vào nước cũng làm giảm lượng chlorine. Các máy lọc nước RO (reverse osmosis: thẩm thấu ngược) cũng có thể giúp loại bỏ lượng chlorine trong nước một cách hiệu quả
Hãy trả lời các câu hỏi sau đây:
a) Dấu hiệu nào cho thấy chlorine có trong nước sinh hoạt
b) Vì sao người ta cần cho chlorine đến dư vào nước sinh hoạt
c) Cho biết một số phương pháp có thể loại bỏ khí chlorine dư trong nước sinh hoạt.
Astatine là nguyên tố phóng xạ, được xếp dưới nguyên tố iodine trong nhóm VIIA. Thực tế, các nhà khoa học chỉ thu được đồng vị bền của astatine từ quá trình nghiên cứu về phóng xạ, đồng thời nó chỉ tồn tại khoảng 8 giờ
Dựa vào xu hướng biến đổi một số tính chất của nhóm halogen, hãy dự đoán:
a) Tính oxi hóa của nguyên tử astatine mạnh hơn hay yếu hơn so với nguyên tử iodine?
b) Đơn chất astatine có màu đậm hơn hay nhạt hơn so với đơn chất iodine?