`4FeS_2+11O_2-> 2Fe_2O_3+8SO_2`(to)
`1,44--3,96mol`
`->m_(FeS_2)=1,44.120=172,8g`
`4FeS_2+11O_2-> 2Fe_2O_3+8SO_2`(to)
`1,44--3,96mol`
`->m_(FeS_2)=1,44.120=172,8g`
Cho m gam hôn hợp sắt trong không khí khoảng 1 thời gian sau thu được 7,2 gam hỗn hợp X gồm các oxit của sắt và sắt , sau đó cho hỗn hợp X vào dd H2So4 đ thu được V So2 (đktc) có số mol phản ứng của H2So4 là 0,2 mol tìm m và V. Giải giúp em với ạ :(((
Xác định chất oxi hóa, chất khử, quá trình oxi hóa, quá trình khử và cân bằng phản ứng sau:
1. NH3 + Cl2 → N2 + HCl
2. P + H2SO4 → H3PO4 + SO2+ H2O
3. HNO3 + P → H3PO4+ NO2+ H2O
4. H2S + O2 → S + H2O
5. Al + H2SO4 đặc nóng → Al2(SO4)3 + S + H2O
6. Fe3O4 + HNO3 → Fe(NO3)3 + NO2 + H2O
7. Al + HNO3 ® Al(NO3)3 + N2 + H2O
8. KMnO4 + PH3 + H2SO4 ® MnSO4 + H3PO4 + K2SO4 + H2O
9. KMnO4 + HCl ® MnCl2 + Cl2 + KCl + H2O
10. FeO + HNO3 ® Fe(NO3)3 + NxOy + H2O
Cho phản ứng : Fe2O3 + AL => Fe + Al2O3. Khi có 1,15 mol Fe2O3 bị khử hoàn toàn thành Để thì số mol electron mà AL đã nhường là?
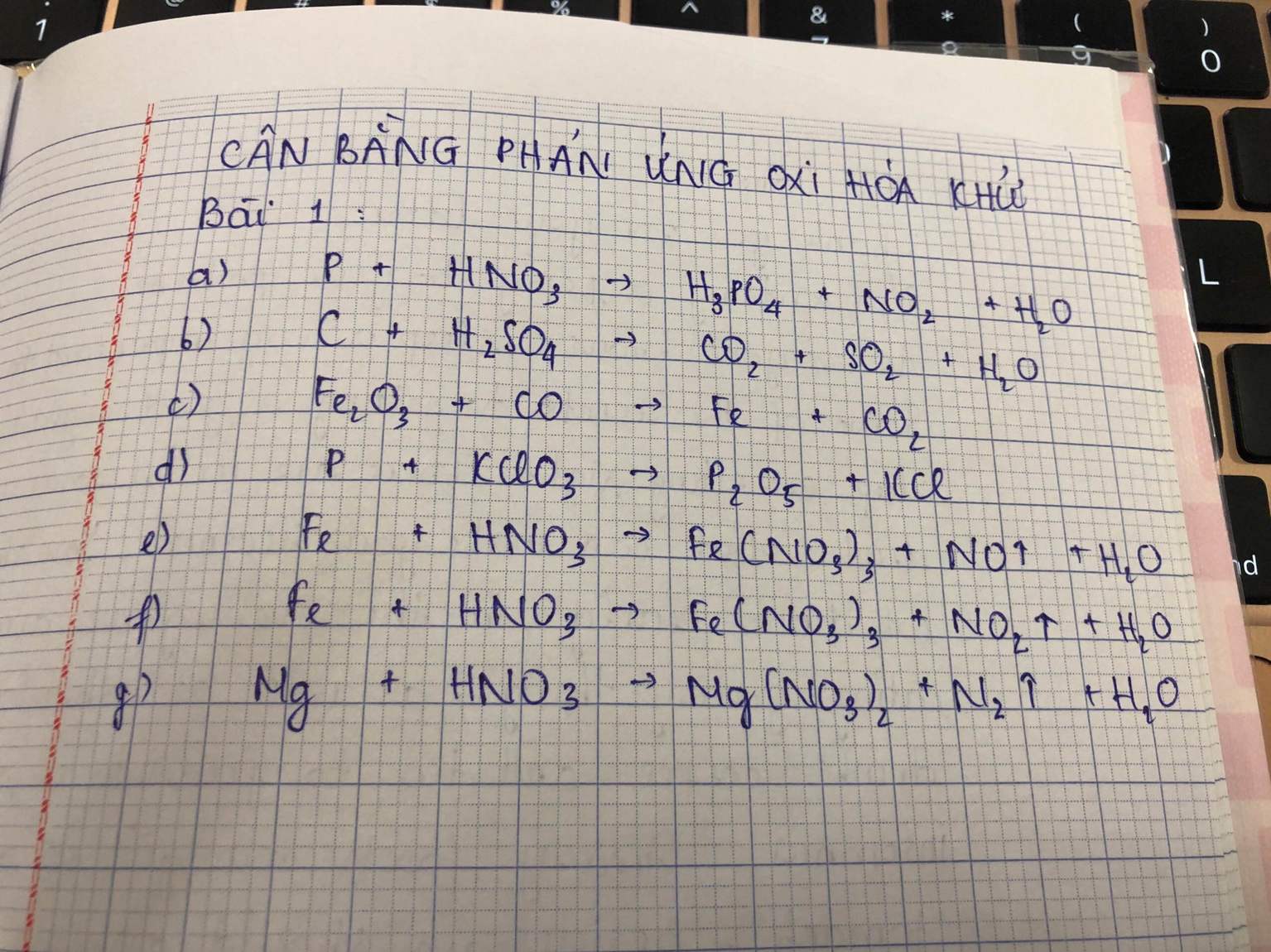
Giúp mình với ạ, mình cần gấp. Tks Làm theo các bước như này a: Trải qua bốn bước -Bước 1: Xác định số oxi hóa của các nguyên tố trong phản ứng để tìm chất khử, chất oxi hóa. -Bước 2: Viết các quá trình khử, quá trình oxi hóa cân bằng mỗi quá trình. -Bước 3: Tìm hệ số thích hợp cho chất khử, chất oxi hóa sao cho tổng số electron do chất khử nhường bằng tổng số electron do chất oxi hóa nhận -Bước 4: Đặt các hệ số của chất khử và chất oxi hóa vào sơ đồ phản ứng , từ đó tính ra hệ số của các chất khác có mặt trong phương trình hóa học . Kiểm tra cân bằng số nguyên tử của các nguyên tố và cân bằng điện tích hai vếđ ể hoàn tất việc lập phương trình hóa học của phản ứng.
Anh chị hãy cân bằng phương trình phản ứng bằng phương pháp thăng bằng electron và chỉ rõ chất oxi hóa, chất khử, quá trình oxi hóa, quá trình khử của a)KClO3 + HCl -> KCL + Cl2 + H2O
b)KMnO4 -> K2MnO4+MnO2+O2
hòa tan hoàn toàn 7.65 gam hỗn hợp Al và Mg tỉ lệ mol là 1:1 vào dung dịch HNO3 loãng dư thu được hỗn hợp khí gồm 0.03 mol N2; 0.05 mol NO và dung dịch chứa m gam muối. Giá trị của m là ?
câu 1:thực hiện dãy biến hóa sau bằng phương trình minh họa kèm theo điều kiện của phản ứng nếu có____
FE2O3---> (1)FE---> (2)H2---> (3)H2O
các phản ứng trên thuộc loại phản ứng nào
câu 2:đốt cháy 13g kẽm(ZN) trong ko khí
a:lập PTPƯ.tính khối lượng kẽm oxit (ZNO) sinh ra
b:tính thể tích ko khí cần dùng?(biết lượng oxi chiếm 1 phần 5 thể tích ko khí)
c:nếu có được lượng khí oxi dùng trên cần phân hủy bao nhiêu gam thuốc tímKMnO4
d:nếu đem lượng khí oxi trên để đốt cháy trong 2,24 lít khí hidro(đktc).tính khối lượng chất thu được sau phản ứng
Bài 1 hoà tan 32g X(fe,mg,Zn,Al) bằng dd hcl dư thu được 2,24lít H2(được). Mặt khác cho 32g X vào h2so4 đặc nóng thu được 3,36l so2(được) tính %fe về khối lượng
Bài 2 hoà tan 30g hh một số kim loại vào dung dịch H2so4 đặc nóng(dự), tới khi hết pư thu đc 3,36l so2 (đktc) 3,2g S và 0,112 lít h2s. Xác định số mol h2so4 pư và m muối tạo thành sau pư
Bài 3 hoà tan 4,64g một oxit sắt trong dd H2So4 đặc nóng dư thu đc 0,224lít So2 xác định oxit
(Anh chị giải chi tiết chút e ms hok bảo toàn e)
Cho 2,88 gam Mg vào dd HNO3 sau phản ứng thu được Mg(NO3)2 và hỗn hợp Z khí NO và N2O tỉ lệ mol là 2:3. Tìm V hỗn hợp Z