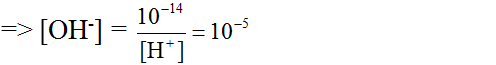Bài 5: Luyện tập về axit-bazo-muối; phản ứng trao đổi ion trong dung dịch chất điện li
Các câu hỏi tương tự
Một dung dịch có [H+] = 0,01 OM. Tính [OH-] và pH của dung dịch. Môi trường của dung dịch này là axit, trung tính hay kiềm ? Hãy cho biết màu của quỳ tím trong dung dịch này.
Hòa tan 41,6 gam BaCl2 vào nước được 500 ml dung dịch A. Tính nồng độ mol/lit của các ion trong dung dịch A?
Hòa tan 80 gam CuSO4 vào nước thu được 2 lit dung dịch A. Tính nồng độ mol/lit của các ion trong dung dịch A?
tim nồng độ mol cua các ion có trong dung dịch fe(no3)3. biết trong 1 lit dung dịch co hoa tan 60.5g Fe(no3)3 ( bo qua su thuỷ phân của ion fe3+
Trộn 300ml dung dịch Ba(OH)2 0,05M với 200ml dung dịch H2SO4 0,1M thu được m gam kết tủa
a) Tính m
b) Tính nồng độ mol của các ion sau phản ứng
c) Dung dịch A có pH bằng bao nhiêu?
Dung dịch axit mạnh một nấc X nồng độ 0,010 mol/l có pH = 2 và dung dịch bazơ mạnh một nấc Y nồng độ 0,010 mol/l có pH = 12. Vậy:
A. X và Y là các chất điện li mạnh.
B. X và Y là các chất điện li yếu.
C. X là chất điện li mạnh, Y là chất điện li yếu.
D. X là chất điện li yếu, Y là chất điện li mạnh.
Giải thích cụ thể ạ !!!
Cho 300 ml dung dịch NH3 1M vào 200 ml dung dịch HCI 1M. Tinh CM của các ion NH4+, Cl- và muối NH4Cl trong dung dịch thu được
CÂU 3.1: Tính khối lượng KOH có 500 ml dung dịch KOH có pH 12,3.CÂU 3.2: Tính khối lượng HNO3 (đktc) có trong 200 ml dung dịch có pH 2CÂU 4: Trộn 100 ml dung dịch Ba(OH)2 0,05M vào 400 ml dung dịch HNO3 0,02M thu được dung dịch X. Tính giá trị pH của dung dịch X.CÂU 5: Trộn 300ml dung dịch hỗn hợp X gồm H2SO4 0,1M và HCl 0,05M với 200ml dung dịch KOH 0,4M. Tính giá trị pH của dung dịch thu được?CÂU 6: Trộn V lít dung dịch HCl 0,05 M với 2 lít dung dịch Ba(OH)2 0,01M thu được dung dịch X có pH...
Đọc tiếp
CÂU 3.1: Tính khối lượng KOH có 500 ml dung dịch KOH có pH = 12,3.
CÂU 3.2: Tính khối lượng HNO3 (đktc) có trong 200 ml dung dịch có pH = 2
CÂU 4: Trộn 100 ml dung dịch Ba(OH)2 0,05M vào 400 ml dung dịch HNO3 0,02M thu được dung dịch X. Tính giá trị pH của dung dịch X.
CÂU 5: Trộn 300ml dung dịch hỗn hợp X gồm H2SO4 0,1M và HCl 0,05M với 200ml dung dịch KOH 0,4M. Tính giá trị pH của dung dịch thu được?
CÂU 6: Trộn V lít dung dịch HCl 0,05 M với 2 lít dung dịch Ba(OH)2 0,01M thu được dung dịch X có pH = 2. Tính giá trị của V?
Dung dịch X chứa các ion sau: Al3+, Cu2+, S O 4 2 - và N O 3 - . Để kết tủa hết ion có trong 500 ml dung dịch X cần 100 ml dung dịch BaCl2 1M. Cho 500 ml dung dịch X tác dụng với dung dịch NaOH dư thì được 19,6 gam kết tủa. Cô cạn 500 ml dung dịch X được 66,75 gam hỗn hợp muối khan. Nồng độ mol/l của N O 3 - là: