Câu 3. Hydrogen peroxide phân hủy theo phản ứng: 2H2O2 → 2H2O + O2.
Đo thể tích oxygen thu được theo thời gian, kết quả được ghi trong bảng sau:
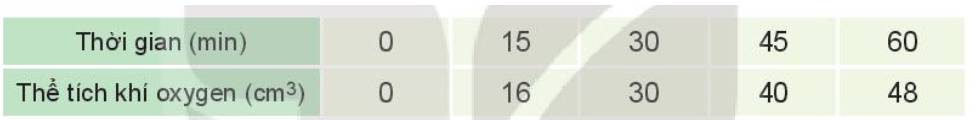
a) Vẽ đồ thị mô tả sự phụ thuộc của thể tích khí oxygen theo thời gian.
b) Tính tốc độ trung bình của phản ứng (theo cm3/min) trong khoảng thời gian:
- Từ 0 – 15 phút
- Từ 15 – 30 phút
- Từ 30 – 45 phút
- Từ 45 – 60 phút
Nhận xét sự thay đổi tốc độ trung bình theo thời gian.
a) Đồ thị em vẽ mãi không được a tham khảo tí nhé :v
Đồ thị mô tả sự phụ thuộc của thể tích khí oxygen theo thời gian: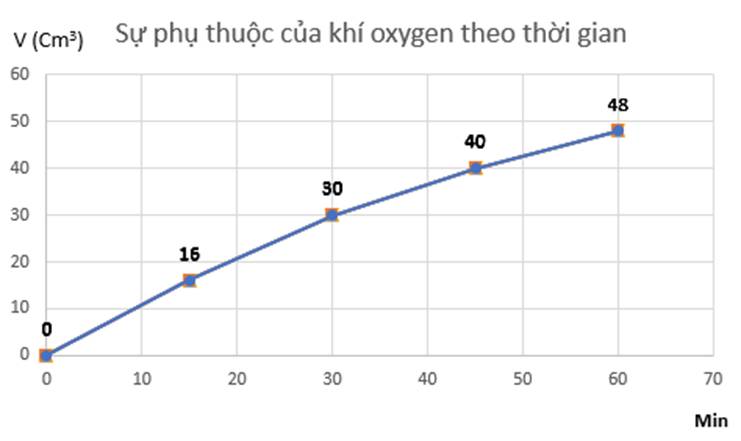 b)
b)
Ta có công thức tính vận tốc trung bình: \(V_{tb}=\dfrac{S_1+S_2....}{t_1+t_2....}\)
Tốc độ trung bình của phản ứng từ 0 - 15 phút là:
\(V_{tb_1}=\dfrac{16-0}{15-0}=1,0666....\approx1,067\) (cm3/min)
Tốc độ trung bình của phản ứng từ 15 - 30 phút là:
\(V_{tb_2}=\dfrac{30-16}{30-15}=0,9333....\approx0,933\) (cm3/min)
Tốc độ trung bình của phản ứng từ 30 - 45 phút là:
\(V_{tb_3}=\dfrac{40-30}{45-30}=0,66666.....\approx0,667\) (cm3/min)
Tốc độ trung bình của phản ứng từ 45 - 60 phút là:
\(V_{tb_4}=\dfrac{48-40}{60-45}=0,5333.....\approx0,533\) (cm3/min)
Ta thấy \(V_{tb_1}>V_{tb_2}>V_{tb_3}>V_{tb_4}\)
=> Tốc độ trung bình của phản ứng giảm dần theo thời gian.




