Từ gạo, ngô, khoai, sắn và vỏ bào mùn cưa điều chế được một chất lỏng có nhiều ứng dụng trong sản xuất, đời sống và pha vào xăng để làm nhiên liệu. Vậy chất lỏng đó có thành phần, cấu tạo và tính chất như thế nào?
Bài 23. Ethylic alcohol
Mở đầu (SGK Cánh Diều - Trang 114)
Thảo luận (1)
Câu hỏi 1 (SGK Cánh Diều - Trang 114)
Nêu sự khác nhau về cấu tạo của phân tử ethylic alcohol và phân tử ethane.
Thảo luận (1)Hướng dẫn giải(Trả lời bởi Nguyễn Quốc Đạt)
Ethylic alcohol
Ethane
Trong cấu tạo, có các liên kết giữa carbon với carbon và carbon với hydrogen, ngoài ra còn có nhóm –OH liên kết với một nguyên tử C.
Trong cấu tạo, chỉ có các liên kết giữa carbon với carbon và carbon với hydrogen.
Câu hỏi 2 (SGK Cánh Diều - Trang 114)
Dùng ống hút nhỏ giọt khoảng 2ml ethylic alcohol cho vào ống nghiệm. Quan sát và nêu trạng thái, màu sắc của ethylic alcohol.
Thảo luận (1)Hướng dẫn giảiEthylic alcohol là chất lỏng, không màu.
(Trả lời bởi Nguyễn Quốc Đạt)
Luyện tập 1 (SGK Cánh Diều - Trang 115)
Có hai ống nghiệm, ống 1 chứa 3 mml nước, ống 2 chứa 3 ml C2H5OH. Thêm 2 ml xăng vào mỗi ống nghiệm, lắc nhẹ sau đó để yên. Dự đoán các hiện tượng xảy ra trong hai ống nghiệm.
Thảo luận (1)Hướng dẫn giảiDự đoán hiện tượng:
- Ống nghiệm 1: Xăng không tan trong nước, hỗn hợp phân thành 2 lớp, xăng nổi lên trên.
- Ống nghiệm 2: Xăng tan trong C2H5OH, thu được dung dịch đồng nhất.
(Trả lời bởi Nguyễn Quốc Đạt)
Luyện tập 2 (SGK Cánh Diều - Trang 115)
Trong mỗi dung dịch sau đó có bao nhiêu ml ethylic alcohol?
a) 50 ml dung dịch ethylic alcohol 30oC.
b) 40 ml dung dịch ethylic alcohol 45oC.
Thảo luận (1)Hướng dẫn giảia)
Trong 100mL dung dịch ethylic alcolhol 30o có 30 ml ethylic alcohol nguyên chất.
Vậy 50 mL dung dịch ethylic alcolhol 30o có \(\dfrac{50.30}{100}\) = 15 ml ethylic alcohol nguyên chất.
b)
Trong 100mL dung dịch ethylic alcolhol 45o có 45 ml ethylic alcohol nguyên chất.
Vậy 40 mL dung dịch ethylic alcolhol 45o có \(\dfrac{40.45}{100}\) = 18 ml ethylic alcohol nguyên chất.
(Trả lời bởi Nguyễn Quốc Đạt)
Thí nghiệm 1 (SGK Cánh Diều - Trang 115)
Chuẩn bị• Dụng cụ: bát sứ, tấm bìa màu đen, ống nghiệm, kẹp ống nghiệm, giá để ống nghiệm.• Hoá chất: C2H5OH, nước vôi trong.Tiến hành thí nghiệm và thảo luận• Cho 1 mL C2H5OH vào bát sứ, đặt tấm bìa đen sau bát sứ, châm lửa, quan sát màu ngọn lửa.• Úp ống nghiệm phía trên ngọn lửa, khi lửa tắt xoay ống nghiệm lại, rót 3 - 4 mL nước vôi trong vào ống nghiệm, lắc đều.• Quan sát thí nghiệm, mô tả và giải thích các hiện tượng xảy ra.
Đọc tiếp
Chuẩn bị
• Dụng cụ: bát sứ, tấm bìa màu đen, ống nghiệm, kẹp ống nghiệm, giá để ống nghiệm.
• Hoá chất: C2H5OH, nước vôi trong.
Tiến hành thí nghiệm và thảo luận
• Cho 1 mL C2H5OH vào bát sứ, đặt tấm bìa đen sau bát sứ, châm lửa, quan sát màu ngọn lửa.
• Úp ống nghiệm phía trên ngọn lửa, khi lửa tắt xoay ống nghiệm lại, rót 3 - 4 mL nước vôi trong vào ống nghiệm, lắc đều.
• Quan sát thí nghiệm, mô tả và giải thích các hiện tượng xảy ra.
Thảo luận (1)Hướng dẫn giảiKhi châm lửa C2H5OH cháy với ngọn lửa màu xanh mờ, tỏa nhiều nhiệt. Khi úp ống nghiệm lên phía trên ngọn lửa, ta thu được sản phẩm cháy (CO2 + hơi nước), rót nước vôi trong vào ống nghiệm và lắc đều thấy dung dịch vẩn đục do CO2 phản ứng với Ca(OH)2 sinh ra CaCO3.
Phương trình hóa học:
C2H5OH + 3O2 \(\underrightarrow{t6o}\) 2CO2 + 3H2O
CO2 + Ca(OH)2 → CaCO3↓ + H2O
(Trả lời bởi Nguyễn Quốc Đạt)
Câu hỏi 3 (SGK Cánh Diều - Trang 115)
Hiện tượng nào trong thí nghiệm 1 chứng tỏ trong ethylic alcohol có carbon.
Thảo luận (1)Hướng dẫn giảiHiện tượng trong thí nghiệm 1 chứng tỏ ethylic alcohol có carbon là khi rót nước vôi trong vào ống thí nghiệm thấy xuất hiện vẩn đục.
CO2 + Ca(OH)2 → CaCO3↓ + H2O
(Trả lời bởi Nguyễn Quốc Đạt)
Vận dụng 1 (SGK Cánh Diều - Trang 115)
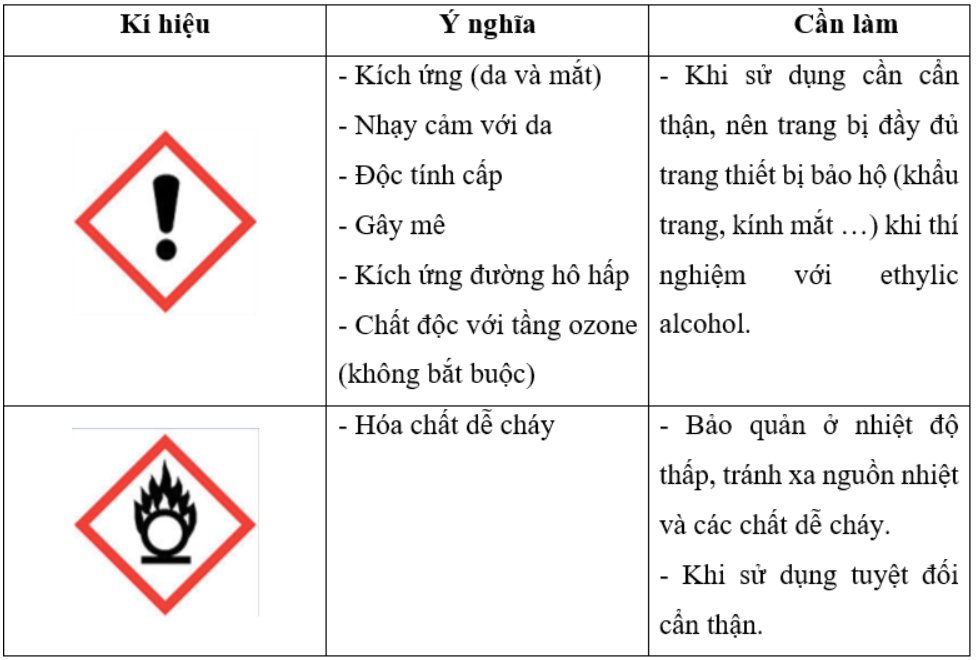
Trên chai đựng ethylic alcohol có các kí hiệu:

Nêu ý nghĩa của các kí hiệu trên. Cần phải làm gì khi sử dụng và lưu trữ ethylic alcohol?
Thảo luận (1)Hướng dẫn giải
Thí nghiệm 2 (SGK Cánh Diều - Trang 116)
Chuẩn bị• Dụng cụ: ống nghiệm, giá thí nghiệm, ống hút nhỏ giọt.• Hoá chất: C2H5OH, Na.Tiến hành thí nghiệm và thảo luận• Lắp ống nghiệm vào giá thí nghiệm, cho vào ống nghiệm khoảng 4 mL ethylic alcohol. Cắt lấy một mẩu nhỏ Na (cỡ hạt đậu xanh) cho vào ống nghiệm trên.• Quan sát thí nghiệm, mô tả và giải thích các hiện tượng xảy ra.
Đọc tiếp
Chuẩn bị
• Dụng cụ: ống nghiệm, giá thí nghiệm, ống hút nhỏ giọt.
• Hoá chất: C2H5OH, Na.
Tiến hành thí nghiệm và thảo luận
• Lắp ống nghiệm vào giá thí nghiệm, cho vào ống nghiệm khoảng 4 mL ethylic alcohol. Cắt lấy một mẩu nhỏ Na (cỡ hạt đậu xanh) cho vào ống nghiệm trên.
• Quan sát thí nghiệm, mô tả và giải thích các hiện tượng xảy ra.
Thảo luận (1)Hướng dẫn giảiHiện tượng: Mẩu Na tan dần và có sủi bọt khí.
Phương trình hóa học:
2C2H5OH + 2Na → 2C2H5ONa + H2
(Trả lời bởi Nguyễn Quốc Đạt)
Câu hỏi 4 (SGK Cánh Diều - Trang 116)
Những chất nào sau đây phản ứng được với Na?
(a) CH3 – OH
(b) CH3 – CH2 – CH3
(c) CH3 – CH2 – CH2 – OH
(d) H2O
Viết các phương trình hoá học minh hoạ.
Thảo luận (1)Hướng dẫn giảiCác chất phản ứng được với Na là (a), (c) và (d)
Phương trình hóa học:
2CH3 – OH + 2Na → 2CH3 – ONa + H2
2CH3 – CH2 – CH2 – OH + 2Na → 2CH3 – CH2 – CH2 – ONa + H2
2H2O + 2Na → 2NaOH + H2
(Trả lời bởi Nguyễn Quốc Đạt)