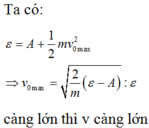Vì sao một số kim loại như magnesium, kẽm để lâu ngoài không khí sẽ mất đi ánh kim ban đầu?

Những câu hỏi liên quan
a) Giải thích tại sao sắt để ngoài không khí lâu ngày lại bỉ gỉ
b) nung 1 mẫu kim loại đồng trong không khí thì khối lượng thì mẫu kim loại tăng hay giảm ? vì sao
c) tại sao hỗn hợp hidro và oxi là 1 hỗn hợp nổ
giúp e với ạ , e cảm ơn
Khi H2 phản ứng với O2 sinh ra nước kèm theo nhiệt lượng lớn làm bề mặt nước giãn nở đột ngột , gây nổ mạnh
2H2+O2to→2H2O2H2+O2→to2H2O
Tiếng nổ lớn nhất khi tỉ lệ VH2:VO2=2:1VH2:VO2=2:1
Khi điều chế hidro, để thử tinh khiết hidro, người ta đốt khí thu được. Nếu khí cháy với ngọn lửa màu xanh và tiếng nổ nhẹ thì là hidro tinh khiết.
Đúng 2
Bình luận (0)
1. Chỉ khi có nước và khí oxi tác dụng đồng thời mới làm cho sắt bị gỉ.
Thành phần của gỉ sắt: oxit sắt, sắt hiđrôxít, sắt cacbonat, ...
2. Nếu làm vậy thì các dụng cụ đó nhanh chóng bị hư vì trong vôi, vữa đều có Ca(OH)2 là 1 chất kiềm có thể tác dụng với Al2O3 (vỏ bọc ngoài các đồ dùng bằng nhôm), sau đó nhôm bị ăn mòn.
Pthh: Al2O3 + Ca(OH)2 → Ca(AlO2)2 + H2O
Đúng 3
Bình luận (1)
a) Giải thích tại sao sắt để ngoài không khí lâu ngày lại bỉ gỉ
do bị oxi hóa
3Fe+2O2-to>Fe3O4
b) nung 1 mẫu kim loại đồng trong không khí thì khối lượng thì mẫu kim loại tăng hay giảm ? vì sao
tăng
2Cu+O2-to>2CuO
c) tại sao hỗn hợp hidro và oxi là 1 hỗn hợp nổ
đó là hỗn hợp có thể dãn nở mạnh nhất là tỉ lệ 1:2
2H2+O2-to>2H2O
Đúng 3
Bình luận (0)
Xem thêm câu trả lời
Khi cắt miếng Na kim loại để ở ngoài không khí, bề mặt vừa cắt có ánh kim lập tức mờ đi, đó là do Na đã bị oxi hóa bởi những chất nào trong không khí A. O2 B. H2O C. CO2 D. cả O2 và H2O
Đọc tiếp
Khi cắt miếng Na kim loại để ở ngoài không khí, bề mặt vừa cắt có ánh kim lập tức mờ đi, đó là do Na đã bị oxi hóa bởi những chất nào trong không khí
A. O2
B. H2O
C. CO2
D. cả O2 và H2O
Khi cắt miếng Na kim loại để ở ngoài không khí, bề mặt vừa cắt có ánh kim lập tức mờ đi, đó là do Na đã bị oxi hóa bởi những chất nào trong không khí? A. O2. B. H2O. C. CO2. D. O2 và H2O.
Đọc tiếp
Khi cắt miếng Na kim loại để ở ngoài không khí, bề mặt vừa cắt có ánh kim lập tức mờ đi, đó là do Na đã bị oxi hóa bởi những chất nào trong không khí?
A. O2.
B. H2O.
C. CO2.
D. O2 và H2O.
Khi cắt miếng Na kim loại để ở ngoài không khí, bề mặt vừa cắt có ánh kim lập tức mờ đi, đó là do Na đã bị oxi hóa bởi những những chất nào trong không khí A. O2 B. H2O C. CO2 D. Cả O2 và H2O
Đọc tiếp
Khi cắt miếng Na kim loại để ở ngoài không khí, bề mặt vừa cắt có ánh kim lập tức mờ đi, đó là do Na đã bị oxi hóa bởi những những chất nào trong không khí
A. O2
B. H2O
C. CO2
D. Cả O2 và H2O
Nếu bơm không khí vào một quả bóng bay thì dù có buộc chặt không khí vẫn thoát được ra ngoài, còn nếu bơm không khí vào một quả cầu bằng kim loại rồi hàn thì hầu như không khí không thể thoát ra ngoài. Tại sao?
Khoảng cách giữa các phân tử của vỏ bóng bay lớn hơn nên các phân tử không khí trong bóng bay có thể lọt ra ngoài. Khoảng cách giữa các nguyên tử kim loại rất nhỏ nên các phân tử không khí trong quả cầu hầu như không thể lọt ra ngoài.
Đúng 0
Bình luận (0)
Trong hiện tượng quang điện ngoài của một kim loại do một ánh sáng đơn sắc chiếu tới thì vận tốc ban đầu của electron quang điện bật ra khỏi kim loại có giá trị lớn nhất ứng với electron hấp thụ A. toàn bộ năng lượng của phôtôn B. nhiều phôtôn nhất C. được phôtôn có năng lượng lớn nhất D. phôtôn ở ngay bề mặt kim loại
Đọc tiếp
Trong hiện tượng quang điện ngoài của một kim loại do một ánh sáng đơn sắc chiếu tới thì vận tốc ban đầu của electron quang điện bật ra khỏi kim loại có giá trị lớn nhất ứng với electron hấp thụ
A. toàn bộ năng lượng của phôtôn
B. nhiều phôtôn nhất
C. được phôtôn có năng lượng lớn nhất
D. phôtôn ở ngay bề mặt kim loại
Một khối trụ kim loại được treo ở đầu 1 lực kế là X0. Ban đầu khối trụ để ngoài không khí thì chỉ số của lực kế là 8N. Sau đó, khối trụ được nhấn chìm trong nước thì chỉ số của lực kế là 6N. Cho biết TL riêng của nước là d0 10 000N/m3. a) Giải thích vì sao có sự chênh lệch trên. b) Thể tích của vật và trọng lượng riêng của vật là...
Đọc tiếp
Một khối trụ kim loại được treo ở đầu 1 lực kế là X0. Ban đầu khối trụ để ngoài không khí thì chỉ số của lực kế là 8N. Sau đó, khối trụ được nhấn chìm trong nước thì chỉ số của lực kế là 6N. Cho biết TL riêng của nước là d0 = 10 000N/m3. a) Giải thích vì sao có sự chênh lệch trên. b) Thể tích của vật và trọng lượng riêng của vật là bao nhiêu?
a) Vì khi nhúng vật vào nước có lực đẩy Ác-Si-Mét đẩy từ dưới lên(ngược chiều với trọng lực) nên số chỉ của lực kế giảm.
b) Gọi P' là số chỉ của lực kết khi nhúng vào nước, tá có:
Fa=P-P'=8-6=2N
Mà Fa=d.V(thể tích của vật đúng bằng thể tích của phần nước bị chiếm chỗ
⇒V=\(\dfrac{Fa}{d}\)=\(\dfrac{2}{10000}\)=0,0002m3=200cm3
Trọng lượng riêng của vật là:
dvật=\(\dfrac{P}{V}\)=\(\dfrac{8}{0,0002}\)=40000N/m3
Vậy V=200cm3; dvật=40000N/m3
Đúng 2
Bình luận (0)
Cho các nhận định sau: (a) Tính chất hoá học đặc trưng của kim loại là tính khử. (b) Đồng (Cu) không khử được muối sắt(III) (Fe3+). (c) Ăn mòn kim loại là một quá trình hoá học trong đó kim loại bị ăn mòn bởi các axit trong môi trường không khí. (d) Để bảo vệ vỏ tàu biển làm bằng thép, người ta gắn vào mặt ngoài vỏ tàu (phần chìm trong nước biển) những khối kẽm. Số nhận định đúng là A. 2. B. 3. C. 4. D. 1.
Đọc tiếp
Cho các nhận định sau:
(a) Tính chất hoá học đặc trưng của kim loại là tính khử.
(b) Đồng (Cu) không khử được muối sắt(III) (Fe3+).
(c) Ăn mòn kim loại là một quá trình hoá học trong đó kim loại bị ăn mòn bởi các axit trong môi trường không khí.
(d) Để bảo vệ vỏ tàu biển làm bằng thép, người ta gắn vào mặt ngoài vỏ tàu (phần chìm trong nước biển) những khối kẽm.
Số nhận định đúng là
A. 2.
B. 3.
C. 4.
D. 1.
Đáp án A
(a) Tính chất hoá học đặc trưng của kim loại là tính khử.
(d) Để bảo vệ vỏ tàu biển làm bằng thép, người ta gắn vào mặt ngoài vỏ tàu (phần chìm trong nước biển) những khối kẽm.
Đúng 0
Bình luận (0)
Lấy cùng một khối lượng kẽm và nhôm cho vào dd H2SO4 loãng, dư. Kim loại nào cho nhiều khí hiđro hơn? Vì sao?
Giả sử mZn = mAl = a (g)
\(n_{Zn}=\dfrac{a}{65}\left(mol\right)\); \(n_{Al}=\dfrac{a}{27}\left(mol\right)\)
PTHH: Zn + H2SO4 --> ZnSO4 + H2 (1)
=> \(n_{H_2\left(1\right)}=\dfrac{a}{65}\left(mol\right)\)
2Al + 3H2SO4 -->Al2(SO4)3 + 3H2
=> \(n_{H_2\left(2\right)}=\dfrac{a}{18}\left(mol\right)\)
Có \(n_{H_2\left(1\right)}< n_{H_2\left(2\right)}\)
=> Nhôm cho nhiều H2 hơn
Đúng 3
Bình luận (0)
Hòa tan M gam kim loại R ( có một hóa trị duy nhất ) vào dung dịch H2SO4 loãng dư sau phản ứng thấy khối lượng dung dịch tăng 1,2 gam so với dung dịch axit ban đầu nung lượng kim loại R nói trên ngoài không khí đến khối lượng không đổi thu được 2,55 gam chất rắn . Thấy có V lít không khí ( đktc ) tham gia phản ứng.
a ) Xác định kim loại R và tính m
b ) tính V ( biết oxi chiếm khoảng 20% thể tích không khí )
Đọc tiếp
Hòa tan M gam kim loại R ( có một hóa trị duy nhất ) vào dung dịch H2SO4 loãng dư sau phản ứng thấy khối lượng dung dịch tăng 1,2 gam so với dung dịch axit ban đầu nung lượng kim loại R nói trên ngoài không khí đến khối lượng không đổi thu được 2,55 gam chất rắn . Thấy có V lít không khí ( đktc ) tham gia phản ứng. a ) Xác định kim loại R và tính m b ) tính V ( biết oxi chiếm khoảng 20% thể tích không khí )
a)
Gọi số mol R là a (mol)
PTHH: 2R + nH2SO4 --> R2(SO4)n + nH2
a------------------------->0,5an
mtăng = mR - mH2 = a.MR - 2.0,5an = a.MR - an = 1,2 (1)
PTHH: 4R + nO2 --to--> 2R2On
a--------------->0,5a
=> \(0,5a\left(2.M_R+16n\right)=2,55\)
=> a.MR + 8an = 2,55 (2)
(1)(2) => a.MR = 1,35; an = 0,15
=> \(M_R=9n\left(g/mol\right)\)
Xét n = 3 thỏa mãn => MR = 27 (g/mol)
=> R là Al
a = 0,05 (mol)
m = 1,35 (g)
b)
PTHH: 4Al + 3O2 --to--> 2Al2O3
0,05->0,0375
=> VO2 = 0,0375.22,4 = 0,84 (l)
=> Vkk = 0,84 : 20% = 4,2 (l)
Đúng 2
Bình luận (2)