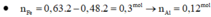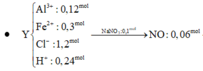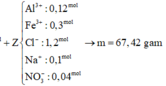Cho 2,4 gam Mg vào 109,5 gam dung dịch acid hydrochloric 10% đến khi phản ứng xảy ra hoàn toàn, thu được dung dịch A và có V lít khí thoát ra (dkc). a) Viết PTPƯ, tính V b) Dung dịch A chứa chất tan nào? Tính nồng độ C% của dung dịch A.

Những câu hỏi liên quan
cho 2,4 gam Mg vào 109,5 gam dung dịch axit clohiđric 10% đến khi phản ứng xảy ra hoàn toàn, thu được dung dịch A và có A lít khí thoát ra (đktc).
a) viết PTPƯ, tính V?
b) dung dịch A chứa chất tan nào? tính nồng độ C% của dung dịch A.
\(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\\ m_{HCl}=\dfrac{109,5\cdot10\%}{100\%}=10,95\left(g\right)\\ \Rightarrow n_{HCl}=\dfrac{10,95}{36,5}=0,3\left(mol\right)\\ a,PTHH:Mg+2HCl\rightarrow MgCl_2+H_2\\ \text{Vì }\dfrac{n_{Mg}}{1}< \dfrac{n_{HCl}}{2}\text{ nên sau p/ứ }HCl\text{ dư}\\ \Rightarrow n_{H_2}=0,1\left(mol\right)\\ \Rightarrow V_{H_2\left(đktc\right)}=0,1\cdot22,4=2,24\left(l\right)\)
\(b,n_{MgCl_2}=0,1\left(mol\right)\\ \Rightarrow m_{CT_{MgCl_2}}=0,1\cdot95=9,5\left(g\right)\\ m_{H_2}=0,1\cdot2=0,2\left(mol\right)\\ m_{dd_{MgCl_2}}=2,4+109,5-0,2=111,7\left(g\right)\\ \Rightarrow C\%_{MgCl_2}=\dfrac{9,5}{111,7}\cdot100\%\approx8,5\%\)
Đúng 3
Bình luận (1)
Hòa tan hoàn toàn 4,8g Magnesium Mg vào dd Hydrochloric acid HCl10%, sau phản ứng thu được dung dịch A và khí B.
a. Viết PTPƯ xảy ra?
b. Tính thể tích khí B thoát ra ở 25oC 1 bar?
c. Tính khối lượng dd Hydrochloric acid10% đã dùng?
d. Tính nồng độ phần trăm của dd A tạo thành sau phản ứng?
\(a,n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ b,n_{MgCl_2}=n_{H_2}=n_{Mg}=0,2\left(mol\right)\\ b,V_{H_2\left(25\text{đ}\text{ộ}C,1bar\right)}=0,2.24,79=4,958\left(l\right)\\ c,n_{HCl}=2.0,2=0,4\left(mol\right)\\ m_{\text{dd}HCl}=\dfrac{0,4.36,5.100}{10}=146\left(g\right)\\ m_{\text{dd}A}=m_{Mg}+m_{\text{dd}HCl}-m_{H_2}=4,8+146-0,2.2=150,4\left(g\right)\\ d,C\%_{\text{dd}MgCl_2}=\dfrac{95.0,2}{150,4}.100\approx12,633\%\)
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn 5,85 g kim loại Kali vào 100 gam H2O. Sau khi phản ứng xảy ra xong thu được dung dịch A và V lít khí thoát ra (đktc). Viết phương trình phản ứng xảy ra, tìm giá trị V và tính nồng độ phần trăm của dung dịch A
\(n_K=\dfrac{5,85}{39}=0,15\left(mol\right)\)
PTHH: 2K + 2H2O --> 2KOH + H2
_____0,15------------->0,15-->0,075
=> VH2 = 0,075.22,4 =1,68(l)
mdd = 5,85 + 100 - 0,075.2 = 105,7(g)
=> \(C\%=\dfrac{0,15.56}{105,7}.100\%=7,95\%\)
Đúng 2
Bình luận (0)
Cho 8,4 gam bột sắt vào 270 gam dung dịch CuCl2 10% (d = 1,35 g/ml), khi đến phản ứng xảy ra hoàn toàn thu được a gam chất rắn và dung dịch A.
a) Viết PTPƯ, tính a?
b) Tính C% của dung dịch A.
c) Xác định nồng độ mol/lít của dd A (coi thể tích dung dịch thay đổi không đáng kể)
\(n_{Fe}=\dfrac{8,4}{56}=0,15mol\)
\(m_{CuCl_2}=\dfrac{270\cdot10\%}{100\%}=27g\Rightarrow n_{CuCl_2}=0,2mol\)
\(Fe+CuCl_2\rightarrow FeCl_2+Cu\)
0,15 0,2 0,15 0,15
\(a=m_{Cu}=0,15\cdot64=9,6g\)
\(m_{FeCl_2}=0,15\cdot127=19,05g\)
\(m_{ddFeCl_2}=8,4+270-0,15\cdot64=268,8g\)
\(C\%=\dfrac{19,05}{268,8}\cdot100\%=7,09\%\)
Đúng 3
Bình luận (0)
Cho m gam hỗn X gồm Fe và Al tan hoàn toàn trong 1,2 lít dung dịch HCl 1M (dư), thu được dung dịch Y và thoát ra 10,752 lít H2 (đktc). Mặt khác cho m gam hỗn hợp X vào dung dịch H2SO4 đặc nóng, dư, khi phản ứng xảy ra hoàn toàn, thu được 14,112 lít SO2 (đktc, sản phẩm khử duy nhất của S+6). Thêm 0,1 mol NaNO3 vào dung dịch Y, khi phản ứng xảy ra hoàn toàn thu được dung dịch Z và thoát ra V lít khí NO (đktc, sản phẩm khử duy nhất của N+5). Khối lượng muối có trong Z là? A. 82,34 gam. B. 54,38 g...
Đọc tiếp
Cho m gam hỗn X gồm Fe và Al tan hoàn toàn trong 1,2 lít dung dịch HCl 1M (dư), thu được dung dịch Y và thoát ra 10,752 lít H2 (đktc). Mặt khác cho m gam hỗn hợp X vào dung dịch H2SO4 đặc nóng, dư, khi phản ứng xảy ra hoàn toàn, thu được 14,112 lít SO2 (đktc, sản phẩm khử duy nhất của S+6). Thêm 0,1 mol NaNO3 vào dung dịch Y, khi phản ứng xảy ra hoàn toàn thu được dung dịch Z và thoát ra V lít khí NO (đktc, sản phẩm khử duy nhất của N+5). Khối lượng muối có trong Z là?
A. 82,34 gam.
B. 54,38 gam.
C. 67,42 gam.
D. 72,93 gam.
Cho 8,1 gam kim loại M tác dụng với 4,8 gam khí oxi, để phản ứng xảy ra hoàn toàn thu được chất rắn A. Cho A vào dung dịch HCl (dùng dư 10%) thu được dung dịch B và 3,36 lít khí thoát ra (đktc).
a) Xác định kim loại M.
b) Cho V ml dung dịch NaOH 2M vào dung dịch B, phản ứng kết thúc thu được 15,6 gam kết tủa. Tính V.
Đặt hóa trị của M là x(x>0)
\(n_{O_2}=\dfrac{4,8}{32}=0,15(mol)\\ n_{H_2}=\dfrac{3,36}{22,4}=0,15(mol)\\ a,PTHH:4M+xO_2\xrightarrow{t^o}2M_2O_x\\ 2M+2xHCl\to 2MCl_x+xH_2\\ \Rightarrow \Sigma n_{M}=\dfrac{0,6}{x}+\dfrac{0,3}{x}=\dfrac{0,9}{x}\\ \Rightarrow M_{M}=\dfrac{8,1}{\dfrac{0,9}{x}}=9x(g/mol)\\ \text {Thay }x=3 \Rightarrow M_{M}=27(g/mol)\\ \text {Vậy M là nhôm (Al)}\)
\(b,\text {Dung dịch B là }AlCl_3\\ n_{Al}=\dfrac{8,1}{27}=0,3(mol)\\ \Rightarrow n_{AlCl_3}=n_{Al}=0,3(mol)\\ n_{Al(OH)_3}=\dfrac{15,6}{78}=0,2(mol)\\ PTHH:3NaOH+AlCl_3\to Al(OH)_3\downarrow +3NaCl\\ \text {Vì }\dfrac{n_{AlCl_3}}{1}>\dfrac{n_{Al(OH)_3}}{1} \text {nên } AlCl_3 \text { dư}\\ \Rightarrow n_{NaOH}=3n_{Al(OH)_3}=0,6(mol)\\ \Rightarrow V_{dd_{NaOH}}=0,6.2=1,2(l)\)
Đúng 0
Bình luận (2)
Hoà tan hoàn toàn 5,28 gam magnesium Mg vào 200 gam dung dịch hydrochloric acid HCl a) Viết PTHH và tính thể tích khí thoát ra (đkc) b) Tính nồng độ phần trăm dung dịch HCl đã dùng c) Tính nồng độ phần trăm của chất có trong dung dịch sau phản ứng
\(a)Mg+2HCl\rightarrow MgCl_2+H_2\\ n_{Mg}=\dfrac{5,28}{24}=0,22mol\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ 0,22...0,44........0,22........0,22\\ V_{H_2\left(đkc\right)}=0,22.24,79=5,4538l\\ b)C_{\%HCl}=\dfrac{0,44.26,5}{200}\cdot100=8,03\%\\ c)C_{\%MgCl_2}=\dfrac{0,22.95}{200+5,28}\cdot100\approx10,18\%\)
Đúng 1
Bình luận (0)
: Cho 19,5g Zinc tác dụng hết với dung dịch có chứa a gam hydrochloric acid HCl, thấy thoát ra V lít khí X và dung dịch Y. Cô cạn dung dịch Y thu được b gam muối.
a. Tính V ở đkc
b. Tìm a , b
a) \(n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,3--->0,6------>0,3-->0,3
=> V = 0,3.24,79 = 7,437 (l)
b) a = mHCl = 0,6.36,5 = 21,9 (g)
b = mZnCl2 = 0,3.136 = 40,8 (g)
Đúng 1
Bình luận (0)
Cho 26 gam Zn vào dung dịch HCl dư sau khi phản ứng xảy ra hoàn toàn thu được V lít H2 (đktc)a, Tính V và khối lượng ZnCl2 thu được?b, Dẫn V lít khí H2 trên qua ống nghiệm đựng 46,4 gam nung nóng đến khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Tính m và % theo khối lượng mỗi chất trong m?c, Nếu dẫn khí H2 trên qua ống nghiệm đựng 46,4 gam chất rắn sau khi kết thúc phản ứng thu được 41,28 gam chất rắn. Tính hiệu suất phản ứng?
Đọc tiếp
Cho 26 gam Zn vào dung dịch HCl dư sau khi phản ứng xảy ra hoàn toàn thu được V lít H2 (đktc)
a, Tính V và khối lượng ZnCl2 thu được?
b, Dẫn V lít khí H2 trên qua ống nghiệm đựng 46,4 gam nung nóng đến khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Tính m và % theo khối lượng mỗi chất trong m?
c, Nếu dẫn khí H2 trên qua ống nghiệm đựng 46,4 gam chất rắn sau khi kết thúc phản ứng thu được 41,28 gam chất rắn. Tính hiệu suất phản ứng?