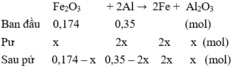0,81 gam kim loại nhôm trong 270ml dung dịch H2SO4 0,2M (loãng). Hỏi sau phản ứng Al hay H2SO4 dư? Dư bao nhiêu gam?

Những câu hỏi liên quan
Hòa tan 0,81g nhôm trong 270ml dung dịch H2SO4 0,2M ( loãng ). Hỏi sau phản ứng Al hay H2SO4 còn dư ? Dư bao nhiêu gam ?
+ n Al = 0,81 /27 = 0,03 (mol)
+ n H2SO4 = 0,2 . (270 / 1000) = 0,054 (mol)
2Al + 3H2SO4 --------> Al2(SO4)3 + 3H2
0,03---->0,045 (mol)
Vì nAl / 2 = 0,015 < n H2SO4 / 3 = 0,018
=> H2SO4 dư sau phản ứng
mH2SO4 dư = (0,054 - 0,045) . 98 = 0,882 (g)
cho 5,4 gam Al phản ứng với 132,2 gam dung dịch H2SO4 20% . a)Kim loại hay axit còn dư sau phản ứng ? Dư bao nhiêu gam ? b)Tính thể tích khí hiđro?
nAl=5,4/27=0,2(mol)
mH2SO4=132,2.20%=26,44(g)
=>nH2SO4=26,44/98~0,27(mol)
pt:2Al+3H2SO4--->Al2(SO4)3+3H2
2_______3
0,2_____0,27
Ta có: 0,2/1>0,27/3
=>Al dư
mAl dư=0,02.27=0,54(g)
Theo pt: nH2=nH2SO4=0,27(mol)
=>VH2=0,27.22,4=6,048(l)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn m gam oxit FexOy bằng H2SO4 đặc, nóng được 4,48 lít SO2 (đkc), phần dung dịch chứa 240 gam một loại muối Fe duy nhất. Trộn 5,4 gam bột Al với 17,4 gam FexOy trên rồi tiến hành phản ứng nhiệt nhôm. Hòa tan hoàn toàn hỗn hợp rắn sau phản ứng bằng dung dịch H2SO4 loãng dư được 5,376 lít H2 (đkc). Tính hiệu suất phản ứng nhiệt nhôm. A. 80% B. 73,33% C. 26,67% D. 20%
Đọc tiếp
Hòa tan hoàn toàn m gam oxit FexOy bằng H2SO4 đặc, nóng được 4,48 lít SO2 (đkc), phần dung dịch chứa 240 gam một loại muối Fe duy nhất. Trộn 5,4 gam bột Al với 17,4 gam FexOy trên rồi tiến hành phản ứng nhiệt nhôm. Hòa tan hoàn toàn hỗn hợp rắn sau phản ứng bằng dung dịch H2SO4 loãng dư được 5,376 lít H2 (đkc). Tính hiệu suất phản ứng nhiệt nhôm.
A. 80%
B. 73,33%
C. 26,67%
D. 20%
Trộn 27,84 gam
Fe
2
O
3
với 9,45 gam bột Al rồi thực hiện phản ứng nhiệt nhôm (giả sử chỉ có phản ứng khử oxit sắt thành Fe kim loại), sau một thời gian thu được hỗn hợp B. Cho hỗn hợp B tác dụng vớí dung dịch
H
2
SO
4
loãng dư thu được 9,744 lít khí
H
2
(đktc). Hiệu suất phản ứng nhiệt nhôm là ...
Đọc tiếp
Trộn 27,84 gam Fe 2 O 3 với 9,45 gam bột Al rồi thực hiện phản ứng nhiệt nhôm (giả sử chỉ có phản ứng khử oxit sắt thành Fe kim loại), sau một thời gian thu được hỗn hợp B. Cho hỗn hợp B tác dụng vớí dung dịch H 2 SO 4 loãng dư thu được 9,744 lít khí H 2 (đktc). Hiệu suất phản ứng nhiệt nhôm là
A. 51,43%,
B. 51,72%.
C. 75,00%.
D. 68,50%.
Hòa tan hoàn toàn a gam hỗn hợp 2 kim loại Al, Cu trong dung dịch H2SO4 loãng, dư. Sau phản ứng thu được 3,36 lít khí H2 (đktc) và 8 gam chất rắn không tan.
a) Tính a.
b)Tính khối lượng dung dịch H2SO4 20% tối thiểu cần dùng cho phản ứng trên
a) PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑
2 mol : 3 mol : 1 mol : 3 mol
0,1 mol <-- 0,15 mol <--- 0,15 mol
số mol của H2 là: 3,36 / 22,4 = 0,15 mol
khối lượng Al là: 0,1 * 27 = 2,7 g
ta có: 8 g chất rắn không tan sau phản ứng là: Cu
vậy khối lượng hỗn hợp a là: mAl + mCu = 2,7 + 8 = 10,7 g
b) khối lượng chất tan của H2SO4 là: mchất tan= 0,15 * 98 = 14,7 g
ta có: C% H2SO4= (mchất tan/ m dung dịch) * 100
→ m dung dịch H2SO4 = ( m chất tan * 100) / C% = ( 14,7 * 100) / 20= 73,5 g
Đúng 0
Bình luận (0)
Bài 1: Hòa tan 4,5 gam hợp kim nhôm, magie trong dung dịch H2SO4 loãng, dư, thấy có 5,04 lít khí hiđro bay ra (đktc).A) Viết phương trình hoá học. B) Tính thành phần phần trăm khối lượng của các kim loại trong hợp kim.Bài 2: Cho 5,4 gam Al vào 100 ml dung dịch H2SO4 0.5M.A) Tính thể tích khí H2 sinh ra (đktc).B) Tính nồng độ mol của các chất trong dung dịch sau phản ứng. Cho rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể.
Đọc tiếp
Bài 1: Hòa tan 4,5 gam hợp kim nhôm, magie trong dung dịch H2SO4 loãng, dư, thấy có 5,04 lít khí hiđro bay ra (đktc).
A) Viết phương trình hoá học.
B) Tính thành phần phần trăm khối lượng của các kim loại trong hợp kim.
Bài 2: Cho 5,4 gam Al vào 100 ml dung dịch H2SO4 0.5M.
A) Tính thể tích khí H2 sinh ra (đktc).
B) Tính nồng độ mol của các chất trong dung dịch sau phản ứng. Cho rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể.
1.nH2=5.04/22.4=0.225mol
Đặt x,y lần lượt là số mol của Al,Mg
a)2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
x 3/2 x
Mg+ H2SO4 --> MgSO4 + H2
y y
b) theo đề, ta có hệ pt: 27x + 24y= 4.5
1.5x + y =0.225
giải hệ pt trên,ta có :x=0.1 ; y=0.075
thay vào pt,suy ra :
mAl=0.1*27=2.7g =>%Al=(2.7/4.5)*100=60%
=>%Mg=40%
vậy % của Al,Mg lần lượt là 60% và 40%
2.nAl=5.4/27=0.2mol
nH2SO4=0.5*0.1=0.05 mol
pt:2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
0.2 0.05 0.02 0.05
a)theo pt, ta thấy Al dư
VH2=0.05*22.4=1.12 l
b)CMAl2(SO4)3= 0.02/0.1=0.2M
Bài này không khó đâu nh,tính theo pthh thôi à.
Chúc em học tốt!!!:))
Đúng 1
Bình luận (3)
Cho 25 (gam) hỗn hợp gồm Nhôm và Đồng vào dung dịch H2SO4 loãng dư, sau phản ứng thấy thoát ra 5,6 (lít) khí H2 (ở đktc). Tính khối lượng mỗi kim loại có trong hỗn hợp ban đầu.
nH2 = 5.6/22.4 = 0.25 (mol)
2Al + 3H2SO4 => Al2(SO4)3 + 3H2
1/6............................................0.25
mAl = 1/6 * 27 = 4.5 (g)
mCu = 25 - 4.5 = 20.5 (g)
Đúng 1
Bình luận (0)
Hòa tan 10 gam hỗn hợp 3 kim loại Mg, Al, Zn trong 300 gam dung dịch H2SO4 loãng (lấy dư), sau khi phản ứng kết thúc thu được dung dịch X có khối lượng tăng so với dung dịch ban đầu a gam và 4,48 lít khí H2 (đktc). Tính giá trị của a.
Ta có: \(m_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\) \(\Rightarrow m_{H_2}=0,2\cdot2=0,4\left(g\right)\)
\(\Rightarrow m_{dd\left(sau.pư\right)}=m_{hh}+m_{ddH_2SO_4}-m_{H_2}=309,6\left(g\right)\)
\(\Rightarrow a=309,6-300=9,6\left(g\right)\)
Đúng 4
Bình luận (2)
đề ko cho nồng độ phần trăm của dd H2SO4 à
Đúng 0
Bình luận (1)
Trộn 10,8 gam bột Al với 34,8 gam bột
F
e
3
O
4
rồi tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí. Hoà tan hoàn toàn hỗn hợp rắn sau phản ứng bằng dung dịch
H
2
S
O
4
loãng (dư), thu được 10,752 lít khí
H
2
(đktc). Tính hiệu suất của phản ứng nhiệt nhôm.
Đọc tiếp
Trộn 10,8 gam bột Al với 34,8 gam bột F e 3 O 4 rồi tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí. Hoà tan hoàn toàn hỗn hợp rắn sau phản ứng bằng dung dịch H 2 S O 4 loãng (dư), thu được 10,752 lít khí H 2 (đktc). Tính hiệu suất của phản ứng nhiệt nhôm.