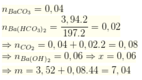Cho 28,4g hỗn hợp CaCO3 và MgCO3 tác dụng với acid HCl dư. Khí sinh ra cho hấp thu hoàn toàn với 50 ml dung dịch Ba(OH)2, tạo ra 5,91g chất kết tủa. Tìm tỉ lệ % của CaCO3 và MgCO3 trong hỗn hợp.
Các bạn giúp mình với. Minh tick cho nhé!

Những câu hỏi liên quan
Cho 18,4 gam hỗn hợp A gồm MgCO3 và CaCO3 tác dụng với dd HCl dư. Toàn bộ khí CO2 sinh ra cho qua 150 ml dd Ba(OH)2 1M thu được 19,7 gam kết tủa. Tính % khối lượng muối trong A.
\(n_{BaCO_3}=\dfrac{19.7}{197}=0.1\left(mol\right)\)
\(n_{Ba\left(OH\right)_2}=0.15\cdot1=0.15\left(mol\right)\)
\(n_{MgCO_3}=a\left(mol\right),n_{CaCO_3}=b\left(mol\right)\)
\(\Rightarrow m_A=84a+100b=18.4\left(g\right)\left(1\right)\)
\(MgCO_3+2HCl\rightarrow MgCl_2+CO_2+H_2O\)
\(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\)
\(n_{CO_2}=a+b\left(mol\right)\)
TH1 : Không tạo muối axit , Ba(OH)2 dư
\(\Rightarrow n_{CO_2}=n_{BaCO_3}=0.1\left(mol\right)\)
\(\Rightarrow a+b=0.1\left(2\right)\)
\(\left(1\right),\left(2\right):a=-0.525,b=0.625\left(L\right)\)
TH2 : Phản ứng tạo hai muối vừa đủ
\(n_{CO_2}=0.1+\left(0.15-0.1\right)\cdot2=0.2\left(mol\right)\)
\(\Rightarrow a+b=0.1\left(3\right)\)
\(\left(1\right),\left(3\right):a=b=0.1\)
\(\%MgCO_3=\dfrac{8.4}{18.4}\cdot100\%=45.65\%\)
\(\%CaCO_3=54.35\%\)
Đúng 2
Bình luận (0)
Cho 5,86g hỗn hợp CaCO3 và MgCO3 hòa tan với dd HCl dư. Khí CO2 thu được cho hấp thụ hoàn toàn bởi 50ml dd Ba(OH)2 0,9M tạo ra 5,91g kết tủa. Tính khối lượng mỗi muối trong hỗn hợp
Câu 15; Một hỗn hợp gồm 2 muối CaCO3 và MgCO3. Lấy 1,42g hỗn hợp trên tác dụng với dung dịch HCl dư thì thu được một chất khí. Dẫn khí này đi vào dung dịch có chứa 0,0225 mol Ba(OH)2 thì thu được một chất kết tủa. Lọc bỏ kết tủa sau đó cho vào dung dịch thu được một dung dịch H2SO4 dư thì thu được 1,7475g một kết tủa mới.a: Viết các pt phản ứng xảy ra b: Tính khối lượng mỗi muối trong hỗn hợp đầu
Đọc tiếp
Câu 15; Một hỗn hợp gồm 2 muối CaCO3 và MgCO3. Lấy 1,42g hỗn hợp trên tác dụng với dung dịch HCl dư thì thu được một chất khí. Dẫn khí này đi vào dung dịch có chứa 0,0225 mol Ba(OH)2 thì thu được một chất kết tủa. Lọc bỏ kết tủa sau đó cho vào dung dịch thu được một dung dịch H2SO4 dư thì thu được 1,7475g một kết tủa mới.
a: Viết các pt phản ứng xảy ra
b: Tính khối lượng mỗi muối trong hỗn hợp đầu
\(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\uparrow\)
\(x\) \(x\)
\(MgCO_2+2HCl\rightarrow MgCl_2+H_2O+CO_2\uparrow\)
\(y\) \(y\)
Thu đc kết tủa \(BaSO_4\)
\(n_{BaSO_4}=\dfrac{1,7475}{233}=0,0075mol=n_{Ba\left(OH\right)_2dư}\)
\(\Rightarrow n_{Ba\left(OH\right)_2PƯ}=0,0225-0,0075=0,015mol=n_{BaCO_3}\)(BT Ba)
\(\Rightarrow n_{CO_2}=n_{BaCO_3}=0,015mol\left(BtC\right)\)
Ta có:
\(\left\{{}\begin{matrix}100x+84y=1,42\\x+y=n_{CO_2}=0,015\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,01\\y=0,005\end{matrix}\right.\)
\(m_{CaCO_3}=0,01\cdot100=1g\)
\(m_{MgCO_3}=0,005\cdot84=0,42g\)
Đúng 3
Bình luận (0)
Nhiệt phân hoàn toàn hỗn hợp MgCO3, CaCO3 rồi cho toàn bộ khí thoát ra (khí X) hấp thụ vừa hết bằng dung dịch Ca(OH)2, thu được kết tủa Y và dung dịch Z. Các chất X, Y, Z lần lượt là: A. CO, CaCO3, Ca(HCO3)2. B. CO, Ca(HCO3)2, CaCO3. C. CO2, CaCO3, Ca(HCO3)2. D. CO2 ,Ca(HCO3)2, CaCO3.
Đọc tiếp
Nhiệt phân hoàn toàn hỗn hợp MgCO3, CaCO3 rồi cho toàn bộ khí thoát ra (khí X) hấp thụ vừa hết bằng dung dịch Ca(OH)2, thu được kết tủa Y và dung dịch Z. Các chất X, Y, Z lần lượt là:
A. CO, CaCO3, Ca(HCO3)2.
B. CO, Ca(HCO3)2, CaCO3.
C. CO2, CaCO3, Ca(HCO3)2.
D. CO2 ,Ca(HCO3)2, CaCO3.
Nhiệt phân hoàn toàn hỗn hợp MgCO3; CaCO3 rồi cho toàn bộ khí X vào dung dịch thu được ↓ Y và dung dịch Z![]()
![]() Khí X là CO2
Khí X là CO2
CO2 + Ca(OH)2 → CaCO3↓ + H2O
CaCO3↓ + CO2 + H2O → Ca(HCO3)2
→ Kết tủa Y là CaCO3; dung dịch Z là Ca(HCO3)2 → Đáp án đúng là đáp án C
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 20 gam hỗn hợp A gồm MgCO3 và RCO3 (với tỉ lệ mol 1 : 1) bằng dung dịch HCl dư. Lượng CO2 sinh ra cho hấp thụ hoàn toàn bởi 500ml dung dịch Ba(OH)2 0,5M thu được 39,4 gam kết tủa. Kim loại R là A. Ba B. Ca C. Fe D. Cu
Đọc tiếp
Hòa tan hoàn toàn 20 gam hỗn hợp A gồm MgCO3 và RCO3 (với tỉ lệ mol 1 : 1) bằng dung dịch HCl dư. Lượng CO2 sinh ra cho hấp thụ hoàn toàn bởi 500ml dung dịch Ba(OH)2 0,5M thu được 39,4 gam kết tủa. Kim loại R là
A. Ba
B. Ca
C. Fe
D. Cu
Bài 3*: Cho m gam hỗn hợp gồm CaCO3 và CaSO3 tác dụng với dung dịch HCl loãng dư thấy thoát ra 4,48 lít hỗn hợp hai khí ở đktc. Cho toàn bộ lượng hỗn hợp khí trên hấp thụ hết vào dung dịch Ba(OH)2 dư thấy tạo ra (m + a) gam kết tủa. Hãy tính a
giúp em với ạ
\(CaCO_3 + 2HCl \rightarrow CaCl_2 + CO_2 + H_2O\) (1)
\(CaSO_3 + 2HCl \rightarrow CaCl_2 + SO_2 + H_2O\) (2)
\(Ba(OH)_2 + CO_2 \rightarrow BaCO_3 + H_2O\) (3)
\(Ba(OH)_2 + SO_2 \rightarrow BaSO_3 + H_2O\) (4)
2 PTHH (3) và (4) tạo muối trung hòa và nước do Ba(OH)2 dư
\(n_{H_2}= \dfrac{4,48}{22,4}= 0,1 mol\)
Theo PTHH:
\(n_{khí}= n_{H_2}= 0,2 mol\)
Bảo toàn nguyên tố C và S
Ta có nC và nS trong 2 muối canxi ban đầu bằng nC và nS trong 2 muối Ba sau
Nên n\(CO_3\) và n\(SO_3\) trong muối canxi ban đầu và n\(CO_3\) và n\(SO_3\) trong muối Ba sau bằng nhau
Vậy a là khối lượng tăng lên từ Ca lên Ba
Tăng giảm khối lượng:
Từ Ca lên Ba tăng 137 - 40= 97 g tạo 1 mol khí
=> Từ Ca lên Ba tăng 0,2 . 97= 19,4 g tạo 0,2 mol khí
Vậy a= 19,4 g
Đúng 1
Bình luận (0)
Nung m gam hỗn hợp X gồm 2 muối MgCO3 và CaCO3 cho đến khi không còn khí thoát ra, thu được 3,52 gam chất rắn Y và khí Z. Cho toàn bộ khí Z hấp thụ hết bởi 1 lít dung dịch Ba(OH)2 x mol/l, thu được 7,88 gam kết tủa. Đun nóng tiếp dung dịch thấy tạo ra 3,94 gam kết tủa nữa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m và x lần lượt là A. 3,52 gam và 0,03 mol/l. B. 7,04 gam và 0,06 mol/l. C. 7,04 gam và 0,03 mol/l. D. 3,52 gam và 0,06 mol/l.
Đọc tiếp
Nung m gam hỗn hợp X gồm 2 muối MgCO3 và CaCO3 cho đến khi không còn khí thoát ra, thu được 3,52 gam chất rắn Y và khí Z. Cho toàn bộ khí Z hấp thụ hết bởi 1 lít dung dịch Ba(OH)2 x mol/l, thu được 7,88 gam kết tủa. Đun nóng tiếp dung dịch thấy tạo ra 3,94 gam kết tủa nữa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m và x lần lượt là
A. 3,52 gam và 0,03 mol/l.
B. 7,04 gam và 0,06 mol/l.
C. 7,04 gam và 0,03 mol/l.
D. 3,52 gam và 0,06 mol/l.
Nung 10g hỗn hợp MgCO3, CaCO3, và Al2O3 trong đó Al2O3 chiếm 10% về khối lượng đến khi các phản ứng xảy ra hoàn toàn thu được 5,688g chất rắn. Khí thoát ra được hấp thụ hoàn toàn vào 200ml dung dịch Ba(OH)2 0,4M thu được m gam kết tủa A.
a) Tính khối lượng mỗi muối cacbonat trong hỗn hợp
b) Tính khối lượng chất kết tủa tạo thành
ai đó lm ơn júp mình vs mình đag gấp, thanks nhiu
Đúng 0
Bình luận (0)
Nung 10g hỗn hợp MgCO3, CaCO3, và Al2O3 trong đó Al2O3 chiếm 10% về khối lượng đến khi các phản ứng xảy ra hoàn toàn thu được 5,688g chất rắn. Khí thoát ra được hấp thụ hoàn toàn vào 200ml dung dịch Ba(OH)2 0,4M thu được m gam kết tủa A.
a) Tính khối lượng mỗi muối cacbonat trong hỗn hợp
b) Tính khối lượng chất kết tủa tạo thành
Khối lượng Al2O3 là: 10 : 100 x 10 = 1 (g)
Khối lượng hai muối là: 10 - 1= 9 (g)
Gọi a, b lần lượt số mol MgCO3 và CaCO3
MgCO3 = MgO + CO2
a a (mol)
CaCO3 = CaO + CO2
b b (mol)
Chất rắn thu đc gồm MgO, CaO và Al2O3
Khí thoát ra là CO2
Khối lượng MgO và CaO là: 5,688 -1 = 4,688 (g)
Ta có hệ PT: 84a + 100b= 9(g)
40a + 56b= 4,688 (g)
=> a = 0,05(mol) ; b= 0,048 (mol)
Khối lượng MgCO3 là: 84 x 0,05 = 4,2 (g)
Khối lượng CaCO3 là: 100 x 0,048 = 4,8 (g)
Đổi 200ml = 0,2 l
Số mol Ba(OH)2 là: 0,4 x 0,2 = 0,08 (mol)
CO2 + Ba(OH)2 = BaCO3 + H2O
0,08 0,08 (mol)
Khối lượng kết tủa là:
0,08 x 197 = 15,76 (g)
Đúng 1
Bình luận (0)