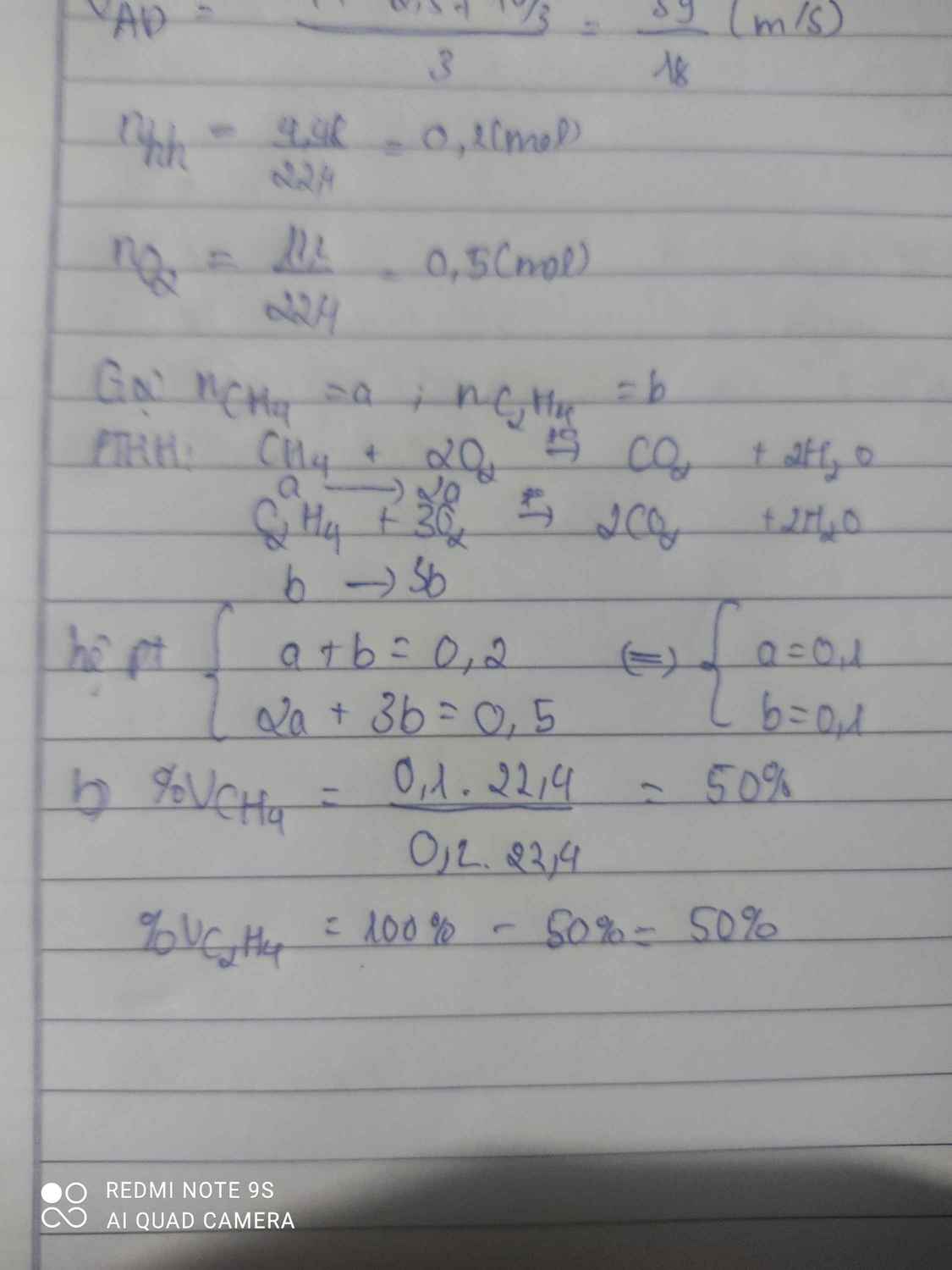Tính ${\Delta _r},H_{298}^0$các phản ứng đốt cháy hoàn toàn 1 mol mỗi chất C2H4(g), C2H6(g), CO(g). Biết các sản phẩm thu được đều ở thể khí.

Những câu hỏi liên quan
Dựa vào năng lượng liên kết, tính ${\Delta _r},H_{298}^0$ các phản ứng sau:
a) Các phản ứng đốt cháy hoàn toàn 1 mol mỗi chất C2H4, C2H6, H2 ở thể khí.
b) F2(g) + H2O(g) → 2HF(g) + ½ O2(g)
Dự đoán các phản ứng trên là thuận lợi hay không thuận lợi.
a)
- Xét phản ứng đốt cháy 1 mol C2H4
C2H4 (g) + 3O2 (g) → 2CO2 (g)+ 2H2O (g)
∆fH0298 = 1 x Eb (C2H4) + 3 x Eb (O2) - 2 x Eb (CO2) - 2 x Eb (H2O)
∆fH0298 = 1 x EC=C + 4 x EC-H + 3 x EO2 – 2 x 2EC=O – 2 x 2EO-H
∆fH0298 = 1x611 + 4x414 + 3x498 – 2x2x799 – 2x2x464 = -1291kJ
- Xét phản ứng đốt cháy 1 mol C2H6
C2H6 (g) + 7/2 O2 (g) → 2CO2 (g)+ 3H2O (g)
∆fH0298 = 1 x Eb (C2H6) + 7/2 x Eb (O2) - 2 x Eb (CO2) - 3 x Eb (H2O)
∆fH0298 = 1 x EC-C + 6 x EC-H + 7/2 x EO2 – 2 x 2EC=O – 3 x 2EO-H
∆fH0298 = 1x347 + 6x414 + 7/2 x498 – 2x2x799 – 3x2x464 = -1406kJ
- Xét phản ứng đốt cháy 1 mol CO
CO(g) + ½ O2 (g) → CO2(g)
∆fH0298 = 1 x Eb (CO) + 1/2 x Eb (O2) - 1 x Eb (CO2)
∆fH0298 = 1 x ECO + 1/2 x EO2 – 1 x 2EC=O
∆fH0298 = 1 x 1072 + 1/2 x 498– 1x2x799 = -277kJ
b)
F2(g) + H2O(g) → 2HF(g) + ½ O2 (g)
∆fH0298 = 1 x Eb (F2) + 1 x Eb (H2O) - 2 x Eb (HF) – 1/2 x Eb (O2)
∆fH0298 = 1 x EF-F + 1x2EO-H - 2 x EH-F - 1/2 x EO2
∆fH0298 = 1 x 159 + 2x464– 2x565 - 1/2 x 498= -292kJ
Các phản ứng trên đều có giá trị elthanpy âm => Các phản ứng trên đều thuận lợi
Đúng 0
Bình luận (0)
Cho hai phản ứng đốt cháy:
(1) C(s) + O2(g) → CO2(g) ${\Delta _r},H_{298}^0$ = -393,5 kJ
(2) 2Al(s) + 3/2 O2(g) → Al2O3(s) ${\Delta _r},H_{298}^0$ = -1675,7 kJ
Với cùng một khối lượng C và Al, chất nào khi đốt cháy tỏa ra nhiều nhiệt hơn?
Giả sử: 1 gam C và Al
+ 1 gam C có 1/12 mol
1 mol C : ${\Delta _r},H_{298}^0$ = -393,5 kJ
1/12 mol C ${\Delta _r},H_{298}^0$ = -32,79 kJ
+ 1 gam Al có 1/27 mol
2 mol Al : ${\Delta _r},H_{298}^0$= -1675,7 kJ
1/27mol Al : ${\Delta _r},H_{298}^0$= -31,03 kJ
⇒ Với cùng một khối lượng C và Al, C khi đốt cháy tỏa ra nhiều nhiệt hơn.
Đúng 0
Bình luận (0)
Cho phản ứng:CH4(g) + H2O(l) → CO(g) + 3H2(g) ${Delta _r},H_{298}^0$ 250 kJ.Ở điều kiện chuẩn, để thu được 1 gam H2, phản ứng này cần hấp thu nhiệt lượng bằng bao nhiêu.
Đọc tiếp
Cho phản ứng:
CH4(g) + H2O(l) → CO(g) + 3H2(g) ${\Delta _r},H_{298}^0$= 250 kJ.
Ở điều kiện chuẩn, để thu được 1 gam H2, phản ứng này cần hấp thu nhiệt lượng bằng bao nhiêu.
1 gam H2 ⇒ nH2 = $\frac{1}{2}$mol
3 mol H2 : ${\Delta _r},H_{298}^0$ = 250 kJ.
$\frac{1}{2}$ mol H2 : ${\Delta _r},H_{298}^0$ = 250. $\frac{1}{2}$ :3 = 41,67 kJ.
⇒ Để thu được 1 gam H2, phản ứng này cần hấp thu 41,67 kJ.
Đúng 0
Bình luận (0)
Craking n-butan thu được 35 mol hỗn hợp A gồm H2, CH4, C2H4, C2H6, C3H6, C4H8 và một phần butan chưa bị craking. Giả sử chỉ có các phản ứng tạo ra các sản phẩm trên. Cho A qua bình nước brom dư thấy còn lại 20 mol khí. Nếu đốt cháy hoàn toàn A thì thu được x mol CO2. Hiệu suất phản ứng tạo hỗn hợp A là: A. 57,14% B. 75,00% C. 42,86% D. 25,00%
Đọc tiếp
Craking n-butan thu được 35 mol hỗn hợp A gồm H2, CH4, C2H4, C2H6, C3H6, C4H8 và một phần butan chưa bị craking. Giả sử chỉ có các phản ứng tạo ra các sản phẩm trên. Cho A qua bình nước brom dư thấy còn lại 20 mol khí. Nếu đốt cháy hoàn toàn A thì thu được x mol CO2. Hiệu suất phản ứng tạo hỗn hợp A là:
A. 57,14%
B. 75,00%
C. 42,86%
D. 25,00%
Đáp án : B
Phương trình phản ứng:
C4H10 => C4H8 + H2 (1)
C4H10 => C3H6 + CH4 (2)
C4H10 => C2H4 + C2H6 (3)
Sau phản ứng còn C4H10 dư
từ (1), (2), (3):
n C4H8 = n H2
n C3H6 = n CH4
n C2H4 = n C2H6
và n C4H8 + n C3H6 + n C2H4 = n H2 + n CH4 + n C2H6 = n C4H10 đã bị cracking.
n anken bị dung dịch Br2 giữ lại = 35 - 20 = 15 mol --> n C4H10 dư = 20 - 15 = 5 mol
=> n C4H10 ban đầu = 5 + 15 = 20 mol
=> hiệu suất phản ứng = 15 x100%/20 = 75%
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 3,1 g Photpho trong bình chứa khí O2 . Sản phẩm thu được là điphotpho pentaoxit.
a. Hãy viết phương trình phản ứng xảy ra.
b. Tính thể tích khí O2 (ở đktc) đã tham gia phản ứng trên.
c. Tính khối lượng của chất được tạo thành.
Giải rồi cho mình công thức của mấy bài như vậy với ạ. Mình cảm ơn
nP = 3,1/31 = 0,1 (mol)
PTHH: 4P + 5O2 -t°-> 2P2O5
0,1---> 0,125--->0,05
VO2 = 0,125 . 22,4 = 2,8 (l)
mP2O5 = 0,05 . 142 = 7,1 (g)
Đúng 3
Bình luận (1)
\(n_P=\dfrac{3,1}{31}=0,1mol\)
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
0,1 0,125 0,05
\(V_{O_2}=0,125\cdot22,4=2,8l\)
\(m_{P_2O_5}=0,05\cdot142=7,1g\)
Đúng 3
Bình luận (1)
a,PTHH : \(4P+5O_2->2P_2O_5\)
b,
Số mol O2 tham gia phản ứng :
nO2 = 5/4.nP = 5/4 . 0,1 = 0,125 ( mol )
=> V O2 phản ứng : 0,125 . 22,4 = 2,8 ( lít )
c,
Số mol P2O5 : np2o5 = 1/2.np = 0,05 ( mol )
=> m = 142 . 0,05 = 7,1 (g)
Đúng 2
Bình luận (1)
Cracking n-butan thu được 35 mol hỗn hợp X gồm H2, CH4, C2H4, C2H6, C3H6, C4H8 và một phần butan chưa bị cracking. Giả sử chỉ có các phản ứng tạo ra các sản phẩm trên. Cho X qua bình nước brom dư thấy còn lại 20 mol khí. Nếu đốt cháy hoàn toàn X thì thu được a mol CO2. Giá trị của a là? A. 140. B. 70. C. 80. D. 40.
Đọc tiếp
Cracking n-butan thu được 35 mol hỗn hợp X gồm H2, CH4, C2H4, C2H6, C3H6, C4H8 và một phần butan chưa bị cracking. Giả sử chỉ có các phản ứng tạo ra các sản phẩm trên. Cho X qua bình nước brom dư thấy còn lại 20 mol khí. Nếu đốt cháy hoàn toàn X thì thu được a mol CO2. Giá trị của a là?
A. 140.
B. 70.
C. 80.
D. 40.
Đáp án C
Crackinh CH3-CH2-CH2-CH3
→ 35 mol hhX gồm H2, CH4, C2H4, C3H6, C4H8 và C4H10 dư.
X + Brom dư thì thu được 20 mol khí.
20 mol khí bao gồm CH4, C2H6, C3H8, C4H10dư và H2 cũng chính là số mol C4H10 ban đầu.
→ nC4H10ban đầu = 20 mol.
Đốt cháy butan ban đầu cũng chính là đốt cháy hhX → nCO2 = 20 x 4 = 80 mol
Đúng 0
Bình luận (0)
Để đốt cháy hoàn toàn 4,48 lít hỗn hợp khí X gồm CH4 và C2H4 cần dùng vừa đủ 11,2 lít khí oxi, sau phản ứng thu được sản phẩm gồm khí cacbon đioxit và hơi nước.
a) Viết các phương trình phản ứng xảy ra.
b) Tính % thể tích mỗi khí trong hỗn hợp X. Biết các thể tích khí đo ở đktc.
a, Tính thể tích của oxi (đktc) cần dùng để đốt cháy hết 3,1 gam P, biết phản ứng sinh ra chất rắn P2O5.
b, Đốt cháy hoàn toàn 1,12 lít khí CH4 (đktc) cần dùng V lít khí O2 (đktc), sau phản ứng thu được sản phẩm là khí cacbonic (CO2) và nước (H2O). Giá trị của V là
a, Theo giả thiết ta có: \(n_P=\dfrac{3,1}{31}=0,1\left(mol\right)\)
\(4P+5O_2--t^o->2P_2O_5\)
Ta có: \(n_{O_2}=\dfrac{5}{4}.n_P=0,125\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=0,125.22,4=2,8\left(l\right)\)
b, Theo giả thiết ta có: \(n_{CH_4}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(CH_4+2O_2--t^o->CO_2+2H_2O\)
Ta có: \(n_{O_2}=2.n_{CH_4}=0,1\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=2,24\left(l\right)\)
Đúng 1
Bình luận (0)
Câu 4. Đốt cháy hoàn toàn 1,12 lít khí C2H4, dẫn toàn bộ sản phẩm cháy vào bình đựng dung dịch Ca(OH)2 dư thu được m(g) kết tủa. a. Tính m b. Tính thể tích oxi và thể tích không khí cần dùng.( Biết thể tích khí đo ở đktc, oxi chiếm 20% thể tích không khí,
Đọc tiếp
Câu 4. Đốt cháy hoàn toàn 1,12 lít khí C2H4, dẫn toàn bộ sản phẩm cháy vào bình đựng dung dịch Ca(OH)2 dư thu được m(g) kết tủa.
a. Tính m
b. Tính thể tích oxi và thể tích không khí cần dùng.
( Biết thể tích khí đo ở đktc, oxi chiếm 20% thể tích không khí,
a, \(n_{C_2H_4}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
PT: \(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
Theo PT: \(n_{CaCO_3}=n_{CO_2}=2n_{C_2H_4}=0,1\left(mol\right)\)
\(\Rightarrow m_{CaCO_3}=0,1.100=10\left(g\right)\)
b, Theo PT: \(n_{O_2}=3n_{C_2H_4}=0,15\left(mol\right)\Rightarrow V_{O_2}=0,15.22,4=3,36\left(l\right)\)
\(\Rightarrow V_{kk}=\dfrac{V_{O_2}}{20\%}=16,8\left(l\right)\)
Đúng 2
Bình luận (0)