Nguyên tử Li (Z = 3) có 2 electron ở lớp K và 1 electron ở lớp L. So sánh năng lượng của electron giữa hai lớp theo mô hình Rutherford – Bohr.

Những câu hỏi liên quan
Các nguyên tố chu kì 2 có bao nhiêu lớp electron? Vẽ mô hình nguyên tử theo Rutherford – Bohr của Li và F để giải thích về sự khác biệt bán kính nguyên tử.
- Các nguyên tố chu kì 2 có 2 lớp electron.
- Mô hình nguyên tử của Li (Z = 3) và F (Z = 9) theo Rutherford – Bohr như sau:

- Nguyên tố Li và F đều có 2 lớp electron nên cùng chu kì 2, số đơn vị điện tích hạt nhân của Li nhỏ hơn F. Vì vậy bán kính nguyên tử Li lớn hơn nguyên tử F.
Đúng 0
Bình luận (0)
Cho biết sự phân bố electron theo lớp của các nguyên tử H, He, Li như sau:
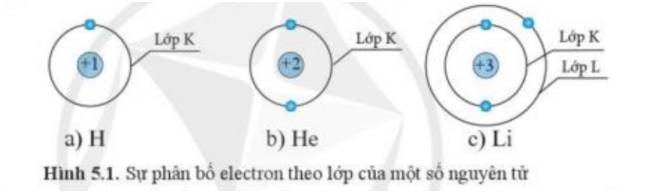
Dựa vào hình 5.1, hãy cho biết số electron tối đa ở lớp K của các nguyên tử có số hiệu nguyên tử Z $ \geqslant $ 2 là bao nhiêu. Theo em, thứ tự phân bố electron vào lớp vỏ nguyên tử như thế nào?
Dựa vào hình 5.1 số electron tối đa ở lớp K của các nguyên tử có số hiệu nguyên tử Z ≥ 2 là 2.
Các electron sẽ được phân bố lần lượt vào các lớp theo chiều từ gần hạt nhân ra ngoài. Mỗi lớp có số electron đối đa xác định, như lớp thứ nhất có tối đa 2 electron, lớp thứ 2 có tối đa 8 electron,…
Đúng 0
Bình luận (0)
Cấu hình electron của nguyên tử nhôm (Z = 13) là 1s22s22p63s23p1. Vậy:
A. Lớp thứ nhất (Lớp K) có 2 electron.
B. Lớp thứ hai (Lớp L) có 8 electron.
C. Lớp thứ ba (Lớp M) có 3 electron.
D. Lớp ngoài cùng có 1 electron.
Tìm câu sai.
Câu D là sai.
Lớp ngoài cùng là 3s23p1 có 3 electron
Đúng 0
Bình luận (0)
Hãy dự đoán xu hướng nhường, nhận electron của mỗi nguyên tử trong từng cặp nguyên tử sau. Vẽ mô hình (hoặc viết số electron theo lớp) quá trình các nguyên tử nhường, nhận electron để tạo ion
a) K (Z = 19) và O (Z = 8).
b) Li (Z = 3) và F (Z = 9).
c) Mg (Z = 12) và P (Z = 15).
a)
- K (Z = 19): 1s22s22p63s23p64s1 => Có 1 electron ở lớp vỏ ngoài cùng => Xu hướng nhường 1 electron
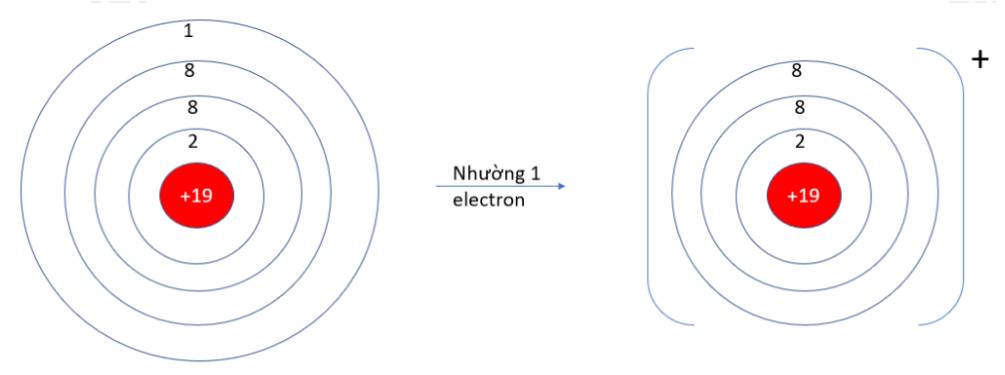
- O (Z = 8): 1s22s22p4 => Có 6 electron ở lớp vỏ ngoài cùng => Xu hướng nhận 2 electron

b)
- Li (Z = 3): 1s22s1 => Có 1 electron ở lớp vỏ ngoài cùng => Xu hướng nhường 1 electron
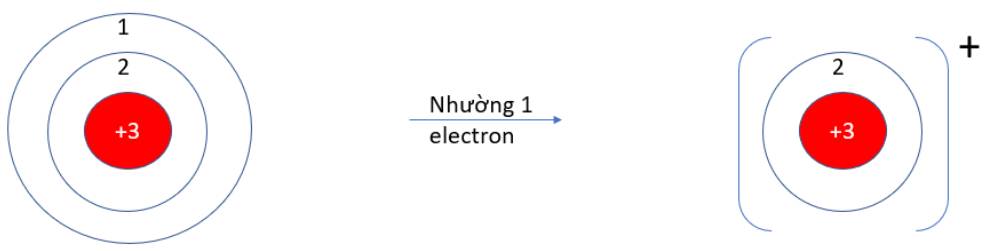
- F (Z = 9): 1s22s22p5 => Có 7 electron ở lớp vỏ ngoài cùng => Xu hướng nhận 1 electron
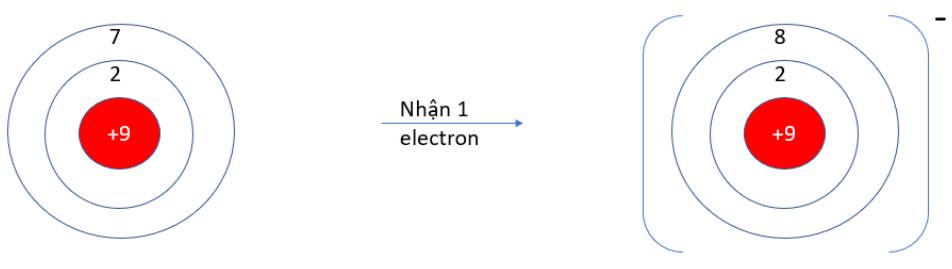
c)
- Mg (Z = 12): 1s22s22p63s2 => Có 2 electron ở lớp vỏ ngoài cùng => Xu hướng nhường 2 electron
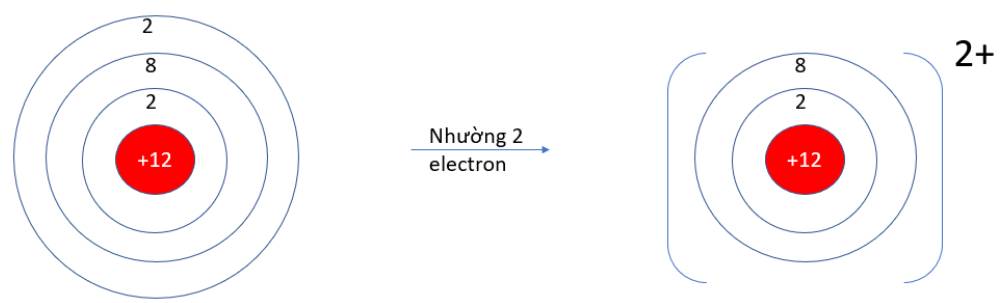
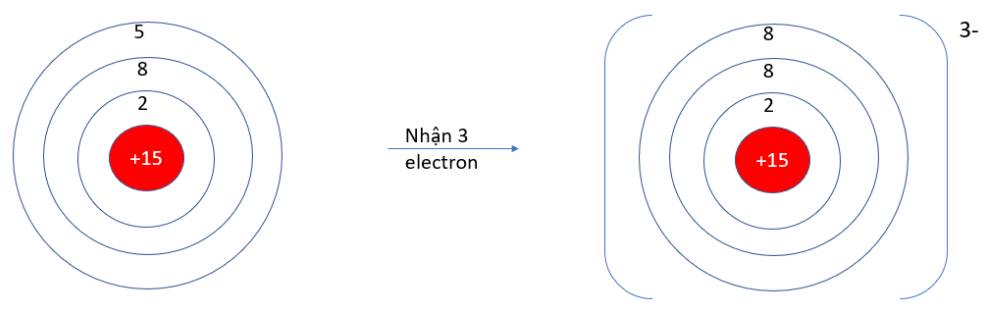
- P (Z = 15): 1s22s22p63s23p3 => Có 5 electron ở lớp vỏ ngoài cùng => Xu hướng nhận 3 electron
Đúng 0
Bình luận (0)
Sử dụng mô hình Rutherford – Bohr, hãy cho biết khi electron của nguyên tử H hấp thụ một năng lượng phù hợp, electron đó sẽ chuyển ra xa hay tiến gần vào hạt nhân hơn. Giải thích.
Theo mô hình Rutherford – Bohr Electron ở càng xa hạt nhân thì có năng lượng càng cao.
Vì thế nên khi electron của nguyên tử H hấp thụ một năng lượng phù hợp, electron đó sẽ chuyển ra xa hạt nhân hơn.
Đúng 0
Bình luận (0)
Tìm hiểu mối quan hệ giữa số electron ở lớp ngoài cùng của nguyên tử các nguyên tố với số thứ tự của nhómChuẩn bị: 4 mô hình sắp xếp electron ở vỏ nguyên tử của Li, Na, F, Cl theo mẫu mô tả trong Hình 4.4.Quan sát các mô hình đã chuẩn bị, thảo luận và trả lời câu hỏi:1. Hãy cho biết nguyên tử các nguyên tố nào có cùng số electron ở lớp ngoài cùng2. Hãy so sánh số electron lớp ngoài cùng của nguyên tử các nguyên tố với số thứ tự nhóm của các nguyên tố đó
Đọc tiếp
Tìm hiểu mối quan hệ giữa số electron ở lớp ngoài cùng của nguyên tử các nguyên tố với số thứ tự của nhóm
Chuẩn bị: 4 mô hình sắp xếp electron ở vỏ nguyên tử của Li, Na, F, Cl theo mẫu mô tả trong Hình 4.4.
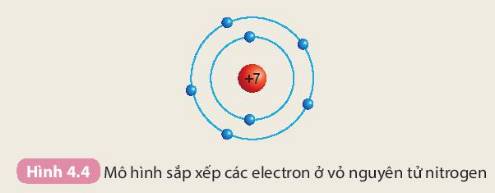
Quan sát các mô hình đã chuẩn bị, thảo luận và trả lời câu hỏi:
1. Hãy cho biết nguyên tử các nguyên tố nào có cùng số electron ở lớp ngoài cùng
2. Hãy so sánh số electron lớp ngoài cùng của nguyên tử các nguyên tố với số thứ tự nhóm của các nguyên tố đó
1:
Nguyên tử Li, Na có cũng số electron ở lớp ngoài cùng
Nguyên tử F, Cl có cũng số electron ở lớp ngoài cùng
2: Số electron lớp ngoài cùng của nguyên tử các nguyên tố chính là số thứ tự nhóm của các nguyên tố
Đúng 0
Bình luận (0)
Biết rằng các electron của nguyên tử X được phân bố trên bốn lớp electron (K, L, M, N), lớp ngoài cùng có 5 electron. Viết cấu hình electron và xác định số electron ở lớp M của X. A. 8. B. 18. C. 11. D. 13.
Đọc tiếp
Biết rằng các electron của nguyên tử X được phân bố trên bốn lớp electron (K, L, M, N), lớp ngoài cùng có 5 electron. Viết cấu hình electron và xác định số electron ở lớp M của X.
A. 8.
B. 18.
C. 11.
D. 13.
Đáp án B
Các electron của nguyên tử X được phân bố trên bốn lớp electron (K, L, M, N)
→ X có lớp ngoài cùng với n = 4
Lớp ngoài cùng có 5 eletron → X có cấu hình electron: 1s22s22p63s23p63d104s24p3
→ Số electron ở lớp M (n = 3) của X là 2 + 6 + 10 = 18 → Chọn B.
Đúng 0
Bình luận (0)
Biết rằng các electron của nguyên tử X được phân bố trên bốn lớp electron (K, L, M, N), lớp ngoài cùng có 5 electron. Viết cấu hình electron và xác định số electron ở lớp M của X. A. 8. B. 18. C. 11. D. 13.
Đọc tiếp
Biết rằng các electron của nguyên tử X được phân bố trên bốn lớp electron (K, L, M, N), lớp ngoài cùng có 5 electron. Viết cấu hình electron và xác định số electron ở lớp M của X.
A. 8.
B. 18.
C. 11.
D. 13.
Các eletron của nguyên tử X được phân bố trên bốn lớp electron (K, L, M, N)
→ X có lớp ngoài cùng với n = 4
Lớp ngoài cùng có 5 electron → X có cấu hình electron: 1s22s22p63s23d103p104s24p3
→ Số electron ở lớp M (n =3) của X là 2 + 6 + 10 = 18 → Chọn B.
Đúng 0
Bình luận (0)
Tìm hiểu mối quan hệ giữa số lớp electron của nguyên tử các nguyên tố với số thứ tự của chu kìChuẩn bị: 6 mô hình sắp xếp electron ở vỏ nguyên tử của sáu nguyên tố H, He, Li, Be, C, N theo mẫu được mô tả trong Hình 4.4Quan sát các mô hình đã chuẩn bị, thảo luận và thực hiện các yêu cầu sau:1. Hãy cho biết số lớp electron của nguyên tử các nguyên tố trên.2. So sánh số lớp electron của nguyên tử các nguyên tố trên với số thứ tự chu kì của các nguyên tố đó.
Đọc tiếp
Tìm hiểu mối quan hệ giữa số lớp electron của nguyên tử các nguyên tố với số thứ tự của chu kì
Chuẩn bị: 6 mô hình sắp xếp electron ở vỏ nguyên tử của sáu nguyên tố H, He, Li, Be, C, N theo mẫu được mô tả trong Hình 4.4
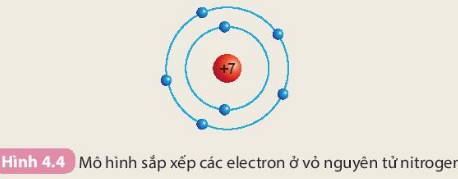
Quan sát các mô hình đã chuẩn bị, thảo luận và thực hiện các yêu cầu sau:
1. Hãy cho biết số lớp electron của nguyên tử các nguyên tố trên.
2. So sánh số lớp electron của nguyên tử các nguyên tố trên với số thứ tự chu kì của các nguyên tố đó.
1. Nguyên tử nguyên tố H , nguyên tử nguyên tố He có 1 lớp e
Nguyên tử nguyên tố Li, Be, C, N có 2 lớp e.
2. STT chu kì của nguyên tử nguyên tố H, He (1) < STT chu kì của nguyên tử nguyên tố Li, Be, C, N (2)
Đúng 0
Bình luận (0)










