cho 12gam hỗn hợp cu và cuo tác dụng hoàn toàn với dung dịch hcl loãng sau phản ứng thấy còn lại m gam chất rắn không tan, lọc lấy lượng chất rắn này vào dung dịch h2so4 đặc nóng thì thu được 2,24 lít khi so2

Những câu hỏi liên quan
cho 24 gam hỗn hợp CuO và Cu tác dụng hết với dung dịch H2SO4 loãng dư . Sau phản ứng , lọc lấy chất rắn không tan cho vào dung dịch H2SO4 đặc nóng đến khi phản ứng kết thúc thu được 5,6 lít khí A(đktc)
-viết pthh của các chất phản ứng và cho biết tên khí A
-tính thành phần phần trăm khối lượng Cu có trong hỗn hợp
PT: \(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
\(Cu+2H_2SO_{4\left(đ\right)}\underrightarrow{t^o}CuSO_4+SO_2+2H_2O\)
Ta có: \(n_{SO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Theo PT: \(n_{Cu}=n_{SO_2}=0,25\left(mol\right)\)
\(\Rightarrow\%m_{Cu}=\dfrac{0,25.64}{24}.100\%\approx66,67\%\)
Đúng 2
Bình luận (0)
11/ Cho 10 gam hỗn hợp Cu và CuO tác dụng với dung dịch H2SO4 loãng dư. Lọc lấy chất rắn không tan cho phản ứng với dung dịch H2SO4 đặc, nóng thu được 1,12 lít khí (đktc ) .
a. Viết phương trình
b. Tính thành phần trăm theo khối lượng mỗi chất rắn có trong hỗn hợp đầu
a. PTHH:
\(Cu+H_2SO_4--\times-->\)
\(CuO+H_2SO_4--->CuSO_4+H_2O\left(1\right)\)
\(Cu+2H_2SO_{4_{đặc}}\overset{t^o}{--->}CuSO_4+SO_2+2H_2O\left(2\right)\)
Ta có: \(n_{SO_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Theo PT(2): \(n_{Cu}=n_{SO_2}=0,05\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,05.64=3,2\left(g\right)\)
\(\Rightarrow\%_{m_{Cu}}=\dfrac{3,2}{10}.100\%=32\%\)
\(\%_{m_{CuO}}=100\%-32\%=68\%\)
Đúng 1
Bình luận (0)
Cho m gam hỗn hợp X gồm Cu, CuO và Fe3O4 tác dụng với dung dịch HCl(loãng, dư), thu được dung dịch Y và còn lại 0,25 gam rắn không tan. Cô cạn Y rồi cho hỗn hợp muối thu được phản ứng với dung dịch AgNO3 dư, thu được 113,44 gam kết tủa. Mặt khác, hoàn tan hoàn toàn m gam X trong dung dịch H2SO4 ( đặc, nóng, dư), thu được 5,04 lít SO2 ( đktc, sản phẩm khử duy nhất của S+6). Giá trị của m là A. 20 B. 24 C. 28 D. 32
Đọc tiếp
Cho m gam hỗn hợp X gồm Cu, CuO và Fe3O4 tác dụng với dung dịch HCl(loãng, dư), thu được dung dịch Y và còn lại 0,25 gam rắn không tan. Cô cạn Y rồi cho hỗn hợp muối thu được phản ứng với dung dịch AgNO3 dư, thu được 113,44 gam kết tủa. Mặt khác, hoàn tan hoàn toàn m gam X trong dung dịch H2SO4 ( đặc, nóng, dư), thu được 5,04 lít SO2 ( đktc, sản phẩm khử duy nhất của S+6). Giá trị của m là
A. 20
B. 24
C. 28
D. 32
Tiến hành phản ứng nhiệt nhôm m gam hỗn hợp A gồm Al và một oxit sắt thu được hỗn hợp chất rắn B. Cho B tác dụng với dung dịch NaOH dư thu được dung dịch C, phần không tan D và 0,672 lít khí H2 (đktc). Cho từ từ dung dịch HCl vào dung dịch C đến khi thu được lượng kết tủa lớn nhất rồi lọc và nung kết tủa đến khối lượng không đổi được 5,1 gam chất rắn. Phần không tan D cho tác dụng hết với dung dịch H2SO4 đặc nóng. Sau phản ứng chỉ thu được dung dịch E chứa một muối sắt duy nhất và 2,688 lít khí...
Đọc tiếp
Tiến hành phản ứng nhiệt nhôm m gam hỗn hợp A gồm Al và một oxit sắt thu được hỗn hợp chất rắn B. Cho B tác dụng với dung dịch NaOH dư thu được dung dịch C, phần không tan D và 0,672 lít khí H2 (đktc). Cho từ từ dung dịch HCl vào dung dịch C đến khi thu được lượng kết tủa lớn nhất rồi lọc và nung kết tủa đến khối lượng không đổi được 5,1 gam chất rắn. Phần không tan D cho tác dụng hết với dung dịch H2SO4 đặc nóng. Sau phản ứng chỉ thu được dung dịch E chứa một muối sắt duy nhất và 2,688 lít khí SO2 duy nhất (đktc). (Biết các phản ứng xảy ra hoàn toàn; dung dịch E không hòa tan được bột Cu). Thành phần % khối lượng của oxit sắt trong hỗn hợp A là
A. 76,19%.
B. 70,33%.
C. 23,81%.
D. 29,67%.
Đáp án A
· Có n Al ( B ) = 2 3 . n H 2 = 2 3 . 0 , 672 22 , 4 = 0 , 02 mol
· Chất rắn thu được sau khi nung là Al2O3:
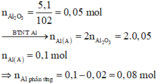
· Quy đổi A tương đương với hỗn hợp gồm 0,1 mol Al, a mol Fe, b mol O
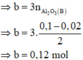
· Phần không tan D gồm Fe và oxit sắt + H2SO4 ® Dung dịch E + 0,12 mol SO2
Dung dịch E chứa một muối sắt duy nhất và không hòa tan được bột Cu
Þ Muối sắt là FeSO4.
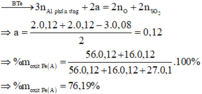
Đúng 0
Bình luận (0)
Một hỗn hợp X gồm 0,2 mol Cu và 0,1 mol Fe3O4. Cho X vào 400 ml dung dịch H2SO4 1M. Sau khi phản ứng kết thúc thu được dung dịch A và còn lại x gam chất rắn B không tan. Cho dung dịch A tác dụng với dung dịch NaOH dư rồi đun nóng trong không khí cho các phản ứng xảy ra hoàn toàn. Lọc lấy kết tủa, nung đến khối lượng không đổi thu được y gam chất rắn C. Xác định giá trị của x và y.
Đọc tiếp
Một hỗn hợp X gồm 0,2 mol Cu và 0,1 mol Fe3O4. Cho X vào 400 ml dung dịch H2SO4 1M. Sau khi phản ứng kết thúc thu được dung dịch A và còn lại x gam chất rắn B không tan. Cho dung dịch A tác dụng với dung dịch NaOH dư rồi đun nóng trong không khí cho các phản ứng xảy ra hoàn toàn. Lọc lấy kết tủa, nung đến khối lượng không đổi thu được y gam chất rắn C. Xác định giá trị của x và y.
Pt:
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
0,1 → 0,4 0,1 0,1
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
0,1 ←0,1 → 0,1 0,2
Rắn B là 0,1 mol Cu → x = 6,4 (g)
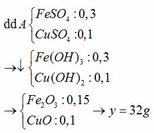
Đúng 0
Bình luận (0)
Cho 1,6g hỗn hợp A gồm Mg và Cu tác dụng với dung dịch HCl (dư) thu đc 2,24 lít khí (ở đktc) a) Tính nồng độ mol của 200ml dung dich HCl tham gia phản ứng b) lọc lấy toàn bộ chất rắn không tan cho tác dụng với H2SO4 đặc nóng tính thể tích khí thoát ra
a, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PT: \(n_{HCl}=2n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow C_{M_{HCl}}=\dfrac{0,2}{0,2}=1\left(M\right)\)
b, Theo PT: \(n_{Mg}=n_{H_2}=0,1\left(mol\right)\)
⇒ mMg = 0,1.24 = 2,4 (g) > mA → vô lý
Bạn xem lại xem đề cho bao nhiêu gam hh A nhé.
Đúng 3
Bình luận (0)
\(a)n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\\ Mg+2HCl\rightarrow MgCl_2+H_2\)
0,1 0,2 0,1 0,1
\(C_{M_{HCl}}=\dfrac{0,2}{0,2}=1M\\ b)m_{\downarrow}=m_{Cu}=1,6-0,1.24=-0,8\rightarrowĐề.sai\)
Đúng 2
Bình luận (0)
BÀI 1) Lấy 8 gam hỗn hợp Cu, Ag, Fe2O3 tạo ra hỗn hợp hoà tan vào dung dịch H2SO4 loãng. Sau khi phản ứng kết thúc, lọc lấy chất rắn không tan cho vào dung dịch H2SO4 đặc, nóng 2,24 lít (đktc)a) Viết phương trình phản ứng xảy ra, gọi tên khi Ab) Tính % khối lượng các chất trong hỗn hợp ban đầuBÀI 2) Cho 120 gam dung dịch NaOH 20% phản ứng với khí CO2 ở đktc để tạo thành hỗn hợp muối trung hoà và muối axit theo tỉ lệ số mol là 3:2. a) Tính thể tích khí CO2 cần dùng
Đọc tiếp
BÀI 1) Lấy 8 gam hỗn hợp Cu, Ag, Fe2O3 tạo ra hỗn hợp hoà tan vào dung dịch H2SO4 loãng. Sau khi phản ứng kết thúc, lọc lấy chất rắn không tan cho vào dung dịch H2SO4 đặc, nóng 2,24 lít (đktc)
a) Viết phương trình phản ứng xảy ra, gọi tên khi A
b) Tính % khối lượng các chất trong hỗn hợp ban đầu
BÀI 2) Cho 120 gam dung dịch NaOH 20% phản ứng với khí CO2 ở đktc để tạo thành hỗn hợp muối trung hoà và muối axit theo tỉ lệ số mol là 3:2.
a) Tính thể tích khí CO2 cần dùng
em không cần gấp lắm nhưng cám ơn bạn đã cmt
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn hỗn hợp gồm FeS2 và Ag2S với số mol bằng nhau thu được 3,696 lít SO2 (đktc) và chất rắn B. Cho B tác dụng với dung dịch H2SO4 loãng dư, sau phản ứng hoàn toàn thấy còn lại m gam chất rắn không tan. Giá trị của m là: A. 13,64 B. 11,88 C. 17,16 D. 8,91
Đọc tiếp
Đốt cháy hoàn toàn hỗn hợp gồm FeS2 và Ag2S với số mol bằng nhau thu được 3,696 lít SO2 (đktc) và chất rắn B. Cho B tác dụng với dung dịch H2SO4 loãng dư, sau phản ứng hoàn toàn thấy còn lại m gam chất rắn không tan. Giá trị của m là:
A. 13,64
B. 11,88
C. 17,16
D. 8,91
Đáp án B
nFeS2 = nAg2S =1/3 nSO2 = 0,055 mol
Chất rắn B gồm có Fe2O3 và Ag, cho qua H2SO4 thì chỉ còn lại Ag
⇒m=0,055 . 2 .108 = 11,88
Đúng 0
Bình luận (0)
Tiến hành phản ứng nhiệt nhôm m gam hỗn hợp gồm Al và FexOy thu được hỗn hợp chất rắn X. Cho X tác dụng với dung dịch NaOH dư thu được dung dịch Y, phần không tan Z và 0,672 lít khí H2. Cho dung dịch HCl vào Y đến khi được lượng kết tủa lớn nhất, lọc kết tủa, nung tới khối lượng không đổi thu được 5,1 gam chất rắn. Cho Z tác dụng với dung dịch H2SO4 đặc nóng (lượng ít nhất) sau phản ứng chỉ thu được dung dịch E chứa một muối sắt duy nhất và 2,688 lít khí SO2. Biết các khí đều đo ở đktc, các phả...
Đọc tiếp
Tiến hành phản ứng nhiệt nhôm m gam hỗn hợp gồm Al và FexOy thu được hỗn hợp chất rắn X. Cho X tác dụng với dung dịch NaOH dư thu được dung dịch Y, phần không tan Z và 0,672 lít khí H2. Cho dung dịch HCl vào Y đến khi được lượng kết tủa lớn nhất, lọc kết tủa, nung tới khối lượng không đổi thu được 5,1 gam chất rắn. Cho Z tác dụng với dung dịch H2SO4 đặc nóng (lượng ít nhất) sau phản ứng chỉ thu được dung dịch E chứa một muối sắt duy nhất và 2,688 lít khí SO2. Biết các khí đều đo ở đktc, các phản ứng xảy ra hoàn toàn. Công thức phân tử của oxit sắt và phần trăm khối lượng của nó trong m gam hỗn hợp ban đầu là
A. FeO và 76,19%
B. FeO và 94,23%
C. Fe2O3 và 70,33%
D. Fe2O3 và 80,07%