Biết nhiệt độ sôi của ethanol là 78,3 oC, propane là -42,1 oC và dimethyl ether là -24,8 oC. Giải thích sự khác biệt đó.

Những câu hỏi liên quan
Ethanol và dimethyl ether có cùng công thức phân tử là C2H6O. Tuy nhiên, dimethyl ether hầu như không tan trong nước và sôi ở -24 oC, còn ethanol tan vô hạn trong nước và sôi ở 78 oC; dimethyl ether không tác dụng với sodium, trong khi ethanol tác dụng với sodium giải phóng hydrogen, … Điều gì gây ra sự khác biệt về tính chất của hai hợp chất có cùng công thức phân tử này?
Đọc tiếp
Ethanol và dimethyl ether có cùng công thức phân tử là C2H6O. Tuy nhiên, dimethyl ether hầu như không tan trong nước và sôi ở -24 oC, còn ethanol tan vô hạn trong nước và sôi ở 78 oC; dimethyl ether không tác dụng với sodium, trong khi ethanol tác dụng với sodium giải phóng hydrogen, … Điều gì gây ra sự khác biệt về tính chất của hai hợp chất có cùng công thức phân tử này?
Do liên kết của nguyên tử O trong phân tử ở các vị trí khác nhau.
Đúng 0
Bình luận (0)
Các hợp chất propane, dimethyl ether và ethanol có phân tử khối tương đương nhau và có một số tính chất như sau:
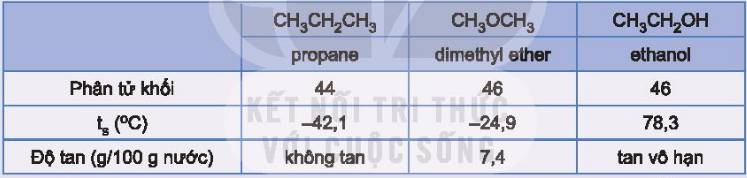
Hãy giải thích tại sao ethanol có nhiệt độ sôi cao hơn và tan trong nước tốt hơn so với hai chất còn lại.
Do các phân tử ethanol có thể tạo liên kết hydrogen với nhau và với nước.
Đúng 0
Bình luận (0)
Cho các chất có công thức C2H6, C2H5Cl, C2H5OH, C6H5CH2OH và nhiệt độ sôi của chúng (không theo thứ tự) là 78,3 oC, -89 oC, 12,3 oC, 205,0 oC. Hãy dự đoán nhiệt độ sôi tương ứng với mỗi chất trên. Giải thích.
Dự đoán nhiệt độ sôi các chất như sau:
Chất | C2H6 | C2H5Cl | C2H5OH | C6H5CH2OH |
to sôi | -89 oC | 12,3 oC | 78,3 oC | 205 oC |
Giải thích dự đoán:
- Do tạo được liên kết hydrogen liên phân tử nên các alcohol có nhiệt độ sôi cao hơn các hydrocarbon hoặc dẫn xuất halogen có phân tử khối tương đương.
- Nhiệt độ sôi của các alcohol tăng dần khi phân tử khối tăng.
Đúng 0
Bình luận (0)
Cho các chất có công thức sau: C2H6, C2H5OH, HCH = O, CH3CH = O, CH3CH2CH=O và các dữ liệu nhiệt độ sôi là 78,3 oC, -89 oC, 21 oC, -21 oC, 49 oC (không theo thứ tự). Hãy dự đoán nhiệt độ sôi tương ứng với mỗi mẫu chất trên. Giải thích.
Giải thích:
+ Các phân tử C2H5OH có liên kết hydrogen liên phân tử và liên kết hydrogen với nước, do đó nhiệt độ sôi của C2H5OH lớn hơn so với các chất còn lại.
+ Các aldehyde có nhiệt độ sôi cao hơn nhiều so với hydrocarbon C2H6.
+ Nhiệt sộ sôi của các aldehyde tăng theo chiều tăng của phân tử khối.
=> Nhiệt độ sôi của các chất được sắp xếp theo thứ tự giảm dần là: C2H5OH, CH3CH2CH=O, CH3CH=O, HCH=O, C2H6
Đúng 0
Bình luận (0)
Ethanol và dimethyl ether có cùng công thức phân tử là C2H6O. Tuy nhiên, dimethyl ether hầu như không tan trong nước và sôi ở –24 °C, còn ethanol tan vô hạn trong nước và sôi ở 78 °C; dimethyl ether không tác dụng với sodium, trong khi ethanol tác dụng với sodium giải phóng hydrogen,... Điều gì gây ra sự khác biệt về tính chất của hai hợp chất có cùng công thức phân tử này?
Cho các chất có công thức: CH3F, CH3Cl, CH3Br, CH3I và nhiệt độ sôi của chúng (không theo thứ tự) là 42 oC, 4 oC, -24 oC và -78 oC. Hãy dự đoán nhiệt độ sôi tương ứng với mỗi chất trên. Giải thích.
Theo nguyên tử khối của Halogen, ta sẽ có: \(M_F< M_{Cl}< M_{Br}< M_I\)
Do đó: Nhiệt độ sôi tương ứng của chúng sẽ tăng dần
=> Nhiệt độ sôi của CH3F, CH3Cl, CH3Br, CH3I lần lượt là -78 độ C, -24 độ C, 4 độ C và 24 độ C
Đúng 1
Bình luận (0)
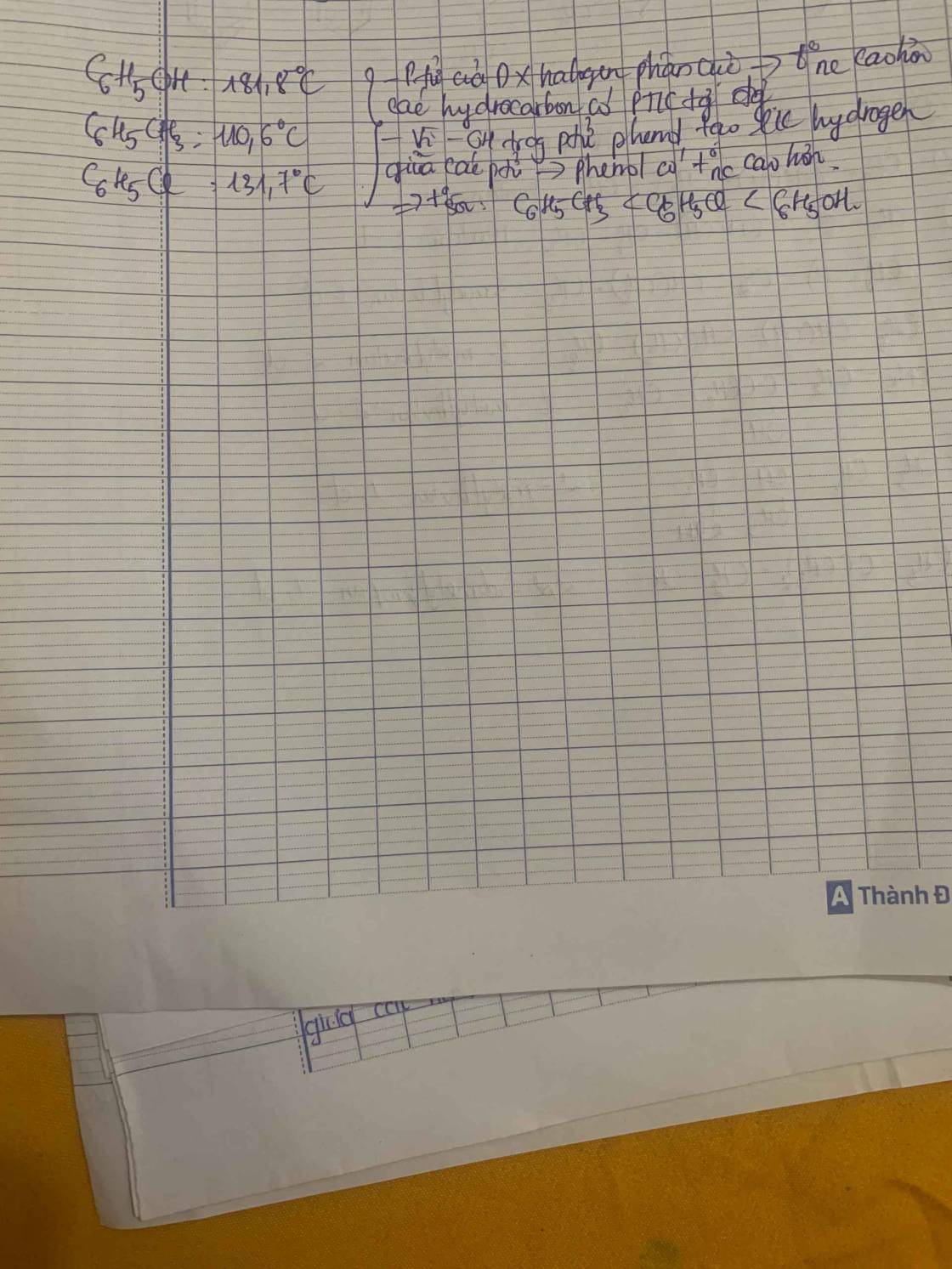
Cho các chất có công thức sau: C6H5OH, C6H5CH3, C6H5Cl và các giá trị nhiệt độ sôi (không theo thứ tự) là 110,6 oC, 131,7 oC, 181,8 oC. Hãy dự đoán nhiệt độ sôi tương ứng với mỗi chất trên. Giải thích.
Dự đoán nhiệt độ sôi các chất như sau:
Chất | C6H5CH3 | C6H5Cl | C6H5OH |
Nhiệt độ sôi | 110 oC | 132 oC | 182 oC |
Giải thích:
- Do có nhóm – OH trong phân tử nên phenol tạo ra liên kết hydrogen giữa các phân tử. Do vậy, phenol có nhiệt độ sôi cao hơn C6H5Cl (có phân tử khối tương đương).
- Do liên kết C – Cl phân cực nên C6H5Cl có nhiệt độ sôi cao hơn C6H5CH3 (có phân tử khối tương đương).
Đúng 0
Bình luận (0)
Cho hai nhiệt kế rượu và thủy ngân. Dùng nhiệt kế nào có thể đo được nhiệt độ của nước đang sôi? Cho biết nhiệt độ sôi của rượu và thủy ngân lần lượt là 80
O
C
và 357
O
C
A. Cả nhiệt kế thủy ngân và nhiệt kế rượu. B. Không thể dùng nhiệt kế thủy ngân và nhiệt kế rượu. C. Nhiệt kế rượu. D. Nhiệt kế thủy ngân
Đọc tiếp
Cho hai nhiệt kế rượu và thủy ngân. Dùng nhiệt kế nào có thể đo được nhiệt độ của nước đang sôi? Cho biết nhiệt độ sôi của rượu và thủy ngân lần lượt là 80 O C và 357 O C
A. Cả nhiệt kế thủy ngân và nhiệt kế rượu.
B. Không thể dùng nhiệt kế thủy ngân và nhiệt kế rượu.
C. Nhiệt kế rượu.
D. Nhiệt kế thủy ngân
- Nước sôi ở 100 O C .
- Vì rượu sôi ở 80 O C < 100 O C → không thể dùng nhiệt kế rượu để đo nhiệt độ của nước đang sôi.
⇒ Đáp án D
Đúng 1
Bình luận (0)
Cho các nhiệt độ sôi: 100,7 oC ; 21oC ; – 23oC ; 78,3oC. Đó là nhiệt độ sôi tương ứng của: A. HCOOH, CH3OCH3, CH3CHO, C2H5OH B. C2H5OH, CH3OCH3, CH3CHO, HCOOH C. HCOOH, CH3CHO, CH3OCH3, C2H5OH D. HCOOH, CH3CHO, C2H5OH ,CH3OCH3
Đọc tiếp
Cho các nhiệt độ sôi: 100,7 oC ; 21oC ; – 23oC ; 78,3oC. Đó là nhiệt độ sôi tương ứng của:
A. HCOOH, CH3OCH3, CH3CHO, C2H5OH
B. C2H5OH, CH3OCH3, CH3CHO, HCOOH
C. HCOOH, CH3CHO, CH3OCH3, C2H5OH
D. HCOOH, CH3CHO, C2H5OH ,CH3OCH3
Các chất cùng khối lượng mol nên ta xét đến khả năng tạo liên kết hidro và độ cồng kềnh của phân tử . Axit tạo liên kết H mạnh nhất, tiếp đó là ancol => 2 chất có nhiệt độ sôi cao nhất và nhì
=> do aceton có cấu trúc cồng kềnh hơn nên có nhiệt độ sôi thấp hơn
=>C
Đúng 0
Bình luận (0)