Cho các hợp chất: hexane, bromoethane, ethanol, phenol. Trong số các hợp chất này, hợp chất tan tốt nhất trong nước là
A. hexane. B. bromoethane. C. ethanol. D. phenol.
Các hợp chất propane, dimethyl ether và ethanol có phân tử khối tương đương nhau và có một số tính chất như sau:
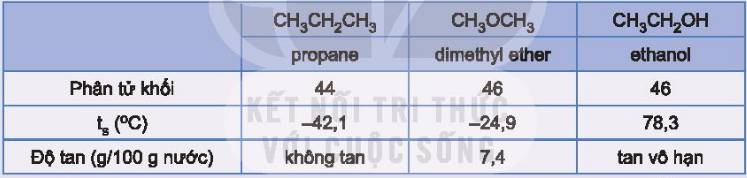
Hãy giải thích tại sao ethanol có nhiệt độ sôi cao hơn và tan trong nước tốt hơn so với hai chất còn lại.
Do các phân tử ethanol có thể tạo liên kết hydrogen với nhau và với nước.
Cho bốn hợp chất sau: ethanol, propanal, acetone, acetic acid.
a) Chất nào trong các chất trên có nhiệt độ sôi cao nhất?
b) Trình bày cách phân biệt các chất trên bằng phương pháp hoá học.
Tham khảo:
a) Trong 4 chất trên acetic acid có nhiệt độ sôi cao nhất. Do phân tử acetic acid chứa nhóm carbonyl phân cực, các phân tử carboxylic acid liên kết hydrogen với nhau tạo thành dạng dimer hoặc dạng liên phân tử.
b) Cách phân biệt: ethanol, propanal, acetone, acetic acid:
- Trích mẫu thử.
- Cho vào mỗi mẫu thử 1 mẩu quỳ tím:
+ Quỳ tím chuyển sang màu đỏ → acetic acid (CH3COOH).
+ Quỳ tím không đổi màu → ethanol, propanal, acetone (nhóm I).
- Cho từng mẫu thử ở nhóm I tác dụng với Na:
+ Mẩu Na tan dần, có khí thoát ra → ethanol (C2H5OH).
Phương trình hoá học: 2C2H5OH + 2Na → 2C2H5ONa + H2.
+ Không hiện tượng → propanal, acetone (nhóm II).
- Cho từng mẫu thử ở nhóm II tác dụng với dung dịch bromine:
+ Dung dịch bromine nhạt dần đến mất màu → propanal.
Phương trình hoá học:
CH3 – CH2 – CHO + Br2 + H2O → CH3 – CH2 – COOH + 2HBr.
+ Không hiện tượng → acetone.
Cho các phát biểu sau:
a) Hợp chất C6H5CH2OH không thuộc loại hợp chất phenol
b) Ancol etylic có thể hòa tan tốt trong nước
c) Ancol và phenol đều có khả năng tác dụng với Na sinh ra H2
d) Phenol có tính axit yếu nên làm quỳ tím chuyển sang màu hồng nhạt
e) Phenol tan trong dung dịch NaOH là do đã phản ứng với NaOH tạo thành muối tan
Số phát biểu không đúng là:
A. 2
B. 3
C. 4
D. 1
Đáp án D
a) Đ. C6H5CH2OH là ancol, không phải phenol
b) Đ. Do C2H5OH tạo được liên kết hidro với H2O
c) Đ. Do ancol và phenol đều chứa nguyên tử H linh động
d) S. Phenol không làm đổi màu quỳ tím do nó có tính axit rất yếu
e) Đ. Vì C6H5OH + NaOH → C6H5ONa + H2O (C6H5ONa là muối tan)
Từ thí nghiệm 1, hãy cho biết các chất lỏng có hoà tan trong nhau không.
Thí nghiệm 1: Tạo hỗn hợp đồng nhất và không đồng nhất
Bước 1: Lấy 2 ống nghiệm, thêm nước cất đến 1/3 ống.
Bước 2: Lần lượt cho một thìa ethanol vào ống nghiệm thứ nhất và một thìa dầu ăn vào ống nghiệm thứ hai.
Bước 3: Lắc đều hai ống nghiệm, để yên và quan sát hiện tượng.
Ống nghiệm them một thìa ethanol: có hòa tan thành hỗn hợp đồng nhất
Ống nghiệm them một thìa dầu ăn: không hòa tan, tách lớp
Ethyl iodide có khối lượng riêng là 1,94 g mL-1 và có nhiệt độ sôi là 72 °C. Ethanol có khối lượng riêng là 0,789 g mL-1 và có nhiệt độ sôi là 78 °C. Ethanol tan trong nước còn ethyl iodide kém tan trong nước nhưng tan được trong ethanol. Ethyl iodide thường được điều chế từ ethanol và sản phẩm thu được thường bị lẫn ethanol. Đề xuất phương pháp tinh chế ethyl iodide từ hỗn hợp của chất này với ethanol.
- Ta có thể sử dụng các phương pháp chiết lỏng – lỏng ethyl iodide để tách ethyl iodide ra khỏi hỗn hợp. Vì các lý do sau:
+ Ethyl iodide kém tan trong nước, còn ethanol tan tốt trong nước.
+ Khối lượng riêng của ethyl iodide lớn hơn nhiều so với khối lượng riêng của ethanol.
- Phương pháp chiết lỏng – lỏng ethyl iodide được thực hiện như sau:
Ethyl iodide kém tan trong nước, còn ethanol tan tốt trong nước nên ta chọn nước là dung môi. Cho dung dịch gồm ethyl iodide, ethanol vào phễu chiết, thêm nước vào. Lắc đều phễu chiết rồi để yên, hỗn hợp sẽ tách thành hai lớp: một lớp là hỗn hợp ethanol và nước nhẹ hơn ở trên, một lớp là ethyl iodide nặng hơn ở dưới. Mở khoá phễu chiết ta thu được ethyl iodide. Làm bay hơi dung môi từ dịch chiết để được ethyl iodide cần phân tách.
Từ thí nghiệm 1, em hãy cho biết dầu ăn và ethanol, chất nào tan hoàn toàn trong nước. Hỗn hợp thu được là đồng nhất hay không đồng nhất?
Thí nghiệm 1: Tạo hỗn hợp đồng nhất và không đồng nhất
- Bước 1: Lấy 2 ống nghiệm, thêm nước cất đến 1/3 ống.
- Bước 2: Lần lượt cho một thìa ethanol vào ống nghiệm thứ nhất và một thìa dầu ăn vào ống nghiệm thứ hai.
- Bước 3: Lắc đều hai ống nghiệm, để yên và quan sát hiện tượng.
Cho dầu ăn vào nước thu được hỗn hợp không đồng nhất
Cho etanol vào nước thu được hỗn hợp đồng nhất
Ethanol là chất tan hoàn toàn trong nước. Hỗn hợp thu được là hỗn hợp đồng nhất.
Dưới đây là hình ảnh các ống nghiệm chứa hexane và hex-1-ene sau khi được thêm nước bromine rồi lắc đều.
a) Trong mỗi ống nghiệm, nước nằm trong lớp chất lỏng ở phía trên hay phía dưới?
b) Ống nghiệm nào chứa hexane, ống nghiệm nào chứa hex-1-ene? Giải thích sự khác nhau về màu sắc giữa hai ống nghiệm.
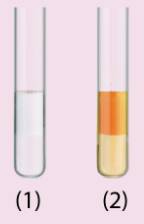
Tham khảo:
a) Trong ống nghiệm, nước nằm trong lớp chất lỏng ở phía dưới.
b) Ống nghiệm (2) chứa hexane, ống nghiệm (1) chứa hex-1-ene. Ở nhiệt độ thường hexane kém hoạt động nên không phản ứng làm mất màu dung dịch bromie, hex-1-ene là alkene làm mất màu vàng của nước bromine.
Ghi Đ (đúng) hoặc S (sai) vào ô vuông cạnh các câu sau:
a) Hợp chất C6H5- CH2-OH không thuộc loại hợp chất phenol mà thuộc ancol thơm.
b) Ancol etylic có thể hòa tan tốt phenol, nước.
c) Ancol và phenol đều có thể tác dụng với natri sinh ra khí hidro.
d) Phenol có tính axit yếu nhưng dung dịch phenol trong nước không làm đổi màu quỳ tím.
e) Phenol tan trong dung dịch NaOH là do đã phản ứng với NaOH tạo thành muối tan.
g) Phenol tan trong dung dịch NaOH chỉ là sự hòa tan bình thường .
h) Dung dịch phenol trong nước làm quỳ tím hóa đỏ.
Bài 3 : Cho magie dư vào 16,6 g hỗn hợp ethanol và acetic acid thấy thoát ra 2,24 lít khi đkc .
a ) Tính khối lượng mỗi chất trong hỗn hợp ban đầu ?
b) Tính % theo khối lượng mỗi chất trong hỗn hợp ?
c) Để có lượng rượu trên cần lên men bao nhiêu gam dung dịch glucose 15%?
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(Mg+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Mg+H_2\)
0,2 0,1 ( mol )
\(\left\{{}\begin{matrix}m_{CH_3COOH}=0,2.60=12\left(g\right)\\m_{C_2H_5OH}=16,6-12=4,6\left(g\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{CH_3COOH}=\dfrac{12}{16,6}.100=72,29\%\\\%m_{C_2H_5OH}=100-72,29=27,71\%\end{matrix}\right.\)
\(n_{C_2H_5OH}=\dfrac{4,6}{46}=0,1\left(mol\right)\)
\(C_6H_{12}O_6\xrightarrow[men.rượu]{30^o-35^o}2C_2H_5OH+2CO_2\)
0,05 0,1 ( mol )
\(m_{dd_{C_6H_{12}O_6}}=\dfrac{0,05.180.100}{15}=60\left(g\right)\)