Viết biểu thức hằng số cân bằng KCcho phản ứng (*), (**) dưới đây.
H2 (g) + I2 (g) ⇌ 2HI(g) (*)
1/2 H2(g) + 1/2 I2 (g) ⇌ HI (g) (**)
Theo em, giá trị hai hằng số cân bằng này có bằng nhau không?
1, cho biết phản ứng sau:N2(g) + H2O(g)<===>CO2 . Nồng độ các chất lúc cân bằng ở nhiệt độ 430 độ c là [h2] =[I2] = 0,107M ; [HI]= 0,786M. tính hằng số cân bằng Kc tại 430 độ c
2, Iodine bị phân hủy bởi nhiệt theo phản ứng sau :I2(g)<==>2I(g).Ở 727 độ c hằng số cân bằng của phản ứng KC = 3,80×10-⁵ .Cho 0,05 mol I2 vào một bình kín dung tích 2,5 lít ở 727°c tính nồng độ của i2 và I ở trạng thái cân bằng
Cho các cân bằng hóa học sau
(1) H 2 + I 2 ⇔ 2 H I
( 2 ) 1 2 H 2 + 1 2 I 2 ⇔ H I
(3) 2 H I ⇔ H 2 + I 2
Với lần lượt các giá trị hằng số cân bằng K c b 1 , K c b 2 , K c b 2 . Nhận định nào sau đây đúng
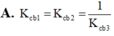
![]()
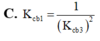
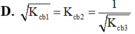
Chọn đáp án D
Khi viết công thức tính các hằng số cân bằng của các phản ứng thuận nghịch trên ta thấy
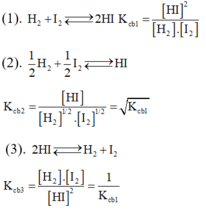
Cân bằng phản ứng H 2 + I 2 ⇄ 2 H I Δ H < 0 được thiết lập ở t o C khi nồng độ các chất ở trạng thái cân bằng là H 2 = 0 , 8 m o l / l ; I 2 = 0 , 6 m o l / l ; [ H I ] = 0 , 96 m o l / l . Hằng số K có giá trị là
A. 1 , 92 . 10 - 2
B. 1 , 82 . 10 - 2
C. 1,92
D. 1,82
Iodine bị phân hủy bởi nhiệt theo phản ứng sau: I2 (g) 2I (g) Ở 727oC hằng số cân bằng của phản ứng KC = 3,80.10-5 . Cho 0,05 mol I2 vào một bình kín dung tích 2,5 lít ở o 727 C. Tính nồng độ của I2 và I ở trạng thái cân bằng
CM(I2)=0.02M
gọi nồng độ iot chuyển hóa là x
I2(k) <=> 2I(k)
pư: x 2x
cb: 0.02-x 2x
Ta có: (2x)^2/ 0.02-x = 3,80*10^-5
=> x=4,311*10^-4
=> [I2] = 0.02-4,311*10^-4=0,019M
=>[I] = 9,5*10^-3(M)
2. Ở nhiệt độ 1000 oK có 28% HI bị phân huỷ theo phản ứng sau:
2HI(k) ⇆ H2(k) + I2(k)
a. Tính hằng số cân bằng K và ΔGo của phản ứng ở 1000 oK?
b. Trong bình V=8.2 dm3 chứa khí H2 và hơi I2 với áp suất riêng phần ![]() =
=![]() =0,5 atm ở 1000 oK. Thêm vào bình 1 mol khí HI. Tính xem có bao nhiêu phần trăm HI bị phân huỷ ở điều kiện này ?
=0,5 atm ở 1000 oK. Thêm vào bình 1 mol khí HI. Tính xem có bao nhiêu phần trăm HI bị phân huỷ ở điều kiện này ?
Khi đun nóng HI trong một bình kín xảy ra phản ứng 2HI khí H2 khí + I2 khí. Ở to C hằng số cân bằng K của phản ứng bằng 11/64. Tỷ lệ %HI bị phân hủy là
A. 20%
B. 25%
C. 15%
D. 30%
Cho phản ứng: \(CO_{\left(g\right)}+Cl_{2\left(g\right)}⇌COCl_{2\left(g\right)}\) được thực hiện trong bình kín ở nhiệt độ không đổi, nồng độ ban đầu của CO và Cl2 bằng nhau và bằng 0,4M
a) Tính hằng số cân bằng của phản ứng biết rằng khi hệ đạt trạng thái cân bằng thì chỉ còn 50% lượng CO ban đầu
b) Sau khi cân bằng được thiết lập ta thêm 0,1 mol CO vào 1 lít hỗn hợp. Tính nồng độ các chất lúc cân bằng mới được thiết lập
Cho các cân bằng sau :
(1) H2 (k) + I2 (k) ⇄ 2HI (k).
(2) 1/2H2 (k) + 1/2I2 (k) ⇄ HI (k).
(3) HI (k) ⇄ 1/2H2 (k) + 1/2I2 (k)
(4) 2HI (k) ⇄ H2 (k) + I2 (k)
(5) H2 (k) + I2 (r) ⇄ 2HI (k).
Ở nhiệt độ xác định, nếu KC của cân bằng (1) bằng 64 thì KC bằng 0,125 là của cân bằng
A. (5)
B. (2)
C. (3)
D. (4)
Cho các cân bằng sau:
(1): H2 (k) + I2 (k) → 2 HI (k) (2): ½ H2 (k) + ½ I2 (k) → HI (k)
(3): HI(k) ó ½H2 (k) + ½I2 (k) (4): 2HI (k) ó H2 (k) + I2 (k)
(5): H2 (k) + I2 (r) → 2 HI (k).
Ở nhiệt độ xác định, nếu KC của cân bằng (1) bằng 64 thì KC bằng 0,125 là của cân bằng:
A. (3)
B. (2)
C. (5)
D. (4)
Chỉ cần áp dụng công thức tính kc, ta dễ dàng suy ra:
K1 = [HI]^2 / [H2][I2]K3 = ([H2][I2])^1/2/[HI] = (1/K1)^1/2 = 1/8 = 0.125
=> Đáp án A