Ở 20 độ C, hòa tan m g Cu(NO3)2.6H2O vào 100g dd Cu(NO3)2 30% thu đc dung dịch bão hòa Cu(NO3)2. Tính m. Biết đọ tan của Cu(NO3)2 tại 20 độ C là 125g
Mong mn giúp :((

Những câu hỏi liên quan
Ở 20 độ C độ tan trong nc của Cu (NO3)2.6H2O là 125g. Tính khối lượng Cu (NO3)2.6H2O cần lấy để pha chế 450g dung dịch bão hòa và tính nồng độ % Cu (NO3)2 bão hòa ở nhiệt độ đó
Cứ 125g Cu(NO3)2.6H2O --> 100g nước --> 225g dung dịch
250g <-- 200g <-- 450g
=> \(m_{Cu\left(NO_3\right)_2}\) = \(\dfrac{250.188}{296}\) = 158,784(g)
=> C% = \(\dfrac{158,784}{450}.100\%\) = 35,285%
Đúng 0
Bình luận (3)
Độ tan của \(Cu\left(NO_3\right)_2.6H_2O\) là 125 g .Nghĩa là 100 g H20 hoà tan 125g muối do đó khối lượng dung dịch là 225 g
125g muối trong 225 g dung dịch
x ( g).........................450 g dung dịch
-> x = 250 g
Cứ 296 muối ngậm nước có 188 g Cu(NO3)2
Vậy 250 g...................................... y g
\(C_{\%}=\dfrac{157,78}{450}.100=35,29\%\)
Đúng 1
Bình luận (0)
Ơ 20 độ C thì cứ 125g chất tan thì có 100g nước và 225g d d
-----> Có 450g d d thì có 250g chất tan và 200g nước
Vậy là ta đã tính đc chất tan là 250g --->
C% chất tan = (250: 450).100=55,5%
Đúng 0
Bình luận (4)
Xem thêm câu trả lời
Hòa tan hoàn toàn m gam Cu vào 400 gam dung dịch Fe(NO3)3 12,1% thu được dung dịch A có nồng độ Cu(NO3)2 là 3,71%. Nồng độ % Fe(NO3)3 trong dung dịch A là
A. 2,39%.
B. 3,12%.
C. 4,20%.
D. 5,64%.
Chọn đáp án A
mFe(NO3)3 bđ = 400.12,1/100 = 48,4 (g)
Gọi số mol của Cu là x (mol)
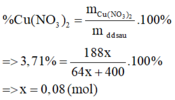
Cu + 2Fe3+ → 2Fe2+ + Cu2+
0,08 → 0,16 (mol)
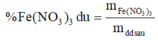
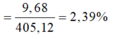
=> mFe(NO3)3 dư = 48,4 – 0,16.242 = 9,68 (g)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn m gam Cu vào 400 gam dung dịch Fe(NO3)3 12,1% thu được dung dịch A có nồng độ Cu(NO3)2 là 3,71%. Nồng độ % Fe(NO3)3 trong dung dịch A là
A. 2,39%.
B. 3,12%.
C. 4,20%.
D. 5,64%.
Chọn đáp án A
mFe(NO3)3 bđ = 400.12,1/100 = 48,4 (g)
Gọi số mol của Cu là x (mol)
mdd sau = mCu + mddFe(NO3)2 => mdd sau =( 64x + 400) g
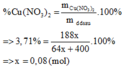
Cu + 2Fe3+ → 2Fe2+ + Cu2+
0,08 → 0,16 (mol)
=> mFe(NO3)3 dư = 48,4 – 0,16.242 = 9,68 (g)
![]()
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn m gam Cu vào 400 gam dung dịch Fe(NO3)3 12,1% thu được dung dịch A có nồng độ Cu(NO3)2 là 3,71%. Nồng độ % Fe(NO3)3 trong dung dịch A là A. 2,39%. B. 3,12%. C. 4,20%. D. 5,64%.
Đọc tiếp
Hòa tan hoàn toàn m gam Cu vào 400 gam dung dịch Fe(NO3)3 12,1% thu được dung dịch A có nồng độ Cu(NO3)2 là 3,71%. Nồng độ % Fe(NO3)3 trong dung dịch A là
A. 2,39%.
B. 3,12%.
C. 4,20%.
D. 5,64%.
Hòa tan hoàn toàn 1,28 g Cu vào 12,6 gam dd NO3 60% thu được dung dịch X. Cho X tác dụng hoàn toàn với 105ml dung dịch KOH 1M, sau đó lọc bỏ kết tủa thu được dung dịch Y. Cô cạn Y được chất rắn Z. Nung Z đến khối lượng không đổi, thu được 8,78 gam chất rắn. Nồng độ phần trăm của Cu(NO3)2 trong X là: A. 28,66% B. 29,89%. C. 30,08% D. 27,09%
Đọc tiếp
Hòa tan hoàn toàn 1,28 g Cu vào 12,6 gam dd NO3 60% thu được dung dịch X. Cho X tác dụng hoàn toàn với 105ml dung dịch KOH 1M, sau đó lọc bỏ kết tủa thu được dung dịch Y. Cô cạn Y được chất rắn Z. Nung Z đến khối lượng không đổi, thu được 8,78 gam chất rắn. Nồng độ phần trăm của Cu(NO3)2 trong X là:
A. 28,66%
B. 29,89%.
C. 30,08%
D. 27,09%
Đáp án A
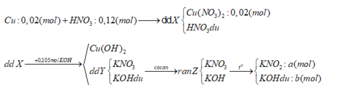
∑nKOH = a + b = 0,105 (1)
∑ mrắn = 85a + 56b = 8,78 (2)
Từ (1) và (2) => a = 0,1 (mol) ; b = 0,005 (mol)
nKNO3 tạo ra từ Cu(NO3)2 = 0,04 (mol)
=> nKNO3 tạo ra từ HNO3 dư = 0,1 – 0,04 = 0,06 (mo)
=> nHNO3 dư = 0,12- 0,06 = 0,06 (mol)
=> nHNO3 bị khử = 0,06 – 0,02.2 = 0,02 (mol)
Với ne( Cu nhường) = 2.nCu = 0,04 (mol) => Trung bình mỗi N+5 nhận 0,04/0,02 = 2e
=> Tạo NO2 (1e) và NO ( 3e)
=> nNO = nNO2 = 0,02/ 2= 0,01(mol)
Vậy mdd X = mCu + mdd HNO3 – m khí = 1,28 + 12,6 – 0,01.30 – 0,01.46 = 13,12 (g)
=> C% Cu(NO3)2 = [( 0,02.188) : 13,12].100% = 28,66%
Đúng 0
Bình luận (0)
ở 20độ C độ tan tronh nc của Cu(NO3)2 * 6H2O là 125g . tính khối lượng của Cu(NO3)2 * 6H2O cần lấy để pha chế 450g đ bão hòa tính khối lượng Cu(NO3)2 VÀ C % của dd đó ở 20 độ C
Ở 20oC
100 g nước ht 125g muối tạo thành 225 g dung dịch
Vậy xg nuoc ht y g muối tạo 450 g dd
--->y=\(\frac{450.125}{225}=250\left(g\right)\)
Cứ 296g Cu(NO3)2.6H2O có 188 g Cu(NO3)2
Vậy 250g .............................a g ................
-->m \(_{Cu\left(NO3\right)2}=\frac{250.188}{296}=158,78\left(g\right)\)
C%=\(\frac{158,78}{450}.100\%=35,28\%\)
hòa tan hoàn toàn 3,37g hỗn hợp Cu,Fe,Mg,Al trong dung dịch HNO3 dư thu được m gam hỗn hợp các muối sau Cu(NO3)2,Fe(NO3)3,Mg(NO3)2,Al(NO3)3 và 616 ml khí N2O là sản phẩm khử duy nhất của N(+5).tìm giá trị m
nN2O = \(\dfrac{0,616}{22,4}\)= 0,0275 mol
2N+5 + 8e --> N2+1
0,22<------- 0,0275
nNO3- tạo muối = ne trao đổi = 0,22 mol
=> mNO3- tạo muối = 0,22.62 = 13,64 gam
mMuối = mKL + mNO3- = 3,37 + 13,64 = 17,01 gam
Đúng 2
Bình luận (0)
Câu 1: Hòa tan 20g K2SO4 vào 150ml H2O đem điện phân cực trơ khi nồng độ dd là 14,925% thì dừng. V khí thoát ra ở anot trong điềi kiện 20C 1atm là bao nhiu?
Câu2: Đpdd chứa NaCl và Cu(NO3)2 đến khi hết màu xanh thì thu đc 6,72 lit hỗn hợp khí A có tỉ khối so với H2 là 29. tính m của Cu(NO3)2
1)khối lượng dd sau điện phân \(=\frac{20\cdot100}{14,925}=134\)
=>khối lượng dd giảm sau điện phân= tổng khối lượng khí thoát ra =20+150-134=36
2H−−−−−>H2+2e
____________a___2a
2O−−+4e−−>O2
_________4b_____b
Ta có các hệ phương trình
\(\begin{cases}2a+32b=36\\2a-4b=0\end{cases}\)\(\Rightarrow\)\(\begin{cases}a=2\\b=1\end{cases}\)
sử dụng CT
\(n=\frac{PV}{RT}\Rightarrow V=\frac{4688}{65}\left(l\right)\)
Đúng 0
Bình luận (1)
2)
BTklg=>mO2=mhht-mhhs
ppe:6*nKClO3+5*nKMnO4-4nO2=nCl2*2
BTng tử ng tố =>nAgCl=nCl2*2
=>mAg=mh***AgCl
ppe:nFe*3=nAg+nCl2*2
=>m=nM
Đúng 0
Bình luận (0)
Hòa tan 5,4 gam bột Al vào 150 ml dung dịch X chứa Fe(NO3)3 1M và Cu(NO3)2 1M. Kết thúc phản ứng thu được m gam rắn. Giá trị của m là
A. 13,80
B. 15,20.
C. 10,95.
D. 13,20.
















