Cho 22,4g tác dụng với 3.36 lít oxi (đktc). a) Xác định chất dư và dư bao nhiêu gam. b) Tính chất rắn sau phản ứng

Những câu hỏi liên quan
Cho 1.48 gam hh fe và Cu tác dụng với H2SO4 dư sau khi phản ứng xong thu được chất rắn A và 3.36 lít H2 đktc
A. Viết phản ứng
B. Tính khối lượng từng Kim loại ban đầu
Xem chi tiết
\(Fe + H_2SO_4 \to FeSO_4 + H_2\)
Chất rắn A : Cu
Theo PTHH :
\(n_{Fe} = n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)\\ \Rightarrow m_{Fe} = 0,15.56 = 8,4(gam)\)
Suy ra : \(m_{Cu} = 1,48 - 8,4 = -6,92 < 0\)→ Sai đề
Đúng 1
Bình luận (0)
Cho 22,4g Fe tác dụng với dung dịch loãng có chứa 24,5 g H2SO4 sau phản ứng hãy cho biết: a, Chất nào dư sau phản ứng và dư bao nhiêu gam? b, Tính thể tích H2 thu được ở đktc.
PTHH: \(Fe+H_2SO_{4\left(l\right)}\rightarrow FeSO_4+H_2\uparrow\)
Ta có: \(\left\{{}\begin{matrix}n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\\n_{H_2SO_4}=\dfrac{24,5}{98}=0,25\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Sắt còn dư, Axit p/ứ hết
\(\Rightarrow\left\{{}\begin{matrix}n_{H_2}=0,25\left(mol\right)\\n_{Fe\left(dư\right)}=0,15\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=0,25\cdot22,4=5,6\left(l\right)\\m_{Fe\left(dư\right)}=0,15\cdot56=8,4\left(g\right)\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Cho 22,4g sắt tác dụng với dung dịch loãng chứa 24,5 axit sufic a: chất nào còn dư sau phản ứng và dư bao nhiêu gam? B: tính thể tích khí hirod thu đc ở Đktc ?
a, \(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{24,5}{98}=0,25\left(mol\right)\)
PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Xét tỉ lệ: \(\dfrac{0,4}{1}>\dfrac{0,25}{1}\), ta được Fe dư.
Theo PT: \(n_{Fe\left(pư\right)}=n_{H_2SO_4}=0,25\left(mol\right)\Rightarrow n_{Fe\left(dư\right)}=0,4-0,25=0,15\left(mol\right)\)
\(\Rightarrow m_{Fe\left(dư\right)}=0,15.56=8,4\left(g\right)\)
b, \(n_{H_2}=n_{H_2SO_4}=0,25\left(mol\right)\Rightarrow V_{H_2}=0,25.22,4=5,6\left(l\right)\)
Đúng 4
Bình luận (1)
Cho 22,4g sắt tác dụng với dung dịch loãng có chứa 24,5g axit sunfuric.
a) Chất nào còn dư sau phản ứng và dư bao nhiêu gam?
b) Tính thể tích khí hiđro thu được ở đktc.
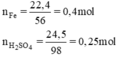
Phương trình hóa học của phản ứng:

So sánh tỉ lệ 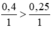 ⇒ Fe dư
⇒ Fe dư
Theo PT nFe (pư) = nH2SO4 = 0,25 mol ⇒ nFe dư = 0,4 – 0,25 = 0,15 mol
mFe dư = 0,15. 56 = 8,4g.
Do khối lượng Fe dư nên tính thể tích khí H2 theo số mol H2SO4.
nH2 = nH2SO4 = 0,25 mol
Vkhí = 0,25 . 22,4 = 5,6l.
Đúng 0
Bình luận (0)
Cho 22,4g sắt tác dụng với dung dịch axit sunfuric loãng có chứa 24,5g H₂SO₄ a. Chất nào còn dư sau phản ứng và dư bao nhiêu gam? b. Tính thể tích khí hiđro thu được ở đktc
a) nFe=0,4(mol); nH2SO4=0,5(mol)
PTHH: Fe + H2SO4 -> FeSO4 + H2
Ta có: 0,4/1 < 0,5/1
=> Fe hết, H2SO4 dư. tính theo nFe.
=> nH2= nH2SO4(p.ứ)=nFe=0,4(mol)
=>nH2SO4(dư)=0,5-0,4=0,1(mol)
=>H2SO4(dư)=0,1.98=9,8(g)
b) V(H2,dktc)=0,4.22,4=8,96(l)
Đúng 3
Bình luận (2)
Cho 4,8 gam magie tác dụng với 5,6 lít khí oxi ( ở đktc ) sau phản ứng thu được magie oxit. Hỏi sau phản ứng chất nào dư và dư bao nhiêu mol ?
PT: \(2Mg+O_2\underrightarrow{t^o}2MgO\)
Ta có: \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
\(n_{O_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{2}< \dfrac{0,25}{1}\), ta được O2 dư.
Theo PT: \(n_{O_2\left(pư\right)}=\dfrac{1}{2}n_{Mg}=0,1\left(mol\right)\)
\(\Rightarrow n_{O_2\left(dư\right)}=0,25-0,1=0,15\left(mol\right)\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
PTHH: \(2Mg+O_2\underrightarrow{t^o}2MgO\)
Ta có: \(\left\{{}\begin{matrix}n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\n_{O_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,2}{2}< \dfrac{0,25}{1}\) \(\Rightarrow\) Magie p/ứ hết, Oxi còn dư
\(\Rightarrow n_{O_2\left(dư\right)}=0,25-0,1=0,15\left(mol\right)\)
Đúng 0
Bình luận (0)
Cho 10,8g nhôm tác dụng với 13,44lit khí oxi (đktc) a. Viết PTHH b. Chất nào còn dư sau phản ứng và dư bao nhiêu gam (lít)? c. Khối lượng nhôm oxit tạo thành là bao nhiêu?
\(a,n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\\ n_{O_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: 4Al + 3O2 --to--> 2Al2O3
b, LTL: \(\dfrac{0,4}{4}>\dfrac{0,6}{3}\) => O2 dư
Theo pthh: \(\left\{{}\begin{matrix}n_{O_2\left(pư\right)}=\dfrac{3}{4}n_{Al}=\dfrac{3}{4}.0,4=0,3\left(mol\right)\\n_{Al_2O_3}=\dfrac{1}{2}n_{Al}=\dfrac{1}{2}.0,4=0,2\left(mol\right)\end{matrix}\right.\)
=> VO2 (dư) = (0,6 - 0,3).22,4 = 6,72 (l)
c, mAl2O3 = 0,2.102 = 20,4 (g)
Đúng 2
Bình luận (3)
\(n_{Al}=\dfrac{10,8}{17}=0,4\left(mol\right)\\ n_{O_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\\ pthh:4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(LTL:\dfrac{0,4}{4}< \dfrac{0,6}{3}\)
=> O2 dư P hết
\(n_{Al_2O_3}=\dfrac{1}{2}n_{Al}=0,2\left(mol\right)\\ m_{Al_2O_3}=0,2.102=20,4g\)
Đúng 1
Bình luận (0)
\(n_{Al}=\dfrac{10,8}{27}=0,4mol\)
\(n_{O_2}=\dfrac{13,44}{22,4}=0,6mol\)
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
Xét: \(\dfrac{0,4}{4}\) < \(\dfrac{0,6}{3}\) ( mol )
0,4 0,3 0,2 ( mol )
Chất dư là O2
\(m_{O_2\left(dư\right)}=\left(0,6-0,3\right).32=9,6g\)
\(m_{Al_2O_3}=0,2.102=20,4g\)
Đúng 1
Bình luận (3)
Cho 2,4g magie tác dụng hết với axit clohidric thu được V lít khí h2 ở đktc a)tính V b)đem thể tích khí hiđrô ở trên tác dụng hết với 0,5 mol oxi. Sau phản ứng chất nào dư và dư bao nhiêu gam?
\(n_{Mg}=\dfrac{2.4}{24}=0.1\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(0.1....................................0.1\)
\(V_{H_2}=0.1\cdot22.4=2.24\left(l\right)\)
\(2H_2+O_2\underrightarrow{^{t^0}}2H_2O\)
\(0.1.....0.05\)
\(m_{O_2\left(dư\right)}=\left(0.5-0.05\right)\cdot32=14.4\left(g\right)\)
Đúng 1
Bình luận (0)
Đem oxi hóa 11,2 gam Fe trong 11,2 lít oxi (đktc) thu được Fe3O4. Tính khối lượng chất dư và lượng Fe3O4 thu được. b) Cho 0,3.1024 nguyên tử Mg tác dụng với 25,55 gam HCl. Sau phản ứng thu được MgCl2 và bao nhiêu lít H2 (đktc).























