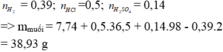người ta lấy a (g) hh gồm Mg và MgO cho vào 400 ml dd HCl x M (vừa đủ ) được 2,24 (l) khí H2 ở DKTC và ddB đem cô cạn dd B được 28,5 g muối khan .tìm các giá trị của a và x

Những câu hỏi liên quan
Người ta lấy x (g) hh gồm Mg và MgO cho vào 400 ml dd HCl xM (vừa đủ) được 2,24l khí H2 ở đktc và dd B. Đem cô cạn dd B dược 28,5g muối khan . Tình giá trị của a và x
Đề là a g hh nha bạn
Mg+2HCl--->MgCl2+H2
MgO+2HCl---->MgCl2+H2O
Ta có
n H2=2,24/22,4=0,1(mol)
Theo pthh1
n Mg=n H2=0,1(mol)
m Mg=0,1.24=2,4(g)
n MgCl2 ở pt1 =n H2 =0,1(mol)
m MgCl2=0,1.95=9,5(g)
m muối ở pt2 =28,5-9,5=19(g)
n MgCl2=19.95=0,2(mol)
Theo pthh2
n MgO=n MgCl2=0,2(mol0
m MgO=0,2.40=8(g)
a=m hh=8+2,4=10,4(g)
Theo pthh1
n HCl=2n H2=0,2(mol)
Theo pthh2
n HCl=2n MgCl2=0,4(mol)
\(\sum nHCl=0,2+0,4=0,6\left(mol\right)\)
x=0,6/0,4=1,5(M)
Ngắn gọn hơn bài Dương nhé:
Mg+2HCl\(\rightarrow\)MgCl2+H2 (1)
MgO+2HCl\(\rightarrow\)MgCl2+H2O (2)
nH2=\(\frac{2,24}{22,4}\)=0,1 mol
\(\rightarrow\) nMg=0,1 mol, nMgCl2 (1)=0,1 mol
\(\rightarrow\)mMgCl2(1)=0,1.95=9,5g
\(\rightarrow\) mMgCl2(2)=28,5-9,5=19g
\(\rightarrow\) nMgCl2(2)=nMgO=19:95=0,2 mol
Ta có:
x gam hh tpu= mMg+mMgO=0,1.24+0,2.95=21,4g
CM HCl=(0,1.2+0,2.2)/0,4=1,5M
a(g) là klg hh
PTHH1:Mg+2HCl->MgCl2+H2
mol:.....0,1........0,2.......0,1.....0,1
PTHH2:MgO+2HCl->MgCl2+H2O
mol:0,2...........0,4.............0,2.....0,2
mH2=2,24:22,4=0,1(mol)
mMgCl2(pt1)=0,1.95=9,5(g)
mMgCl2(pt2)=28,5-9,5=19(g)
nMgCl(pt2)=19:95=0,2(mol)
a=0,1.24+0,2.40=10,4(g)
CM\(_{HCl}\)=\(\frac{0,1.2+0,2.2}{0,4}\)=1,5M
Cho 21g hh A gồm Fe,Mg,Zn phản ứng vừa đủ với V ml dd gồm HCL 2M và H2SO4 1M thu đc 8.96 lít Khí H2 ở đktc và ddC. Cô cạn dd C đc m g muối khan. Giá trị của V và m =? Giúp em với, em đang gấp lắm
Cho 14,3 g hỗn hợp A gồm Al Zn Mg tác dụng vừa đủ với V(ml) dd HCl 2M, sau phản ứng người ta thu được dd B và 11,2L khí H2 ở (đktc)
a) tính V
b) Cô cạn dung dịch B Hỏi thu được bao nhiêu gam hỗn hợp muối khan
c) Tính thành phần % của hỗn hợp A theo khối lượng biết tỉ lệ mol của Mg và Al 1:1
d) Cho dung dịch xút (dư) vào dd B ta được kết tủa C. Lọc kết tủa C (đem nung đến khối lượng không đổi ta được m(g) chất rắn D tính m
Giúp mình vớiii
Đọc tiếp
Cho 14,3 g hỗn hợp A gồm Al Zn Mg tác dụng vừa đủ với V(ml) dd HCl 2M, sau phản ứng người ta thu được dd B và 11,2L khí H2 ở (đktc) a) tính V b) Cô cạn dung dịch B Hỏi thu được bao nhiêu gam hỗn hợp muối khan c) Tính thành phần % của hỗn hợp A theo khối lượng biết tỉ lệ mol của Mg và Al 1:1 d) Cho dung dịch xút (dư) vào dd B ta được kết tủa C. Lọc kết tủa C (đem nung đến khối lượng không đổi ta được m(g) chất rắn D tính m Giúp mình vớiii
: Cho m (g) Mg, Al vào 250 ml dd X chứa hỗn hợp HCl 1M và H2SO4 0,5M thu được 5,32 lít khí H2 ( ở đktc) và dd Y ( Coi thể tích dd không thay đổi).
a. Trong dd Y axit dư hay hết?
b. Tính giá trị m?
c. Cô cạn dd Y thu được a(g) muối. Tính a?
Hòa tan 13,9 g hh Al và Fe vào dd HCl dư thu được V lít khí H2 (đktc) và dd A. Cô cạn dd A thu được 38 g hh muối khan
a. Tính thành phần % khối lượng hh ban đầu và giá trị V
b. Tính khối lượng dd HCl 25% đã lấy biết dùng dư 20% so với lượng phản ứng
Xem chi tiết
a)Gọi x,y lần lượt là số mol của Al, Fe trong hỗn hợp ban đầu (x,y>0)
Sau phản ứng hỗn hợp muối khan gồm: \(\left\{{}\begin{matrix}AlCl_3:x\left(mol\right)\\FeCl_2:y\left(mol\right)\end{matrix}\right.\)
Ta có hệ phương trình: \(\left\{{}\begin{matrix}27x+56y=13,9\\133,5x+127y=38\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x\approx0,0896\\y\approx0,205\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,0896\cdot27\cdot100\%}{13,9}\approx17,4\%\\\%m_{Fe}=\dfrac{0,205\cdot56\cdot100\%}{13,9}\approx82,6\%\end{matrix}\right.\)
Theo Bảo toàn nguyên tố Cl, H ta có:\(n_{H_2}=\dfrac{n_{HCl}}{2}=\dfrac{3n_{AlCl_3}+2n_{FeCl_2}}{2}\\ =\dfrac{3\cdot0,0896+2\cdot0,205}{2}=0,3394mol\\ \Rightarrow V_{H_2}=0,3394\cdot22,4\approx7,6l\)
Đúng 2
Bình luận (0)
Hòa tan hết m gam hỗn hợp gồm Mg, Al, Al2O3 và MgO cần 800ml dd hỗn hợp gồm HCl 0,5M và H2SO4 0,75M. Sau phản ứng thu được dd X và 4,48l khí H2 (đktc) . Cô cạn dd thu được X thu được 88,7 g muối khan. Tính m.
$n_{HCl} = 0,8.0,5 = 0,4(mol) ; n_{H_2SO_4} = 0,6(mol) ;n_{H_2} = 0,2(mol)$
$n_{H(trong\ axit)} = 0,4 + 0,6.2 = 1,6(mol)$
Bảo toàn H : $n_{H_2O} = \dfrac{n_{H(trong\ axit)} - 2n_{H_2} }{2} = 0,6(mol)$
Bảo toàn khối lượng :
$m = 88,7 + 0,6.18 + 0,2.2 - 0,4.36,5 - 0,6.98 = 26,5(gam)$
Đúng 2
Bình luận (0)
Hoà tan hết 7,74 gam hh bột Mg, Al bằng 500 ml dd hh HCl 1M và H2SO4 0,28M thu được dd X và 8,736 lít khí H2 (ở đktc). Cô cạn dd X thu được lượng muối khan là A. 38,93 gam. B. 103,85 gam. C. 25,95 gam. D. 77,86 gam.
Đọc tiếp
Hoà tan hết 7,74 gam hh bột Mg, Al bằng 500 ml dd hh HCl 1M và H2SO4 0,28M thu được dd X và 8,736 lít khí H2 (ở đktc). Cô cạn dd X thu được lượng muối khan là
A. 38,93 gam.
B. 103,85 gam.
C. 25,95 gam.
D. 77,86 gam.
hoà tan 8,8 gam hh Mg và MgO vào trong 200 gam HCL Cô cạn thu được 28,5 gam muối khan
a. tính khối lượng và % khối lượng của mỗi kim loại
b. tính C% dd HCL
Xem chi tiết
a)Gọi : \(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{MgO}=b\left(mol\right)\end{matrix}\right.\)⇒ 24a + 40b = 8,8(1)
\(Mg + 2HCl \to MgCl_2 + H_2\\ MgO + 2HCl \to MgCl_2 + H_2O\)
Theo PTHH :
\(n_{MgCl_2} = a + b = \dfrac{28,5}{95} = 0,3(2)\)
Từ (1)(2) suy ra: a = 0,2 ; b = 0,1
Vậy :
\(m_{Mg} = 0,2.24 = 4,8(gam) ; m_{MgO} = 0,1.40 = 4(gam)\\ \%m_{Mg} = \dfrac{4,8}{8,8}.100\% = 54,54\%\\ \%m_{MgO} = 100\% -54,54\% = 45,45\%\)
b)
\(n_{HCl} = 2n_{MgCl_2} = 0,3.2 = 0,6(mol)\\ C\%_{HCl} = \dfrac{0,6.36,5}{200}.100\% = 10,95\%\)
Đúng 3
Bình luận (0)
hòa tan 12g Mg trong V lít dd HNO3 2M thu được 2,24 lít khí N2O dktc và dd X cô cạn dd X thu được m g muối khan tính V và m
HD:
4Mg + 10HNO3 \(\rightarrow\) 4Mg(NO3)2 + N2O + 5H2O
0,5 0,1 mol
Theo phản ứng trên thì Mg dư 0,1 mol (vì số mol Mg = 4 lần số mol N2O = 0,4 mol, ban đầu Mg có 0,5 mol).
Sau khi cô cạn dung dịch thu được muối Mg(NO3)2 có số mol là 0,4 mol nên m = 0,4.148 = 59,2 g.
Số mol HNO3 đã phản ứng = 10.0,1 = 1,0 mol nên V = 1/2 = 0,5 lít = 500 ml.
Đúng 1
Bình luận (0)