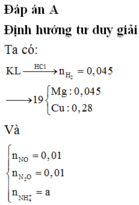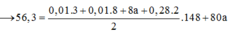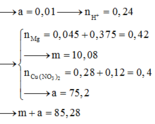oxh hoàn toàn m gam kim loại mg bằng khí chlorine (CL20 ) thu đc 19 gam muối chloride viết pthh của phản ứng xảy ra và tính giá trị m

Những câu hỏi liên quan
1khử hoàn toàn 16g CuO bằng khí H2 ở nhiệt độ cao . sau phản ứng thu đc m gam kim loại a.viết PTHH của phản ứng b.tính giá trị m 2cho 4,6g Nạ vào 100g nước sau khi phản ứng xảy ra hoàn toàn a tính thể tích khí thu đc ở đktc b.tính nồng độ phần trăm của chất tan có trong dung dịch
a)\(n_{CuO}=\dfrac{16}{80}=0,2mol\)
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
b)\(n_{Na}=\dfrac{4,6}{23}=0,2mol\)
\(n_{H_2O}=\dfrac{100}{18}=\dfrac{50}{9}mol\)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
\(0,2\) \(\dfrac{50}{9}\) 0 0
\(0,2\) 0,2 0,2 0,1
0 \(5,35\) 0,2 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn m gam Mg vào 100ml HCl 2M. phản ứng xảy ra hoàn toàn thu được chất khí không màu
a. Viết PTHH của PƯ
b. tính m gam và thể tích khí thoát ra ở đktc?
c. người ta cho một kim loại M (không rõ hóa trị) tác dụng vừa đủ với lượng axit HCl trên, sau PƯ thấy tạo thành 12,7 gam muối của kim loại M. Xác định kim loại M.
\(n_{HCl}=0.1\cdot2=0.2\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(0.1.......0.2.........................0.1\)
\(m_{Mg}=0.1\cdot24=2.4\left(g\right)\)
\(V_{H_2}=0.1\cdot22.4=2.24\left(l\right)\)
\(2M+2nHCl\rightarrow2MCl_n+nH_2\)
\(.........0.2.......\dfrac{0.2}{n}\)
\(M_{MCl_n}=\dfrac{12.7}{\dfrac{0.2}{n}}=63.5n\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow M+35.5n=63.5n\)
\(\Rightarrow M=28n\)
\(BL:n=2\Rightarrow M=56\)
\(M:Fe\)
Đúng 1
Bình luận (0)
a) Mg + 2HCl → MgCl2 + H2
b) n HCl = 0,1.2 = 0,2(mol)
n Mg = n H2 = 1/2 n HCl = 0,1(mol)
Suy ra:
m = 0,1.24 = 2,4(gam)
V H2 = 0,1.22,4 = 2,24(lít)
c) Gọi n là hóa trị M
2M +2nHCl $\to$ 2MCln + nH2
Theo PTHH :
n MCln = 1/n x n HCl = 0,2/n(mol)
Suy ra :
$\dfrac{0,2}{n}(M + 35,5n) = 12,7$
=> M = 28n
Với n = 2 thì M = 56(Fe)
Đúng 0
Bình luận (0)
Câu 3 :1. Để khử hoàn toàn 47,2 gam hỗn hợp CuO , FeO, Fe3O4 cần dùng V lít khí H2 (ở đktc). Sau phản ứng thu được m gam kim loại và 14,4 gam nước.a) Viết PTHH xảy ra?b) Tính giá trị m và V?2. Đốt cháy hoàn toàn 23 gam hợp chất A cần 33,6 lít ôxi (đktc) và thu được thể tích CO2 bằng 2/3 thể tích hơi nước . Xác định CTHH của A. Biết rằng tỉ khối hơi của A so với khí ôxi là 1,4375.
Đọc tiếp
Câu 3 :
1. Để khử hoàn toàn 47,2 gam hỗn hợp CuO , FeO, Fe3O4 cần dùng V lít khí H2 (ở đktc). Sau phản ứng thu được m gam kim loại và 14,4 gam nước.
a) Viết PTHH xảy ra?
b) Tính giá trị m và V?
2. Đốt cháy hoàn toàn 23 gam hợp chất A cần 33,6 lít ôxi (đktc) và thu được thể tích CO2 bằng 2/3 thể tích hơi nước . Xác định CTHH của A. Biết rằng tỉ khối hơi của A so với khí ôxi là 1,4375.
Đốt cháy hoàn toàn 4,8 gam kim loại M (hóa trị 2) bằng khí chlorine, thu được 19 gam muối chloride.Xác định kim loại M
Áp dụng định luật bảo toàn khối lượng:
`m_(Cl_2)=19-4,8=14,2(g)`
`=>n_(Cl_2)=(14,2)/(71)=0,2(mol)`
PTHH: \(M+Cl_2 \rightarrow MCl_2\) (có điều kiện `t^o)`
Từ đó ta suy ra `n_(M)=0,2(mol)`
`=>M=(4,8)/(0,2)=24`
`=>M` là `Mg` (Magiê)
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn m gam kim loại zinc cần dùng hết 7,3 gam hydrochloric acid HCl, sau phản ứng thu được zinc chloride và khí hydrogen. Sơ đồ phản ứng: Zn + HCl ---> ZnCl2 + H2 Viết phương trình hóa học. Tính giá trị của m. Tính thể tích khí thoát ra (đkc). Tính khối lượng muối ZnCl2 tạo thành. (Zn=65, H=1, Cl=35,5)
\(n_{HCl}=\dfrac{7,3}{36,5}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,1<---0,2------>0,1--->0,1
=> mZn = 0,1.65 = 6,5(g)
=> VH2 = 0,1.22,4 = 2,24(l)
=> mZnCl2 = 0,1.136 = 13,6(g)
Đúng 3
Bình luận (0)
\(n_{HCl}=\dfrac{7.3}{36.5}=0.2\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0.1........0.2........0.1..........0.1\)
\(m_{Zn}=0.1\cdot65=6.5\left(g\right)\)
\(m_{ZnCl_2}=0.1\cdot136=13.6\left(g\right)\)
\(V_{H_2}=0.1\cdot22.4=2.24\left(l\right)\)
Đúng 5
Bình luận (0)
Zn + 2HCl \(\rightarrow\) ZnCl2 + H2
\(n_{HCl}=\dfrac{7,3}{36,5}=0,2mol\)
\(\Rightarrow n_{Zn}=\dfrac{0,2}{2}=0,1mol\\ m_{Zn}=0,1.65=6,5g\)
\(\Rightarrow n_{H_2}=\dfrac{0,2}{2}=0,1mol\\ V_{H_2}=0,1.22,4=2,24l\)
\(\Rightarrow n_{ZnCl_2}=\dfrac{0,2}{2}=0,1mol\\ m_{ZnCl_2}=0,1.\left(65+35,5.2\right)=13,6g\)
Đúng 1
Bình luận (0)
Cho m gam kim loại Fe tan hết trong dung dịch HNO3 25,2%, sau phản ứng hoàn toàn thu được 0,672 lít khí NO (đktc) là sản phẩm khử duy nhất của N trong HNO3. Cô cạn dung dịch sau phản ứng thu được 7,82 gam muỗi khan. Viết phương trình phản ứng xảy ra. Tính giá trị của m và tính nồng độ phần trăm của muối trong dung dịch sau phản ứng
Đọc tiếp
Cho m gam kim loại Fe tan hết trong dung dịch HNO3 25,2%, sau phản ứng hoàn toàn thu được 0,672 lít khí NO (đktc) là sản phẩm khử duy nhất của N trong HNO3. Cô cạn dung dịch sau phản ứng thu được 7,82 gam muỗi khan.
Viết phương trình phản ứng xảy ra. Tính giá trị của m và tính nồng độ phần trăm của muối trong dung dịch sau phản ứng
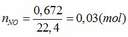
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O (1)
a → 4a → a → a (mol)
3Fe + 8HNO3 → 3Fe(NO3)2 + 2NO + 4H2O (2)
B → 8/3b → b →2/3b (mol)
TH1: xảy ra phản ứng (1) tạo muối Fe(NO3)3 => nFe(NO3)3 = nNO = 0,03 (mol)
=> mmuối = mFe(NO3)3 = 0,03. 242 = 7,26 (g) # 7,82 => loại
TH2: xảy ra phản ứng (2) tạo muối Fe(NO3)2 => nFe(NO3)2 = 3/2 nNO = 3/2 . 0,03 = 0,045 (mol)
=> mmuối = mFe(NO3)2 = 0,045. 180 = 8,1 (g) # 7,82 => loại
TH3: xảy ra cả (1) và (2) phản ứng tạo 2 muối.
Gọi số mol của Fe ở phản ứng (1) và (2) lần lượt là a và b (mol)
Đặt vào phương trình ta có:
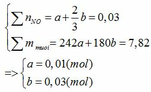
∑ nFe = 0,01 + 0,03 = 0,04 (mol) => mFe = 0,04.56 = 2,24 (g)
∑ nHNO3 pư = 4a + 8/3b = 4. 0,01 + 8/3. 0,03 = 0,12 (mol)
mHNO3 = 0,12.63 = 7,56 (g)
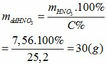
Khối lượng dd sau: mdd sau = mFe + mddHNO3 - mNO = 2,24 + 30 – 0,03.30 = 31,34 (g)
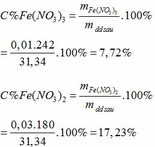
Đúng 1
Bình luận (0)
Cho 4,23 gam hỗn hợp Mg và Al vào dung dịch chứa AgNO3 0,84M và Cu(NO3)2 0,96M, sau khi các phản ứng xảy ra hoàn toàn, thu được 23,12 gam hỗn hợp kim loại và dung dịch X chứa m gam muối. Cho X phản ứng hoàn toàn với dung dịch NaOH loãng (dư), thu được 10,39 gam kết tủa. Bỏ qua sự thủy phân của muối trong dung dịch. Giá trị của m gần nhất với giá trị nào sau đây? A. 32. B. 33. C. 34. D. 35.
Đọc tiếp
Cho 4,23 gam hỗn hợp Mg và Al vào dung dịch chứa AgNO3 0,84M và Cu(NO3)2 0,96M, sau khi các phản ứng xảy ra hoàn toàn, thu được 23,12 gam hỗn hợp kim loại và dung dịch X chứa m gam muối. Cho X phản ứng hoàn toàn với dung dịch NaOH loãng (dư), thu được 10,39 gam kết tủa. Bỏ qua sự thủy phân của muối trong dung dịch. Giá trị của m gần nhất với giá trị nào sau đây?
A. 32.
B. 33.
C. 34.
D. 35.
Điện phân dung dịch T chứa a gam Cu(NO3)2 với điện cực trơ một thời gian rồi nhấc nhanh các điện cực ra thu được dung dịch X. Cho m gam bột Mg vào dung dịch X, sau khi phản ứng xảy ra hoàn toàn thu được 19 gam hỗn hợp kim loại, 0,448 lít hỗn hợp khí Z (đktc) gồm NO và N2O có tỉ khối đối với H2 là 18,5 và dung dịch Y chứa 56,3 gam muối. Cho toàn bộ hỗn hợp bột kim loại trên tác dụng với dung dịch HCl dư thu được 1,008 lít khí H2 (đktc). Giá trị của (m+a) là? A. 85,28 B. 92,80 C. 78,12 D. 88,42
Đọc tiếp
Điện phân dung dịch T chứa a gam Cu(NO3)2 với điện cực trơ một thời gian rồi nhấc nhanh các điện cực ra thu được dung dịch X. Cho m gam bột Mg vào dung dịch X, sau khi phản ứng xảy ra hoàn toàn thu được 19 gam hỗn hợp kim loại, 0,448 lít hỗn hợp khí Z (đktc) gồm NO và N2O có tỉ khối đối với H2 là 18,5 và dung dịch Y chứa 56,3 gam muối. Cho toàn bộ hỗn hợp bột kim loại trên tác dụng với dung dịch HCl dư thu được 1,008 lít khí H2 (đktc). Giá trị của (m+a) là?
A. 85,28
B. 92,80
C. 78,12
D. 88,42
Điện phân dung dịch T chứa a gam Cu(NO3)2 với điện cực trơ một thời gian rồi nhấc nhanh các điện cực ra thu được dung dịch X. Cho m gam bột Mg vào dung dịch X, sau khi phản ứng xảy ra hoàn toàn thu được 19 gam hỗn hợp kim loại, 0,448 lít hỗn hợp khí Z (đktc) gồm NO và N2O có tỉ khối đối với H2 là 18,5 và dung dịch Y chứa 56,3 gam muối. Cho toàn bộ hỗn hợp bột kim loại trên tác dụng với dung dịch HCl dư thu được 1,008 lít khí H2 (đktc). Giá trị của (m+a) là? A. 85,28 B. 92,80 C. 78,12 D. 88,42
Đọc tiếp
Điện phân dung dịch T chứa a gam Cu(NO3)2 với điện cực trơ một thời gian rồi nhấc nhanh các điện cực ra thu được dung dịch X. Cho m gam bột Mg vào dung dịch X, sau khi phản ứng xảy ra hoàn toàn thu được 19 gam hỗn hợp kim loại, 0,448 lít hỗn hợp khí Z (đktc) gồm NO và N2O có tỉ khối đối với H2 là 18,5 và dung dịch Y chứa 56,3 gam muối. Cho toàn bộ hỗn hợp bột kim loại trên tác dụng với dung dịch HCl dư thu được 1,008 lít khí H2 (đktc). Giá trị của (m+a) là?
A. 85,28
B. 92,80
C. 78,12
D. 88,42