. Cho 300 ml dung dịch Al2(SO4)3 0,2M tác dụng dung dịch BaCl2
a. Nêu hiện tượng phản ứng
b. Tính khối lượng sản phẩm
. Cho 200 g dung dịch NaOH 16% tác dụng với FeCl2
a. Nêu hiện tượng phản ứng
b. Tính khối lượng sản phẩm
a, - Hiện tượng: Xuất hiện kết tủa trắng xanh.
b, \(m_{NaOH}=200.16\%=32\left(g\right)\Rightarrow n_{NaOH}=\dfrac{32}{40}=0,8\left(mol\right)\)
PT: \(2NaOH+FeCl_2\rightarrow Fe\left(OH\right)_{2\downarrow}+2NaCl\)
Theo PT: \(\left\{{}\begin{matrix}n_{Fe\left(OH\right)_2}=\dfrac{1}{2}n_{NaOH}=0,4\left(mol\right)\\n_{NaCl}=n_{NaOH}=0,8\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{Fe\left(OH\right)_2}=0,4.90=36\left(g\right)\)
\(m_{NaCl}=0,8.58,5=46,8\left(g\right)\)
1. Cho 3,42 gam Al2(SO4)3 tác dụng với 200 ml dung dịch NaOH, sau phản ứng thu được 0,78 gam kết tủa. Nồng độ mol nhỏ nhất của dung dịch NaOH đã dùng là
2. Rót V ml dung dịch NaOH 2M vào cốc đựng 300 ml dung dịch Al2(SO4)3 0,25M thu được kết tủa. Lọc kết tủa rồi nung đến khối lượng ko đổi được 5,1 gam chất rắn. Giá trị lớn nhất của V là
3. Cho 150 ml dung dịch KOH 1,2M tác dụng với 100 ml dung dịch AlCl3 nồng độ x mol/l, thu được dung dịch Y và 4,68 gam kết tủa. Loại bỏ kết tủa, thêm tiếp 175 ml dung dịch KOH 1,2M vào Y, thu được 2,34 gam kết tủa. Giá trị của x là:
Làm 3 bài trên nhưng không dùng phương trình ion, dùng pthh với ạ
1) \(n_{Al\left(OH\right)_3}=\dfrac{0,78}{78}=0,01\left(mol\right)\)
PTHH: \(Al_2\left(SO_4\right)_3+6NaOH\rightarrow3Na_2SO_4+2Al\left(OH\right)_3\)
0,03<----------------------0,01
=> nNaOH min = 0,03 (mol)
=> \(C_{M\left(NaOH\right)}=\dfrac{0,03}{0,2}=0,15M\)
2) \(n_{Al_2O_3}=\dfrac{5,1}{102}=0,05\left(mol\right)\)
\(n_{Al_2\left(SO_4\right)_3}=0,3.0,25=0,075\left(mol\right)\)
PTHH: \(6NaOH+Al_2\left(SO_4\right)_3\rightarrow3Na_2SO_4+2Al\left(OH\right)_3\)
0,45<------0,075-------------------------->0,15
\(NaOH+Al\left(OH\right)_3\rightarrow NaAlO_2+2H_2O\)
0,05<----0,05
\(2Al\left(OH\right)_3\underrightarrow{t^o}Al_2O_3+3H_2O\)
0,1<-------0,05
=> nNaOH max = 0,5 (mol)
=> \(V_{dd}=\dfrac{0,5}{2}=0,25\left(l\right)=250\left(ml\right)\)
3)
\(n_{KOH\left(1\right)}=0,15.1,2=0,18\left(mol\right)\)
\(n_{Al\left(OH\right)_3\left(1\right)}=\dfrac{4,68}{78}=0,06\left(mol\right)\)
\(n_{AlCl_3}=0,1.x\left(mol\right)\)
Do khi cho KOH tác dụng với dd Y xuất hiện kết tủa
=> Trong Y chứa AlCl3 dư
PTHH: \(3KOH+AlCl_3\rightarrow3KCl+Al\left(OH\right)_3\)
0,18---->0,06----------------->0,06
\(n_{KOH\left(2\right)}=0,175.1,2=0,21\left(mol\right)\)
\(n_{Al\left(OH\right)_3\left(2\right)}=\dfrac{2,34}{78}=0,03\left(mol\right)\)
PTHH: \(3KOH+AlCl_3\rightarrow3KCl+Al\left(OH\right)_3\)
(0,3x-0,18)<--(0,1x-0,06)------->(0,1x-0,06)
\(KOH+Al\left(OH\right)_3\rightarrow KAlO_2+2H_2O\)
(0,1x-0,09)<-(0,1x-0,09)
=> \(\left(0,3x-0,18\right)+\left(0,1x-0,09\right)=0,21\)
=> x = 1,2
Cho 500 ml dung dịch NaCl 2M tác dụng với 600 ml dung dịch AgNO3 2M.
a. Nêu hiện tượng phản ứng.
b. Tính khối lượng kết tủa tạo thành.
c. Tính nồng độ chất còn lại trong dung dịch.
a)
Xuất hiện kết tủa màu trắng
b)
$AgNO_3 + NaCl \to AgCl + NaNO_3$
$n_{NaCl} = 0,5.2 = 1 < n_{AgNO_3} = 0,6.2 = 1,2$ nên $AgNO_3$ dư
$n_{AgCl} = n_{NaCl} = 1(mol)$
$m_{AgCl} = 1.143,5 = 143,5(gam)$
c)
$n_{NaNO_3} = n_{NaCl} = 1(mol)$
$n_{AgNO_3\ dư} = 1,2 - 1 = 0,2(mol)$
$V_{dd} = 0,5 + 0,6 = 1,1(lít)$
$C_{M_{NaNO_3}} = \dfrac{1}{1,1} = 0,91M$
$C_{M_{AgNO_3}} = \dfrac{0,2}{1,1} = 0,18M$
cho kim loại nhôm tác dụng vừa đủ với dung dịch axit sunfuric(H2SO4). sau phản ứng thu được muối sunfat (Al2(SO4)3) vaf3,36 lit khí hidro ở dktc.
a) lập PTHH cho phản ứng
b)tính khối lượng nhôm đẫ tham gia phản ứng
c) tính khối lượng muối nhôm sunfat thu được sau phản ứng.
d) dẫn toàn bộ lượng khí hidro thu được ở trên vào bình đựng khí oxi rồi đốt cháy. hỏi chất nào dư sau phản ứng và thế tích còn dư bao nhiêu/ biết sản phâm thu được là nước (H2O)
e) nếu hiệu suất của phản ứng H=80%. hãy tính khối lượng của axit clohidric thực tế đã lấy và khối lượng Zn ban đầu.
a: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
b: \(n_{H2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(\Leftrightarrow n_{Al}=0.1\left(mol\right)\)
\(m_{Al}=n_{Al}\cdot M_{Al}=0.1\cdot27=2.7\left(g\right)\)
Cho 200ml dung dịch Al2(SO4)3 0,1M vào 300 ml dung dịch KOH 0,2M thu được m gam kết tủa và 500 ml dung dịch X.
a) Tính m và nồng độ CM của dung dịch X.
b) Tiếp tục cho vào 500 ml dung dịch X 350 ml dung dịch KOH ở trên, kết thúc phản ứng thu được m’ gam kết tủa và dung dịch Y. Tính m; và nồng độ CM của dung dịch Y.
\(n_{Al_2(SO_4)_3}=0,1.0,2=0,02(mol)\\ n_{KOH}=0,2.0,3=0,06(mol)\\ PTHH:Al_2(SO_4)_3+6KOH\to 2Al(OH)_3\downarrow+3K_2SO_4\)
Vì \(\dfrac{n_{Al_2(SO_4)_3}}{1}>\dfrac{n_{KOH}}{6}\) nên \(Al_2(SO_4)_3\) dư
\(a,n_{K_2SO_4}=\dfrac{1}{2}n_{KOH}=0,3(mol)\\ n_{Al(OH)_3}=\dfrac{1}{3}n_{KOH}=0,2(mol)\\ \Rightarrow m_{Al(OH)_3}=0,2.78=15,6(g)\\ C_{M_{K_2SO_4}}=\dfrac{0,3}{0,5}=0,6M\)
\(b,K_2SO_4\) ko tác dụng được với \(KOH\), bạn xem lại đề
Cho 200 ml dung dịch chứa KOH 0,9M và Ba(OH)2 0,2M vào 100 ml dung dịch H2SO4 0,3M và Al2(SO4)3 0,3M. Sau khi các phản ứng xảy ra hoàn toàn, khối lượng kết tủa thu được là
A. 9,32
B. 10,88
C. 14,00
D. 12,44
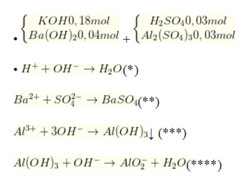
n O H - = n H + = 0 , 06 m o l T h e o ( * * ) n B a S O 4 = n B a 2 + = 0 , 04 m o l T h e o ( * * * ) n O H - = 3 x 0 , 03 x 2 = 0 , 18 m o l ; n A l ( O H ) 3 = 0 , 03 x 2 = 0 , 06 m o l T h e o ( * * * * ) n O H - = 0 , 18 + 0 , 04 x 2 - 0 , 06 - 0 , 18 = 0 , 02 m o l n A l ( O H ) 3 d ư = 0 , 06 - 0 , 02 = 0 , 04 m o l .
→ m↓ = mAl(OH)3 + mBaSO4 = 0,04 × 78 + 0,04 × 233 = 12,44 gam
→ Đáp án đúng là đáp án D
Bài 5: Cho 400 ml dung dịch E gồm AlCl3 x mol/lít và Al2(SO4)3 y mol/lít tác dụng với 612 ml dung dịch
NaOH 1M, sau khi các phản ứng kết thúc thu được 8,424 gam kết tủa. Mặt khác, khi cho 400 ml E tác dụng với dung dịch BaCl2 (dư) thì thu được 33,552 gam kết tủa. Tìm x,y.
400 ml dd E gồm AlCl3 xM và Al2(SO4)3 yM + 0,612 mol NaOH → 0,108 mol Al(OH)3.
400 ml E + BaCl2 dư → 0,144 mol ↓BaSO4.
=> n BaSO4 = 3y = 0,144 → y = 0,048 (*).
Ở TN1:
nAl(OH)3 = nAl3+ - (nOH- - 3nAl3+)
= 4nAl3+ - nOH-
= 4(x + 2y) - 0,612 = 0,108 (**)
Từ (*), (**) => x = 0,084.
Cho 250 ml dung dịch NaOH 4M vào 50 ml dung dịch Al2(SO4)3 2M. Thu được dung dịch X. tính khối lượng kết tủa sau phản ứng
\(n_{NaOH}=0,25.4=1\left(mol\right)\\ n_{Al_2\left(SO_4\right)_3}=2.0,05=0,1\left(mol\right)\\ PTHH:6NaOH+Al_2\left(SO_4\right)_3\rightarrow2Al\left(OH\right)_3+3Na_2SO_4\\ Vì:\dfrac{1}{6}>\dfrac{0,1}{1}\\ \Rightarrow NaOHdư\\ \rightarrow n_{Al\left(OH\right)_3}=2.0,1=0,2\left(mol\right)\\ m_{kt}=m_{Al\left(OH\right)_3}=78.0,2=15,6\left(g\right)\)
\(n_{NaOH}=0.25\cdot4=1\left(mol\right)\)
\(n_{Al_2\left(SO_4\right)_3}=0.05\cdot2=0.1\left(mol\right)\)
\(Al_2\left(SO_4\right)_3+6NaOH\rightarrow2Al\left(OH\right)_3+3Na_2SO_4\)
Lập tỉ lệ :
\(\dfrac{0.1}{1}< \dfrac{1}{6}\) \(\Rightarrow NaOHdư\)
\(n_{NaOH\left(dư\right)}=1-0.6=0.4\left(mol\right)\)
\(n_{Al\left(OH\right)_3}=0.1\cdot2=0.2\left(mol\right)\)
\(NaOH+Al\left(OH\right)_3\rightarrow NaAlO_2+2H_2O\)
\(n_{NaOH}>n_{Al\left(OH\right)_3}\)
=> Kết tủa tan hoàn toàn
\(m_{\downarrow}=0\)
\(n_{NaOH}=1\left(mol\right);n_{Al_2\left(SO_4\right)_3}=0,1\left(mol\right)\)
Al2(SO4)3 + 6NaOH ⟶ 2Al(OH)3 + 3Na2SO4
0,1...................0,6.................0,2
Al(OH)3 + NaOH ⟶ NaAlO2 + 2H2O
0,2............0,4
=> Sau phản ứng NaOH dư, kết tủa tan hết
=> Khối lượng kết tủa là 0g
Cho Mg tác dụng với 200 ml dung dịch HNO3 thu được 4,48 lít khí NO2 (đktc) (sản phẩm khử duy nhất)
a) Tìm khối lượng kim loại Mg đã phản ứng
b) Tìm CM của axit đã dùng.
a) \(n_{NO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Mg + 4HNO3 --> Mg(NO3)2 + 2NO2 + 2H2O
0,1<--0,4<------------------------0,2
=> mMg = 0,1.24 = 2,4 (g)
b) \(C_M=\dfrac{0,4}{0,2}=2M\)