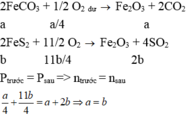oxi hóa 6,7 g hh X gồm Fe, Cu, Al trong Không Khí đến pứ hoàn toàn sau pứ thu đc 8,7 g hh chất rắn Y tính thể tích không khí

Những câu hỏi liên quan
nung m (g) hh X gồm Fe3O4 và Al trong điều kiện không có không khí. sau khi pứ xảy ra hoàn toàn thu được hh Y. chia hh Y thành 2 phần
P1: cho tác dụng với dd NaOH dư thu được 0,06mol H2, dd Z và 20,16g chất rắn không tan.
P2: cho tác dụng với dd HCl dư thu được 0,63mol H2
Tính thành phần % khối lượng các chất trong hh X
PTHH: 3Fe3O4 + 8Al --to--> 4Al2O3 + 9Fe
=> \(\dfrac{n_{Fe}}{n_{Al_2O_3}}=\dfrac{9}{4}\)
P1: Gọi (nAl; nFe; nAl2O3) = (a;b;c)
PTHH: 2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
0,04<---------------------------------0,06
=> a = 0,04 (mol)
Chất rắn không tan là Fe
\(b=\dfrac{20,16}{56}=0,36\left(mol\right)\)
Có: \(\dfrac{n_{Fe}}{n_{Al_2O_3}}=\dfrac{b}{c}=\dfrac{9}{4}\) => c = 0,16 (mol)
P2: Gọi (nAl; nFe; nAl2O3) = (ak;bk;ck)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
ak------------------>1,5ak
Fe + 2HCl --> FeCl2 + H2
bk------------------>bk
=> 1,5ak + bk = 0,63
=> k = 1,5
Bảo toàn Fe: \(n_{Fe_3O_4\left(X\right)}=\dfrac{b+bk}{3}=\dfrac{0,36+0,36.1,5}{3}=0,3\left(mol\right)\)
Bảo toàn Al: \(n_{Al\left(X\right)}=a+2c+ak+2ck=0,9\left(mol\right)\)
\(\left\{{}\begin{matrix}\%m_{Fe_3O_4}=\dfrac{0,3.232}{0,3.232+0,9.27}.100\%=74,12\%\\\%m_{Al}=\dfrac{0,9.27}{0,3.232+0,9.27}.100\%=25,88\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Hòa tan hết 17.44g hh gồm Fe, Fe2o3, CuO ,Cu ,Mg bằng dd H2SO4 đặc nóng sau pứ thu dc dd y và 2.464 lít khí SO2 dktc cho dd y tác dụng với NaOH dư, lọc kết tủa đem nung trong không khí đến khối lượng ko đổi thì dc m g chất rắn. tính m GIẢI CHI TIẾT GIÚP EM VỚI Ạ !
Xem chi tiết
HH X gồm Al, Zn, Cu.Cho 18,3 g X td với dd H2SO4 sau pứ thu đc 8,96 l H2. Ở nhiệt độ cao 0,8 nX td vs 56 l Không Khí. Tính % m các chất trong hh ban đầu
Gọi: \(\left\{{}\begin{matrix}n_{Al}=a\left(mol\right)\\n_{Zn}=b\left(mol\right)\\n_{Cu}=c\left(mol\right)\end{matrix}\right.\) ⇒ 27a + 65b + 64c = 18,3 (1)
- Cho hh pư với H2SO4.
PT: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Zn}=\dfrac{3}{2}a+b=\dfrac{8,96}{22,4}=0,4\left(mol\right)\left(2\right)\)
- Cho hh pư với không khí.
Ta có: ka + kb + kc = 0,8 (3)
PT: \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(2Zn+O_2\underrightarrow{t^o}2ZnO\)
\(2Cu+O_2\underrightarrow{t^o}2CuO\)
Theo PT: \(n_{O_2}=\dfrac{3}{4}n_{Al}+\dfrac{1}{2}n_{Zn}+\dfrac{1}{2}n_{Cu}=\dfrac{3}{4}ka+\dfrac{1}{2}kb+\dfrac{1}{2}kc=\dfrac{56}{22,4}.\dfrac{1}{5}=0,5\left(4\right)\)
Từ (3) và (4) ⇒ a - b - c = 0 (5)
Từ (1) (2) và (5) \(\Rightarrow\left\{{}\begin{matrix}a=0,2\left(mol\right)\\b=0,1\left(mol\right)\\c=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2.27}{18,3}.100\%\approx29,51\%\\\%m_{Zn}=\dfrac{0,1.65}{18,3}.100\%\approx35,52\%\\\%m_{Cu}\approx34,97\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Chia hh X gồm Al và kim loại M (hóa trị không đổi) thành 3 phần bằng nhau: P1: cho vào dd NaOH dư sau khi pứ xảy ra hoàn toàn thấy thoát ra 1,4874 lít khí H2(đktc) và còn lại một phần chất rắn không tan. P2: đốt cháy trong V1 lít khí Oxi(đktc), thu được dd rắn Y gồm 4 chất. Để hòa tan hoàn toàn Y cần dùng vừa đủ 200ml dd gồm H2SO4 0,3M và HCl 0,4M thu được 0,9916 lít khí H2 (đktc) và dd chỉ chứa 10,64g hh các muối trung hòa. 1) Xác định kim loại M và tính giá trị V1 P3: Cho vào V2 lít...
Đọc tiếp
Chia hh X gồm Al và kim loại M (hóa trị không đổi) thành 3 phần bằng nhau:
P1: cho vào dd NaOH dư sau khi pứ xảy ra hoàn toàn thấy thoát ra 1,4874 lít khí H2(đktc) và còn lại một phần chất rắn không tan.
P2: đốt cháy trong V1 lít khí Oxi(đktc), thu được dd rắn Y gồm 4 chất. Để hòa tan hoàn toàn Y cần dùng vừa đủ 200ml dd gồm H2SO4 0,3M và HCl 0,4M thu được 0,9916 lít khí H2 (đktc) và dd chỉ chứa 10,64g hh các muối trung hòa.
1) Xác định kim loại M và tính giá trị V1
P3: Cho vào V2 lít dd CuSO4 0,5M khuấy đều sau khi pứ xảy ra hoàn toàn thu được 5,71g chất rắn. Tính giá trị V2
Bài 1 : hoà tan 7.8g hh Al ,Mg bằng dd HCl dư .sau pư m dd tăng O.7 g .tính k.luợng kloai trong hh đầu
Bài 2 : lấy 3l khí Cl táv dunv vs 2 lit khí H2 hiệu suất 20% .tính thể tích hh khí sau pứ
Bài 3 : cho 10g hh gồm Al , Mg Cu tác dunv vừa đủ vs dd Hcl 20% thu đc 7.84l khí , 2.5g chất rắn . a) tính m k.loai. .b) tính m HCl cần dùng
Giúp mìk với
Bài 1: gọi a,b là ố mol của Mg và Al
Mg + 2HCl - > MgCl2 + H2
-a---------------------------------a
Al + 3HCl -> AlCl3 + 3/2H2
-b---------------------b-------3/2b-
Ta có 24a+27b=7.8 g (1)
Mà bạn thấy nhé! Hòa tan 7,8g kim loại HOÀN TOÀN vào HCl dư mà dung dịch chỉ tăng thêm 7g
=> 0,8g mất đi là do H2 bay hơi -> nH2 = 0.4 mol
Có thêm a+3/2b=0.4 (2)
từ 1 và 2 ta có hệ pt: \(\begin{cases}24a+27b=7,8\\a+\frac{3}{2}b=0,4\end{cases}\)
<=> \(\begin{cases}a=0,1\\b=0,2\end{cases}\)
=> mMg =0,1.24=2,4g
=> mAl=7,8-2,4=5,4g
Bài 2: H2+Cl2=>2HCl
Theo định luật bảo toàn thì là 5 lít thôi
H=20%=> V=5:100.20=1lit
Đúng 0
Bình luận (2)
Nung một hh rắn gồm a mol FeCO3 và b mol FeS2 trong bình kín chứa không khí (dư). Sau khi các pư xảy ra hoàn toàn, đưa bình về nhiệt độ ban đầu, thu được chất rắn duy nhất 1à Fe2O3 và hh khí. Biết áp suất khí trong bình trước và sau pư bằng nhau, mối 1iên hệ giữa a và b 1à (biết sau các pứ,1ưu huỳnh ở mức oxi hoá +4, thể tích các chất rắn 1à không đáng kể) A. a 0,5b. B. a b. C. a 4b. D. a 2b.
Đọc tiếp
Nung một hh rắn gồm a mol FeCO3 và b mol FeS2 trong bình kín chứa không khí (dư). Sau khi các pư xảy ra hoàn toàn, đưa bình về nhiệt độ ban đầu, thu được chất rắn duy nhất 1à Fe2O3 và hh khí. Biết áp suất khí trong bình trước và sau pư bằng nhau, mối 1iên hệ giữa a và b 1à (biết sau các pứ,1ưu huỳnh ở mức oxi hoá +4, thể tích các chất rắn 1à không đáng kể)
A. a = 0,5b.
B. a = b.
C. a = 4b.
D. a = 2b.
Cho 21,9 g hh gồm Al và Cu pứ xủa đủ với 12,,32 l khí Cl2. Tính m mõi muối thu được sau pứ
\(Al+\dfrac{3}{2}Cl_2->AlCl_3\\ Cu+Cl_2->CuCl_2\\ n_{Al}=a;n_{Cu}=b\\ 27a+64b=21,9\\ 1,5a+b=\dfrac{12,32}{22,4}=0,55\\ a=0,19;b=0,26\\ m_{AlCl_3}=133,5\cdot0,19=25,365g\\ m_{CuCl_2}=135\cdot0,26=35,1g\)
Đúng 2
Bình luận (2)
1. Hoà tan hoàn toàn hh kim loại gồm Mg, Cu, Fe trong dd HCl thu được dd X, chất rắn Y và khí X td hoàn toàn với dd NaOH, thu được kết tủa T. Nung hoàn toàn kết tủa T trong không khí thu được kết tủa rắn gồm?
2. Cho 13,44l hh khí A gồm Clo và Xoi td hết với 19,2g hh B gồm Mg và Al tạo ra 48,15g hh muối clorua và oxit của 2 kim loại. Khối lượng của Mg trong hh B là?
3. Cho 22g hh 2 muối NaX với X, Y là hai halogen ở hai chu kỳ liên tiếp vào dd AgNO3 dư thu được 47,5g kết tủa. X và Y là?
4. Cho...
Đọc tiếp
1. Hoà tan hoàn toàn hh kim loại gồm Mg, Cu, Fe trong dd HCl thu được dd X, chất rắn Y và khí X td hoàn toàn với dd NaOH, thu được kết tủa T. Nung hoàn toàn kết tủa T trong không khí thu được kết tủa rắn gồm?
2. Cho 13,44l hh khí A gồm Clo và Xoi td hết với 19,2g hh B gồm Mg và Al tạo ra 48,15g hh muối clorua và oxit của 2 kim loại. Khối lượng của Mg trong hh B là?
3. Cho 22g hh 2 muối NaX với X, Y là hai halogen ở hai chu kỳ liên tiếp vào dd AgNO3 dư thu được 47,5g kết tủa. X và Y là?
4. Cho 11,2l hh khí A gồm Clo và Oxi td hết với 16,98g hh B gồm Mg và Al tạo ra 42,34g hh muối clorua và oxit của 2 kim loại. Khối lượng của Mg, Al trong hh B lần lượt là?
5. Hòa tan 10g hh muối acbonat kim loại hóa trị 2 bằng dd Hcl dư ta thu được dd A và 2,24l khí bay ra. Cô cạn dd A thì thu được khối lượng muối khan là?
C1 :
- Hòa tan hh vào dd HCl :
Mg + 2HCl => MgCl2 + H2
Fe + 2HCl => FeCl2 + H2
X : MgCl2 , FeCl2 , HCl dư
Y : Cu
Z : H2
- Dung dịch X + NaOH :
MgCl2 + 2NaOH => Mg(OH)2 + 2NaCl
FeCl2 + 2NaOH => Fe(OH)2 + 2NaCl
Kết tủa T : Mg(OH)2 , Fe(OH)2
- Nung T :
Mg(OH)2 -to-> MgO + H2O
4Fe(OH)2 + O2 -to-> 2Fe2O3 + 4H2O
Chất rắn : MgO , Fe2O3
C2:
Đặt : nCl2 = x (mol) , nO2 = y (mol)
nA = x + y = 0.6 (mol) (1)
mCl2 + mO2 = 48.15 - 19.2 = 28.95 (g)
=> 71x + 32y = 28.95 (2)
(1),(2) :
x = 0.25 , y = 0.35
Đặt : nMg = a (mol) , nAl = b (mol)
Mg => Mg+2 + 2e
Al => Al+3 + 3e
Cl2 + 2e => 2Cl-1
O2 + 4e => 2O2-
BT e :
2a + 3b = 0.25*2 + 0.35*4 = 1.9
mB = 24a + 27b = 19.2
=> a = 0.35
b = 0.4
%Mg = 0.35*24/19.2 * 100% = 43.75%
Đúng 3
Bình luận (0)
Đốt 6,7 gam hỗn hợp X gồm các kim loại Fe, Al, Cu và Ag trong không khí. Sau phản ứng thu được 8,7 gam hỗn hợp chất rắn Y. Hoà tan Y bằng dung dịch HCl dư thấy còn lại 2,7 gam một chất rắn. Tính thể tích dung dịch HCl 2M vừa đủ để hoà tan Y.
So sánh các phản ứng của hỗn hợp X với oxi và hỗn hợp Y với dung dịch HCl, ta thấy :
n HCl = 2 n trong oxit ; m O 2 = 8,7 - 6,7 = 2g
n O trong oxit = 0,125 mol; n HCl = 0,25 mol
V HCl = 0,25/2 = 0,125l
Đúng 0
Bình luận (0)