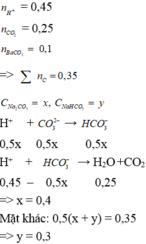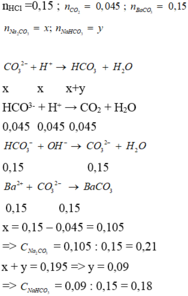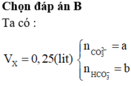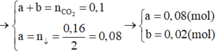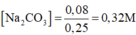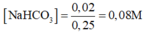Cho 200ml dung dịch Ca(OH)2 1M tác dụng hết với 250ml dung dịch Na2CO3 thu được kết tủa trắng. Tính nồng độ mol Na2CO3 đã dùng và m gam kết tủa.

Những câu hỏi liên quan
Giải giúp e vs ạ e cảm ơn
Bài 2: Cho 200ml dung dịch Na2CO3 1M tác dụng vừa đủ với 200 gam dung dịch Ba (OH) 2 . a. Viết PTHH xảy ra. b. Tính khối lượng chất kết tủa thu được. c. Tính nồng độ % của dung dịch Ba (OH) 2 dùng cho phản ứng trên.
a.
\(Na_2CO_3+Ba\left(OH\right)_2\rightarrow BaCO_3+2NaOH\)
b.
\(n_{BaCO_3}=n_{Na_2CO_3}=0,2.1=0,2\left(mol\right)\\ m_{kt}=197.0,2=39,4\left(g\right)\)
c.
\(n_{Ba\left(OH\right)_2}=n_{Na_2CO_3}=0,2\left(mol\right)\\ C\%_{Ba\left(OH\right)_2}=\dfrac{0,2.171.100\%}{200}=17,1\%\)
Đúng 3
Bình luận (0)
Cho từ từ 450 ml dd HCl 1M vào 500 ml dung dịch X gồm Na2CO3 và NaHCO3 thì thu được 5,6 lít khí (đktc) và dung dịch Y. Cho dung dịch Y tác dụng với dung dịch Ba(OH)2 dư thì thu được 19,7 gam kết tủa. Nồng độ mol của Na2CO3 và NaHCO3 trong dung dịch X lần lượt là: A. 0,2M và 0,15M B. 0,2M và 0,3M C. 0,3M và 0,4M D. 0,4M và 0,3M
Đọc tiếp
Cho từ từ 450 ml dd HCl 1M vào 500 ml dung dịch X gồm Na2CO3 và NaHCO3 thì thu được 5,6 lít khí (đktc) và dung dịch Y. Cho dung dịch Y tác dụng với dung dịch Ba(OH)2 dư thì thu được 19,7 gam kết tủa. Nồng độ mol của Na2CO3 và NaHCO3 trong dung dịch X lần lượt là:
A. 0,2M và 0,15M
B. 0,2M và 0,3M
C. 0,3M và 0,4M
D. 0,4M và 0,3M
Cho từ từ 150 ml dung dịch HCl 1M vào 500 ml dung dịch A gồm Na2CO3 và NaHCO3 thì thu được 1,008 lít khí (đktc) và dung dịch B. Cho dung dịch B tác dụng với dung dịch Ba(OH)2 dư thì thu được 29,55 gam kết tủa. Nồng độ mol của Na2CO3 và NaHCO3 trong dung dịch A lần lượt là: A. 0,21M và 0,18M B. 0,18M và 0,26M C. 0,2M và 0,4M D. 0,21M và 0,32M
Đọc tiếp
Cho từ từ 150 ml dung dịch HCl 1M vào 500 ml dung dịch A gồm Na2CO3 và NaHCO3 thì thu được 1,008 lít khí (đktc) và dung dịch B. Cho dung dịch B tác dụng với dung dịch Ba(OH)2 dư thì thu được 29,55 gam kết tủa. Nồng độ mol của Na2CO3 và NaHCO3 trong dung dịch A lần lượt là:
A. 0,21M và 0,18M
B. 0,18M và 0,26M
C. 0,2M và 0,4M
D. 0,21M và 0,32M
Đáp án A
Có n H C l = 0 , 15 ; n C O 2 = 0 , 045 ; n B a C O 3 = 0 , 15
Gọi n N a 2 C O 3 = a ; n N a H C O 3 = b
Các phản ứng xảy ra theo thứ tự sau:
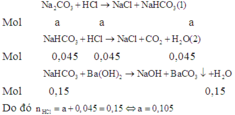
Áp dụng định luật bảo toàn nguyên tố C, ta có:
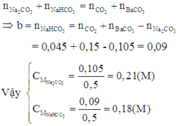
Đúng 0
Bình luận (0)
Cho từ từ 150 ml dung dịch HCl 1M vào 500 ml dung dịch A gồm Na2CO3 và NaHCO3 thì thu được 1,008 lít khí (điều kiện chuẩn) và dung dịch B. Cho dung dịch B tác dụng với dung dịch Ba(OH)2 dư thì thu được 29,55 gam kết tủa. Nồng độ mol của Na2CO3 và NaHCO3 trong dung dịch A lần lượt là: A. 0,18M và 0,26M B. 0,21M và 0,18M C. 0,21M và 0,32M D. 0,2M và 0,4M
Đọc tiếp
Cho từ từ 150 ml dung dịch HCl 1M vào 500 ml dung dịch A gồm Na2CO3 và NaHCO3 thì thu được 1,008 lít khí (điều kiện chuẩn) và dung dịch B. Cho dung dịch B tác dụng với dung dịch Ba(OH)2 dư thì thu được 29,55 gam kết tủa. Nồng độ mol của Na2CO3 và NaHCO3 trong dung dịch A lần lượt là:
A. 0,18M và 0,26M
B. 0,21M và 0,18M
C. 0,21M và 0,32M
D. 0,2M và 0,4M
Đáp án B
Ta có: nHCl = 0,15 mol; n C O 2 = 1,008/22,4 = 0,045 mol.
Giả sử ban đầu có x mol NaHCO3
CO32- + H+ → HCO3- (1)
HCO3-+ H+ → CO2+ H2O (2)
0,045 0,045 ←0,045
Theo PT (2): n H C O 3 - = n H + = n C O 2 = 0,045 mol
→ n H + PT1 = 0,15- 0,045= 0,105 mol
→ n C O 3 2 - PT1 = n H + = n H C O 3 - PT1 = 0,105 mol
→ n N a 2 C O 3 = n C O 3 2 - PT1= 0,105 mol
→ C M N a 2 C O 3 = 0,105/ 0,5 = 0,21M
Dung dịch Y chứa Na+, HCO3- dư:
x+0,105- 0,045 = x+0,06 mol
HCO3-+ OH- → CO32-+ H2O
Ba2++ CO32- → BaCO3
Ta thấy: n H C O 3 - = n C O 3 2 - = n B a C O 3 = 29,55/197 = 0,15 mol
→ x+0,06 = 0,15
→ x = 0,09 mol → C M N a H C O 3 = 0,09/ 0,5 = 0,18M
Đúng 0
Bình luận (0)
Cho từ từ 150 ml dd HCl 1M vào 500 ml dung dịch A gồm Na2CO3 và NaHCO3 thì thu được 1.008 lít khí (điều kiện tiêu chuẩn) và dung dịch B. Cho dung dịch B tác dụng với dung dịch Ba(OH)2 dư thì 2 thu được 29.55 gam kết tủa. Nồng độ mol của Na2CO3 và NaHCO3 trong dung dịch A lần lượt là: A. 0.18M và 0.26M B. 0.21M và 0.18M C. 0.21M và 0.32M D. 0.2M và 0.4M
Đọc tiếp
Cho từ từ 150 ml dd HCl 1M vào 500 ml dung dịch A gồm Na2CO3 và NaHCO3 thì thu được 1.008 lít khí (điều kiện tiêu chuẩn) và dung dịch B. Cho dung dịch B tác dụng với dung dịch Ba(OH)2 dư thì 2 thu được 29.55 gam kết tủa. Nồng độ mol của Na2CO3 và NaHCO3 trong dung dịch A lần lượt là:
A. 0.18M và 0.26M
B. 0.21M và 0.18M
C. 0.21M và 0.32M
D. 0.2M và 0.4M
250ml dung dịch X chứa Na2CO3 và NaHCO3 khi tác dụng với H2SO4 dư cho ra 2,24 lít CO2 (đktc). 250ml dung dịch X với CaCl2 dư cho ra 16 gam kết tủa. Nồng độ mol của Na2CO3 và NaHCO3 trong dung dịch X lần lượt là: A. 0,08M và 0,02M. B. 0,32M và 0,08M. C. 0,16M và 0,24M. D. 0,04M và 0,06M
Đọc tiếp
250ml dung dịch X chứa Na2CO3 và NaHCO3 khi tác dụng với H2SO4 dư cho ra 2,24 lít CO2 (đktc). 250ml dung dịch X với CaCl2 dư cho ra 16 gam kết tủa. Nồng độ mol của Na2CO3 và NaHCO3 trong dung dịch X lần lượt là:
A. 0,08M và 0,02M.
B. 0,32M và 0,08M.
C. 0,16M và 0,24M.
D. 0,04M và 0,06M
Cho 300ml dung dịch H3PO4 1M tác dụng với 300ml dung dịch Ca(OH)2 1M, sau phản ứng thu được m gam muối kết tủa và dung dịch B. Tính khối lượng kết tủa và nồng độ chất có trong B?
\(n_{Ca\left(OH\right)_2}=0,3\left(mol\right)\\ n_{H_3PO_4}=0,3\left(mol\right)\\ Vì:\dfrac{n_{Ca\left(OH\right)_2}}{n_{H_3PO_4}}=\dfrac{0,3}{0,3}=1\\ \Rightarrow Tạo.1.muối:CaHPO_4\\ Ca\left(OH\right)_2+H_3PO_4\rightarrow CaHPO_4+2H_2O\\ m_{\downarrow}=0\\ n_{CaHPO_4}=n_{Ca\left(OH\right)_2}=0,3\left(mol\right)\\ C_{MddCaHPO_4}=\dfrac{0,3}{0,3+0,3}=0,5\left(M\right)\)
Đúng 3
Bình luận (0)
Biết 3,36 lít khí CO2 (đktc) tác dụng vừa hết với 200ml dung dịch Ca(OH)2 sản phẩm là CaCO3 và H2O. a. Viết phương trình hóa học b. Tính nồng độ mol của dung dịch Ba(OH)2 đã dùng c. Tính khối lượng chất kết tủa thu được
a/ Ca(OH)2 + CO2--> CaCO3 + H2O
nCO2=3.36/22.4=0.15(mol)
nCO2=nCa(OH)2=0.15(mol)
200ml=0.2l
b/CMCa(OH)2= 0.15/0.2=0.75(M)
c/nCaCO3=nCO2=0.15(mol)
mCaCO3= 0.15 x 106=15.9(g)
Đúng 1
Bình luận (0)
Cho 2,24 lít khí CO2 (đktc) tác dụng vừa hết 200ml dung dịch Ca(OH)2 thu được muối trung hoà a) Tính nồng độ mol dung dịch Ca(OH)2 đax dùng
b) Tính khối lượng kết tủa thu được
a/ PTHH: CO2 + Ca(OH)2 ===> CaCO3+ H2O
nCO2 = 2,24 / 22,4 = 0,1 mol
=> nCa(OH)2 = nCaCO3 = nCO2 = 0,1 mol
=> CM(CaOH)2 = 0,1 / 0,2 = 0,5M
b/ => mCaCO3 = 0,1 x 100 = 10 gam
Đúng 0
Bình luận (0)