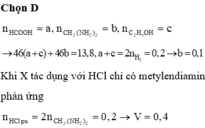Thể tích h2 thu được khi hòa tan 13,8 gam etanol (than) trong lượng natri dư là

Những câu hỏi liên quan
Hòa tan 13,8 gam Natri (Na)/với 3lit H20 a.Viết PTHH b. tính thể tích H2 thu đc sau p.ứng c.tính nồng độ mol của dungdich thu được sau phản ứng
a)\(PTHH:2Na+2H_2O\xrightarrow[]{}2NaOH+H_2\)
b) Số mol của Na là:
\(n_{Na}=\dfrac{m_{Na}}{M_{Na}}=\dfrac{13,8}{23}=0,6\left(mol\right)\)
\(PTHH:2Na+2H_2O\xrightarrow[]{}2NaOH+H_2\)
Tỉ lệ : 2 2 2 1 (mol)
Số mol:0,6 0,6 0,6 0,3 (mol)
Thể tích H2 thu được là:
\(V_{H_2}=n_{H_2}.22,4=0,3.22,4=6,72\left(l\right)\)
c) Nồng độ mol dung dịch sau phản ứng là:
\(C_{MNaOH}=\dfrac{n_{NaOH}}{V_{dd}}=\dfrac{0,6}{3}=0,2M\)
Đúng 1
Bình luận (0)
Cho 13,8 gam hỗn hợp gồm axit fomic và etanol phản ứng hết với Na dư, thu được V lít khi H2 (đktc). Giá trị của V là A. 6,72 B. 4,48 C. 3,36 D. 7,84
Đọc tiếp
Cho 13,8 gam hỗn hợp gồm axit fomic và etanol phản ứng hết với Na dư, thu được V lít khi H2 (đktc). Giá trị của V là
A. 6,72
B. 4,48
C. 3,36
D. 7,84
Đáp án : C
nhh = 13,8 : 46 = 0,3 mol
nH2 = ½ nhh = 0,15 mol
=> V = 3,36 lít
Đúng 0
Bình luận (0)
Hiđro hóa hoàn toàn anđehit acrylic bằng lượng dư H2 (xúc tác Ni, nhiệt độ) thu được ancol X. Hòa tan hết lượng X vào 13,5 gam nước thu được dung dịch Y. Cho natri dư vào dung dịch Y thu được 11,2 khí H2 ( đktc). Nồng độ phần trăm chất X trong dung dịch Y là A. 52,63% B. 51,79% C. 81,63% D. 81,12%
Đọc tiếp
Hiđro hóa hoàn toàn anđehit acrylic bằng lượng dư H2 (xúc tác Ni, nhiệt độ) thu được ancol X. Hòa tan hết lượng X vào 13,5 gam nước thu được dung dịch Y. Cho natri dư vào dung dịch Y thu được 11,2 khí H2 ( đktc). Nồng độ phần trăm chất X trong dung dịch Y là
A. 52,63%
B. 51,79%
C. 81,63%
D. 81,12%
Hòa tan hoàn toàn 2,3 gam natri vào nước.
a. Nêu hiện tượng quan sát được. Viết PTHH.
b. Tính thể tích khí H2 thu được ở điều kiện tiêu chuẩn.
c. Tính khối lượng natri hiđroxit thu được.
d. Toàn bộ khí hiđro thu được ở trên cho tác dụng hết với 8,1 gam kẽm oxit đun nóng. Tính khối lượng chất rắn thu được.
Ta có: \(n_{Na}=\dfrac{2,3}{23}=0,1\left(mol\right)\)
a, Hiện tượng: Na nóng chảy thành giọt tròn có màu trắng chuyển động nhanh trên mặt nước rồi tan dần, có khí thoát ra.
PT: \(2Na+2H_2O\rightarrow2NaOH+H_2\)
____0,1_____________0,1____0,05 (mol)
b, VH2 = 0,05.22,4 = 1,12 (l)
c, mNaOH = 0,1.40 = 4 (g)
d, Ta có: \(n_{ZnO}=\dfrac{8,1}{81}=0,1\left(mol\right)\)
PT: \(ZnO+H_2\underrightarrow{t^o}Zn+H_2O\)
Xét tỉ lệ: \(\dfrac{0,1}{1}>\dfrac{0,05}{1}\), ta được ZnO dư.
Theo PT: \(n_{ZnO\left(pư\right)}=n_{Zn}=n_{H_2}=0,05\left(mol\right)\)
⇒ nZnO (dư) = 0,05 (mol)
⇒ m chất rắn = mZn + mZnO (dư) = 0,05.65 + 0,05.81 = 7,3 (g)
Bạn tham khảo nhé!
Đúng 2
Bình luận (4)
hòa tan hoàn toàn một hỗn hợp có chứ 13,8 gam kim loại natri và 13,7 gam kim loại bari vào cốc chứa 500ml nước .Sau pảnh ứng thu được dung dịch chứa Natri Hidroxt, Bari hidroxit và khí hidro
a. viết pt phản ứng hóa học
b.tính thể tích khí hidro sinh ra
c. nếu cho mẩu giấy quỳ tím vào dung dịch thu được sau phản ứng thì giấy quỳ tím hóa màu gì?
a, PT: \(2Na+2H_2O\rightarrow2NaOH+H_2\)
\(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
b, Ta có: \(\left\{{}\begin{matrix}n_{Na}=\dfrac{13,8}{23}=0,6\left(mol\right)\\\end{matrix}\right.\)
\(n_{Ba}=\dfrac{13,7}{137}=0,1\left(mol\right)\)
Theo PT: \(n_{H_2}=\dfrac{1}{2}n_{Na}+n_{Ba}=0,4\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,4.22,4=8,96\left(l\right)\)
c, Quỳ tím chuyển xanh.
Bạn tham khảo nhé!
Đúng 2
Bình luận (1)
a) PTHH: \(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\uparrow\)
\(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\uparrow\)
b) Theo PTHH: \(n_{H_2}=\dfrac{1}{2}n_{Na}+n_{Ba}=\dfrac{1}{2}\cdot\dfrac{13,8}{23}+\dfrac{13,7}{137}=0,4\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,4\cdot22,4=8,96\left(l\right)\)
c) Quỳ tím hóa xanh
Đúng 1
Bình luận (1)
Cho 13,8 gam hỗn hợp X gồm axit fomic, metylenđiamin và etanol phản ứng hết với Na dư thu được 2,24 lít
H
2
(đktc). Mặt khác 13,8 gam X tác dụng vừa hết với V lít dung dịch HCl 0,5M. Giá trị của V là: A. 0,1 B. 0,2 C. 0,3 D. 0,4
Đọc tiếp
Cho 13,8 gam hỗn hợp X gồm axit fomic, metylenđiamin và etanol phản ứng hết với Na dư thu được 2,24 lít H 2 (đktc). Mặt khác 13,8 gam X tác dụng vừa hết với V lít dung dịch HCl 0,5M. Giá trị của V là:
A. 0,1
B. 0,2
C. 0,3
D. 0,4
Hòa tan hoàn toàn 13,8 gam hỗn hợp A gồm Al và Fe bằng axit clohiđric dư sau phản ứng thu được dung dịch A 10,08 lít H2 (ở đktc).a/ Tính % mỗi chất có trong hỗn hợp A. b/ Tính khối lượng axit ban đầu biết axit lấy dư 20%.c/ Tính khối lượng muối tạo thành bằng nhiều cách.
Đọc tiếp
Hòa tan hoàn toàn 13,8 gam hỗn hợp A gồm Al và Fe bằng axit clohiđric dư sau phản ứng thu được dung dịch A 10,08 lít H2 (ở đktc).
a/ Tính % mỗi chất có trong hỗn hợp A.
b/ Tính khối lượng axit ban đầu biết axit lấy dư 20%.
c/ Tính khối lượng muối tạo thành bằng nhiều cách.
Cho 13,8 gam hỗn hợp X gồm axit fomic, metylenđiamin và etanol phản ứng hết với Na dư, thu được 2,24 lít khí
H
2
(đktc). Mặt khác 13,8 gam X tác dụng vừa hết với V lít dung dịch HCl 0,5M. Giá trị của V là A. 0,1. B. 0,2. C. 0,3. D. 0,4
Đọc tiếp
Cho 13,8 gam hỗn hợp X gồm axit fomic, metylenđiamin và etanol phản ứng hết với Na dư, thu được 2,24 lít khí H 2 (đktc). Mặt khác 13,8 gam X tác dụng vừa hết với V lít dung dịch HCl 0,5M. Giá trị của V là
A. 0,1.
B. 0,2.
C. 0,3.
D. 0,4
Cho 14 gam hỗn hợp X gồm phenol và etanol phản ứng hoàn toàn với natri (dư), thu được 2,24 lít khí H2 (đktc). Khối lượng phenol trong hỗn hợp trên là:
A. 4,6 B. 9,2 C. 4,7 D. 9,4
Gọi $n_{phenol} = a(mol) ; n_{etanol} = b(mol)$
Suy ra: $94a + 46b = 14(1)$
$C_6H_5OH + Na \to C_6H_5ONa +\dfrac{1}{2}H_2$
$C_2H_5OH + Na \to C_2H_5ONa + \dfrac{1}{2}H_2$
$n_{H_2} = 0,5a + 0,5b = \dfrac{2,24}{22,4} = 0,1(mol)$
Từ (1)(2) suy ra a = b = 0,1
$m_{phenol} = 0,1.94 = 9,4(gam)$
Đáp án D
Đúng 2
Bình luận (0)