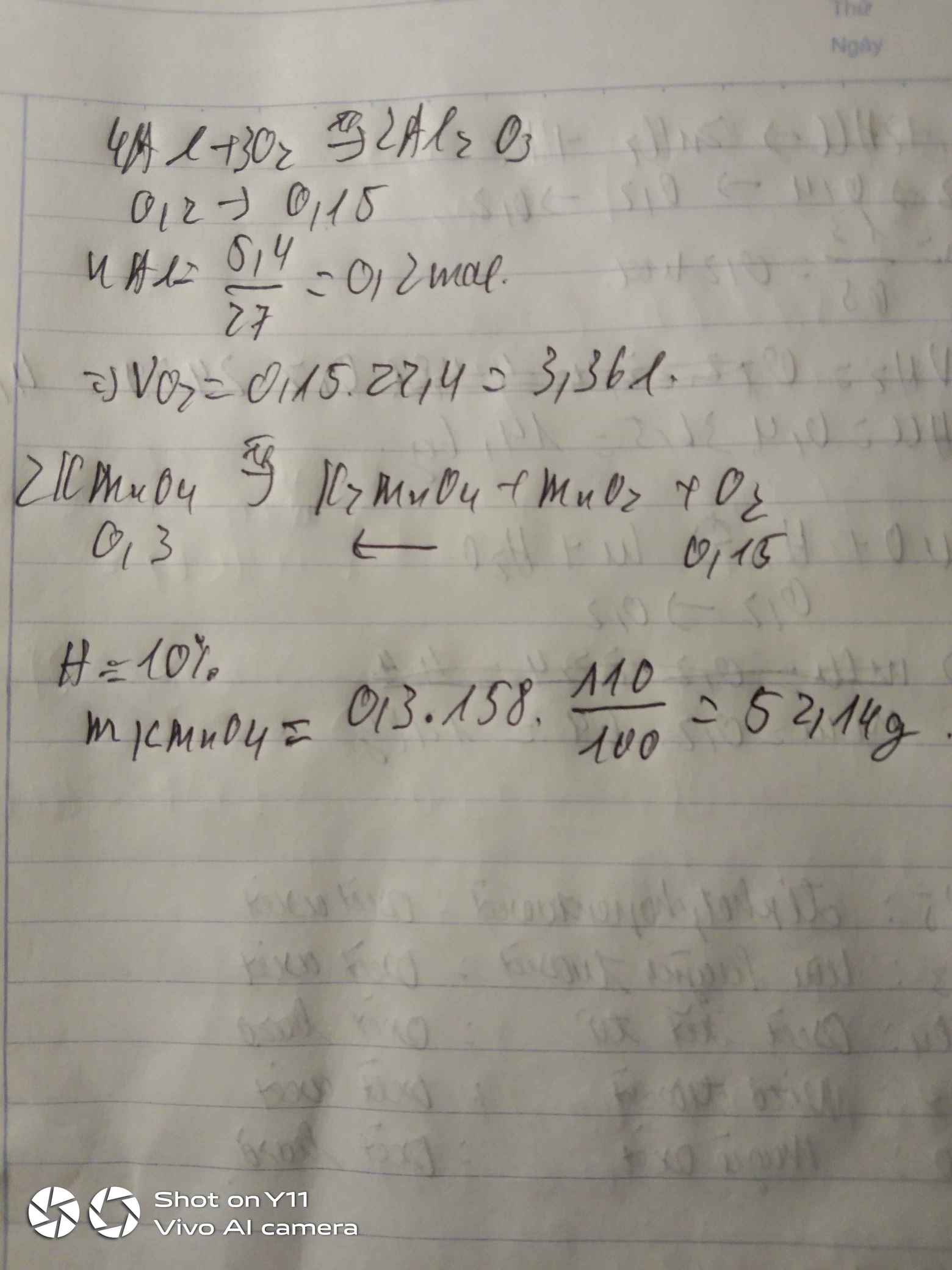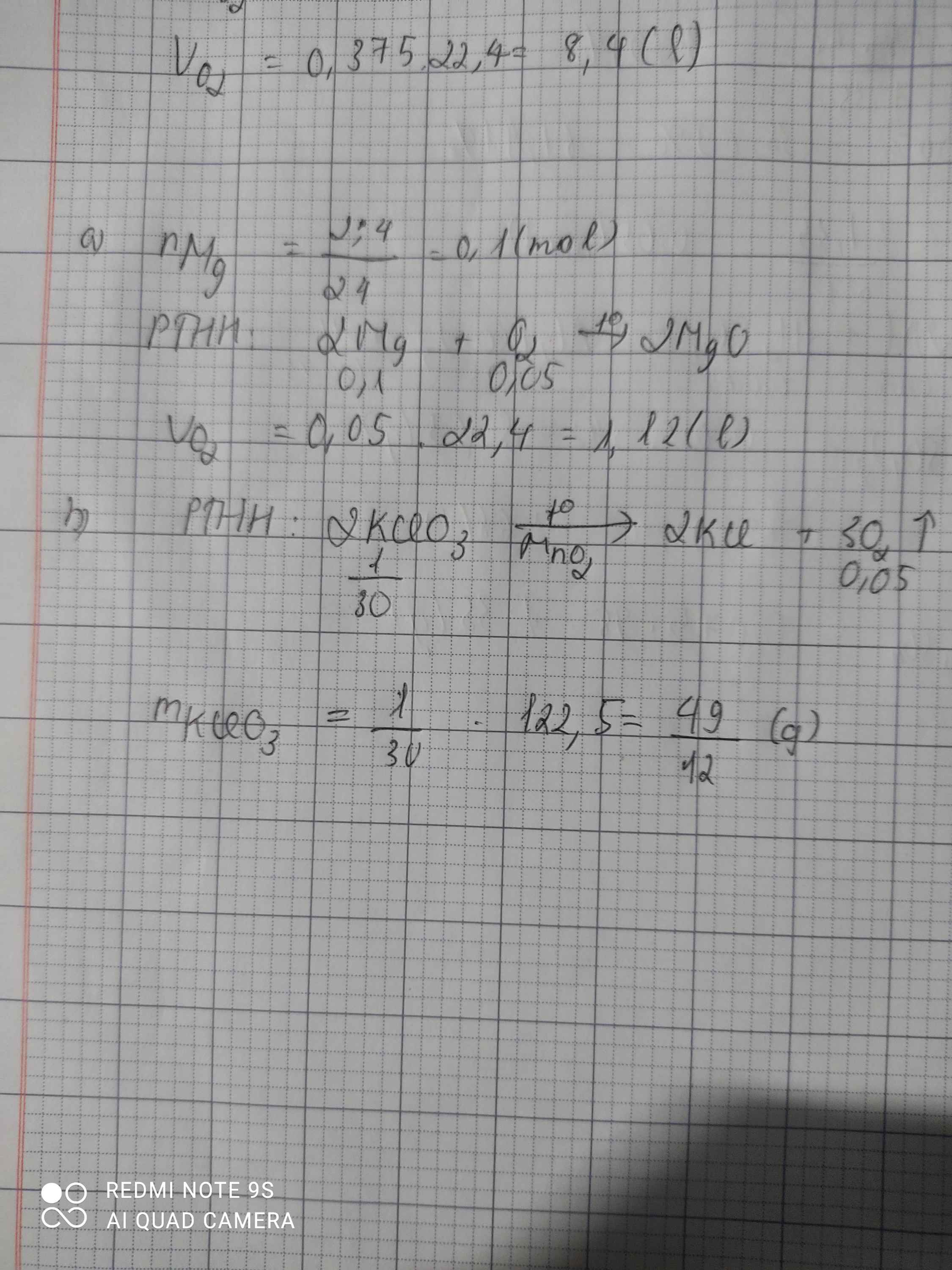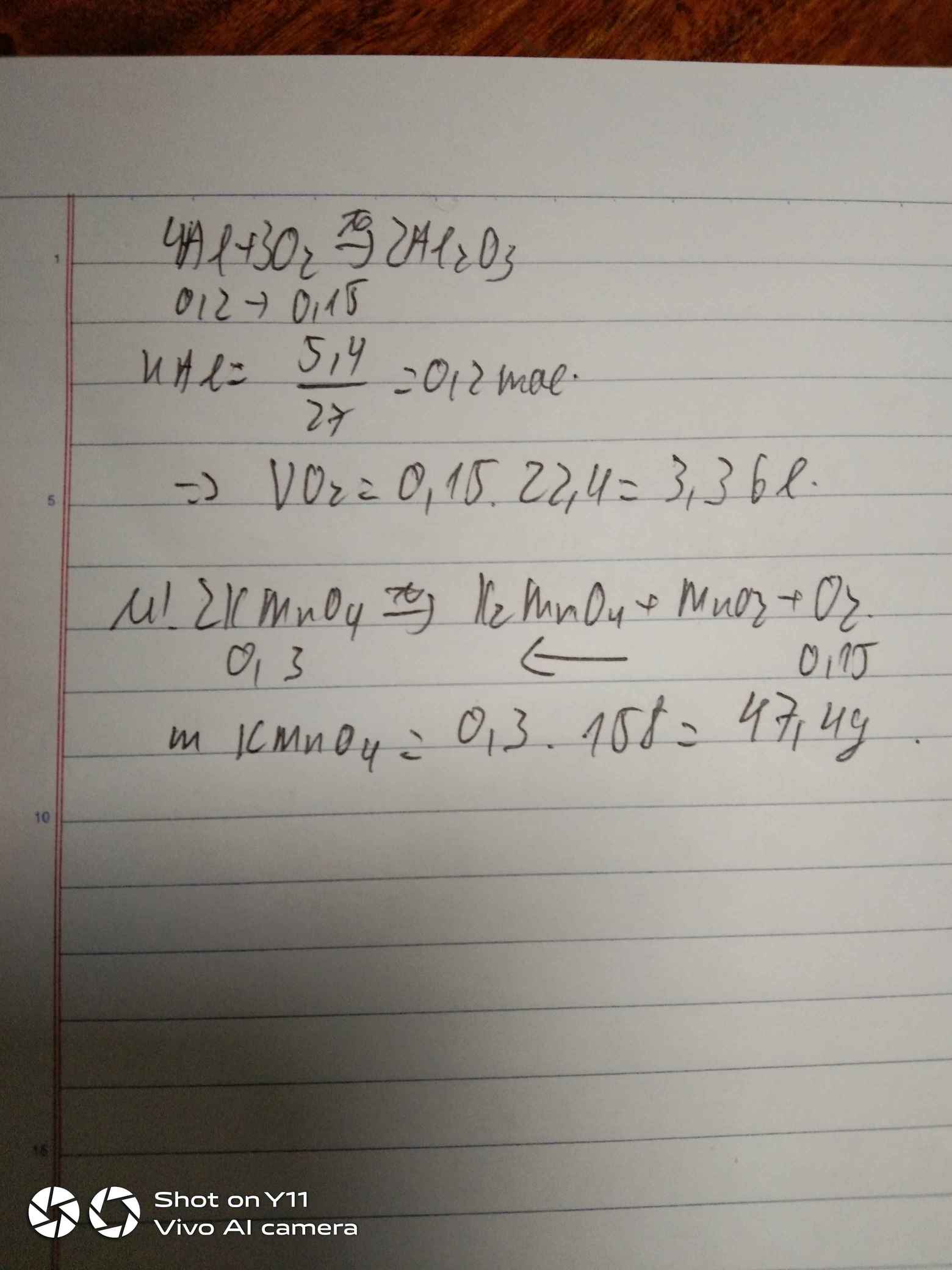Đốt cháy hoàn toàn 5.4g bột nhôm a. Tính thể tích O2 cần dùng ở đktc b. Tính số g KClO3 cần dùng để điều chế lượng oxi trên. Biết trong quá trình điều chế hao hụt 10% và có xúc tác MnO2

Những câu hỏi liên quan
Đốt cháy hoàn toàn 5,4g nhôm. Tính :
a. Thể tích khí O2 (đktc) cần dùng ?
b. Số gam KMnO4 cần dùng để điều chế lượng khí O2 trên giả sử quá trình thu khí oxi bị hao hụt 10% ?
\(n_{Al}=\dfrac{5.4}{27}=0,2mol\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
0,2 0,15 0,1
a)\(V_{O_2}=0,15\cdot22,4=3,36l\)
b)\(n_{O_2}=0,15\cdot10\%=0,015mol\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
0,03 0,015
\(m_{KMnO_4}=0,03\cdot158=4,74g\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 3,6 gam magie trong khí oxi trên thì khối lượng kali clorat cần dùng.
A. Tính thể tích khí oxi (đktc) cần dùng?
B. Nếu dùng dịch KCLO3(có xúc tác MnO2) để điều chế lượng khí oxi trên thì khối lượng kali clorat cần dùng là bao nhiêu?
(O=16,CL=35,5,K=39,Mn=55)
2Mg+O2-to>2MgO
0,15---0,075 mol
2KClO3-to->2KCl+3O2
0,05-----------------------0,075
n Mg=\(\dfrac{3,6}{24}\)=0,15 mol
=>VO2=0,075.22,4=1,68l
=>m KClO3=0,05.122,5=6,125g
Đúng 3
Bình luận (0)
a. \(n_{Mg}=\dfrac{3.6}{24}=0,15\left(mol\right)\)
PTHH : 2Mg + O2 ----to----> 2MgO
0,15 0,075
\(V_{O_2}=0,075.22,4=1,68\left(l\right)\)
b. PTHH : 2KClO3 \(\xrightarrow[MnO_2]{t^o}\) 2KCl + 3O2
0,05 0,075
\(m_{KClO_3}=0,05.122,5=6,125\left(g\right)\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 5,4 g kim loại nhôm Al trong khí oxi. a. Tính thể tích khí oxi (đktc) cần dùng cho phản ứng. b. Tính khối lượng KClO3 cần dùng để điều chế lượng oxi trên.
a) $n_{Al} = \dfrac{5,4}{27} = 0,2(mol)$
$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
Theo PTHH : $n_{O_2} = \dfrac{3}{4}n_{Al} = 0,15(mol)$
$V_{O_2} = 0,15.22,4 = 3,36(lít)$
b) $2 KClO_3 \xrightarrow{t^o} 2KCl + 3O_2$
$n_{KClO_3} = \dfrac{2}{3}n_{O_2} = 0,1(mol)$
$m_{KClO_3} = 0,1.122,5 = 12,25(gam)$
Đúng 1
Bình luận (0)
\(n_{Al}=\dfrac{m}{M}=\dfrac{5,4}{27}=0,2\left(mol\right)\\ PTHH:4Al+3O_2-^{t^o}>2Al_2O_3\)
tỉ lệ: 4 : 3 : 2
n(mol) 0,2---->0,15---->0,1
\(V_{O_2\left(dktc\right)}=n\cdot22,4=0,15\cdot22,4=3,36\left(l\right)\\ PTHH:2KClO_3-^{t^o}>2KCl+3O_2\)
tỉ lệ: 2 : 2 : 3
n(mol) 0,1<-------------------------0,15
\(m_{KClO_3}=n\cdot M=0,1\cdot\left(39+35,5+16\cdot3\right)=12,25\left(g\right)\)
Đúng 1
Bình luận (0)
4Al+3O2-to>2Al2O3
0,2---0,15------0,1 mol
n Al=0,2 mol
VO2=0,15.22,4=3,36l
b) 2KClO3-to>2KCl +3O2
0,1---------------------0,15 mol
->m KClO3=0,1.122,5g
#yT
Đúng 0
Bình luận (0)
bột nhôm cháy trong oxi tạo ra nhôm oxit (al2o3)
a) viết pthh
b) tính thể tích oxi (ở đktc) cần dùng để đốt cháy hoàn toàn 0.54 gam bột nhôm
c) tính khối lượng kmno4 cần dùng để điều chế lượng oxi dùng cho phản ứng trên
Đốt cháy hoàn toàn 2,4g magie (Mg) trong khí oxi thu được magie oxit (MgO)
a) Tính thể tích khí oxi cần dùng (thể tích khí đo ở đktc)
b) Tính số gam KClO3 cần dùng để điều chế lượng oxi trên
\(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\\ a,2Mg+O_2\rightarrow\left(t^o\right)2MgO\\ n_{O_2}=\dfrac{0,1}{2}=0,05\left(mol\right)\\ V_{O_2\left(đktc\right)}=0,05.22,4=1,12\left(l\right)\\ b,2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\\ n_{KClO_3}=\dfrac{0,05.2}{3}=\dfrac{1}{30}\left(mol\right)\\ \Rightarrow m_{KClO_3}=\dfrac{122,5}{30}=\dfrac{49}{12}\left(g\right)\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 5,4 gam nhôm. A. Tính thể tích khí oxi cần dùng (đktc) B. Tính số gam KMnO4 cần dùng để điều chế lượng oxi trên.
nAl = 5,4/27 = 0,2 (mol)
PTHH: 4Al + 3O2 -> (t°) 2Al2O3
Mol: 0,2 ---> 0,15
VO2 = 0,15 . 22,4 = 3,36 (l)
PTHH: 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
nKMnO4 = 0,15 . 2 = 0,3 (mol)
mKMnO4 = 0,3 . 158 = 47,4 (g)
Đúng 3
Bình luận (1)
đốt cháy hoàn toàn 3,6g magie trong khí oxi
a)tính thể tích khí oxi cần dùng
b)nếu dùng kali clorat (có xúc tác Mno2)để điều chế được khí oxi trên thì khối lượng kali clorat cần dùng là bao nhiêu
Theo gt ta có: $n_{Mg}=0,15(mol)$
a, $2Mg+O_2\rightarrow 2MgO$
Ta có: $n_{O_2}=0,5.n_{Mg}=0,075(mol)\Rightarrow V_{O_2}=1,68(l)$
b, $2KClO_3\rightarrow 2KCl+3O_2$ (đk: nhiệt độ, MnO2)
Ta có: $n_{KClO_3}=\frac{2}{3}.n_{O_2}=0,05(mol)\Rightarrow m_{KClO_3}=6,125(g)$
Đúng 0
Bình luận (0)
\(n_{Mg}=\dfrac{3.6}{24}=0.15\left(mol\right)\)
\(2Mg+O_2\underrightarrow{t^0}2MgO\)
\(0.15......0.075......0.15\)
\(V_{O_2}=0.075\cdot22.4=1.68\left(l\right)\)
\(2KClO_3\underrightarrow{t^0}2KCl+3O_2\)
\(0.05.......................0.075\)
\(m_{KClO_3}=0.05\cdot122.5=6.125\left(g\right)\)
Đúng 0
Bình luận (0)
Theo gt ta có: nMg=0,15(mol)nMg=0,15(mol)
a, 2Mg+O2→2MgO2Mg+O2→2MgO
Ta có: nO2=0,5.nMg=0,075(mol)⇒VO2=1,68(l)nO2=0,5.nMg=0,075(mol)⇒VO2=1,68(l)
b, 2KClO3→2KCl+3O22KClO3→2KCl+3O2 (đk: nhiệt độ, MnO2)
Ta có: nKClO3=2/3.nO2=0,05(mol)⇒mKClO3=6,125(g)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
3. Đốt cháy hoàn toàn 5,4g nhôm. Tính : a. thể tích khí O2 (đktc) cần dùng ? b. số gam KMnO4 cần dùng để điều chế lượng khí O2 trên ?
PTHH: \(4Al+3O_2\xrightarrow[]{t^o}2Al_2O_3\)
\(2KMnO_4\xrightarrow[]{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
Ta có: \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}n_{O_2}=0,15\left(mol\right)\\n_{KMnO_4}=0,3\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{O_2}=0,15\cdot22,4=3,36\left(l\right)\\m_{KMnO_4}=0,3\cdot158=47,4\left(g\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)
bài 4: đốt cháy hoàn toàn 5,4g nhôm. Tính :
a) thể tích O2(đktc) cần dùng ?
b) số gam kMnO4 cần dùng để điều chế lượng khí O2 trên
\(n_{Al}=\dfrac{5.4}{27}=0.2\left(mol\right)\)
\(4Al+3O_2\underrightarrow{^{^{t^0}}}2Al_2O_3\)
\(0.2..........0.15\)
\(V_{O_2}=0.15\cdot22.4=3.36\left(l\right)\)
\(2KMnO_4\underrightarrow{^{^{t^0}}}K_2MnO_4+MnO_2+O_2\)
\(0.3...............................................0.15\)
\(m_{KMnO_4}=0.3\cdot158=47.4\left(g\right)\)
Đúng 4
Bình luận (0)