cho 4g canxi tác dụng hoàn toàn với 1,68l khí oxi (đktc) thu được canxioxit. nếu lấy lượng canxioxit trên cho vào nước thì thu được bao nhiêu gam canxihidroxit

Những câu hỏi liên quan
Đem đốt cháy hoàn toàn một lượng Canxi trong bình khí Oxi, sau khi canxi cháy xong thu được 5,6 g bột Canxioxit bằng 7/5 khối lượng Canxi đã bị đốt .
a) Tính khối lượng canxi bị đốt cháy?
b) Mấy lit Oxi tham gia phản ứng ; biết 4g khí Oxi ở điều kiện thường có thể tích 3lit?
c) Đã lấy bao nhiêu gam khí Oxi trong bình, biết rằng Oxi có lấy dư 25% lượng phản ứng .
Cho 5,6 gam sắt vào thu được dung dich khí HCl dư thu được V lít khí hiđrô ở (đktc)
a. Xác định giá trị V
b. nếu cho lượng nước hiđrô trên tác dụng với 6,72 lít khí oxi (đktc) thì lượng nước thu được là bao nhiêu ?
\(a) Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = n_{Fe} = \dfrac{5,6}{56} = 0,1(mol)\\ \Rightarrow V_{H_2} = 0,1.22,4 = 2,24(lít)\\ b) n_{O_2} = \dfrac{6,72}{22,4} = 0,3(mol)\\ 2H_2 + O_2 \xrightarrow{t^o} 2H_2O\\ \dfrac{n_{H_2}}{2} = 0,05 < \dfrac{n_{O_2}}{1} = 0,3 \to O_2\ dư\\ n_{H_2O} = n_{H_2} = 0,1(mol) \Rightarrow m_{H_2O} = 0,1.18 = 1,8(gam)\)
Đúng 1
Bình luận (0)
hoà tan hoàn toàn 12 gam canxi với nước thu được bazo canxi hidroxit và khí hidro a) Tính thể tích chất khí thu được (đktc)? b) tính khối lượng bazo thu được sau phản ứng? c) đem toàn bộ chất khí thu được tác dụng với 8,4 gam sắt từ oxi thì thu được bao nhiêu gam chất rắn?
a, \(n_{Ca}=\dfrac{12}{40}=0,3\left(mol\right)\)
PT: \(Ca+2H_2O\rightarrow Ca\left(OH\right)_2+H_2\)
Theo PT: \(n_{H_2}=n_{Ca}=0,3\left(mol\right)\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
b, \(n_{Ca\left(OH\right)_2}=n_{Ca}=0,3\left(mol\right)\Rightarrow m_{Ca\left(OH\right)_2}=0,2.74=22,2\left(g\right)\)
c, \(n_{Fe_3O_4}=\dfrac{8,4}{232}=\dfrac{21}{580}\left(mol\right)\)
PT: \(Fe_3O_4+4H_2\underrightarrow{t^o}3Fe+4H_2O\)
Xét tỉ lệ: \(\dfrac{\dfrac{21}{580}}{1}< \dfrac{0,3}{4}\), ta được H2 dư.
Theo PT: \(n_{Fe}=3n_{Fe_3O_4}=\dfrac{63}{580}\left(mol\right)\Rightarrow m_{cr}=m_{Fe}=\dfrac{63}{580}.56=\dfrac{882}{145}\left(g\right)\)
Đúng 1
Bình luận (1)
Cho 12.25 gam kali clorat nhiệt phân hoàn toàn
a. Tính thể tích oxi thu được .
b. Nếu cho lượng oxi trên tác dụng với 11.2 gam sắt thì khối lượng oxit sắt từ thu được là bao nhiêu?
Xem chi tiết
a/ Ta có: \(n_{KClO_3}=\dfrac{12.25}{122.5}=0.1\left(mol\right)\)
PTHH:
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\uparrow\)
2 3
0.1 x
\(=>x=\dfrac{0.1\cdot3}{2}=0.15=n_{O_2}\)
\(=>V_{O_2}=0.15\cdot22.4=3.36\left(l\right)\)
Đúng 1
Bình luận (0)
PTHH: \(KClO_3\underrightarrow{t^o}KCl+\dfrac{3}{2}O_2\)
a) Ta có: \(n_{KClO_3}=\dfrac{12,25}{122,5}=0,1\left(mol\right)\)
\(\Rightarrow n_{O_2}=0,15\left(mol\right)\) \(\Rightarrow V_{O_2}=0,15\cdot22,4=3,36\left(l\right)\)
b) PTHH: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
Ta có: \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{3}< \dfrac{0,15}{2}\) \(\Rightarrow\) Oxi còn dư, Fe p/ứ hết
\(\Rightarrow n_{Fe_3O_4}=\dfrac{1}{15}\left(mol\right)\) \(\Rightarrow m_{Fe_3O_4}=\dfrac{1}{15}\cdot232\approx15,47\left(g\right)\)
Đúng 1
Bình luận (0)
\(n_{KClO_3}=\dfrac{m_{KClO_3}}{M_{KClO_3}}=\dfrac{12,25}{122,5}=0,1\left(mol\right)\\ PTHH:2KClO_3\underrightarrow{t^o}2KCl+3O_2\\ n_{O_2}=\dfrac{3}{2}n_{KClO_3}=\dfrac{3}{2}\cdot0,1=0,15\left(mol\right)\\ V_{O_2\left(ĐKTC\right)}=n_{O_2}\cdot22,4=0,15\cdot22,4=3,36\left(l\right)\\ n_{Fe}=\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{11,2}{56}=0,2\left(mol\right)\\ PTHH:3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\\ \dfrac{n_{Fe}}{n_{O_2}}=2>\dfrac{3}{2}\Rightarrow Fe\text{ dư, bài toán tính theo lượng }O_2\\ m_{Fe_3O_4}=n_{Fe_3O_4}\cdot M_{Fe_3O_4}=0,075\cdot232=17,4\left(g\right)\)
Đúng 0
Bình luận (2)
giúp mik mik cần gấpĐốt cháy hoàn toàn m gam hỗn hợp khí A gồm C2H4 và C2H6 bằng lượng khí oxi vừa đủ. Sau phản ứng thu được 8,96 lit CO2(đktc) và a gam nước. Mặt khác nếu lấy m gam hỗn hợp trên cho tác dụng với dung dịch brom thì thấy làm mất màu vừa đủ 1 lit dung dịch Br2 0,05M. a) Viết các phương trình phản ứng xảy ra và tính a. b) Lấy m gam hỗn hợp A cho tác dụng với H2 (dư) xúc tác Ni thu được hỗn hợp khí B. Cho toàn bộ hỗn hợp B qua dung dịch Br2 thấy làm mất màu vừa đủ 200ml dung dịch bro...
Đọc tiếp
giúp mik mik cần gấp
Đốt cháy hoàn toàn m gam hỗn hợp khí A gồm C2H4 và C2H6 bằng lượng khí oxi vừa đủ. Sau phản ứng thu được 8,96 lit CO2(đktc) và a gam nước. Mặt khác nếu lấy m gam hỗn hợp trên cho tác dụng với dung dịch brom thì thấy làm mất màu vừa đủ 1 lit dung dịch Br2 0,05M. a) Viết các phương trình phản ứng xảy ra và tính a. b) Lấy m gam hỗn hợp A cho tác dụng với H2 (dư) xúc tác Ni thu được hỗn hợp khí B. Cho toàn bộ hỗn hợp B qua dung dịch Br2 thấy làm mất màu vừa đủ 200ml dung dịch brom 0,05M. Tính hiệu suất phản ứng hiđro hóa hỗn hợp A trên.
cho m gam kim loại Ca tác dụng hết với khí oxi thu được canxioxit. Cho toàn bộ lượng oxit này tác dụng hết với nước sinh ra 14,8 gam canxi hidroxit. Tính giá trị m
nca(oh)2=14,8/74=0,2mol
pt(1): 2Ca +O2\(\underrightarrow{t^o}\)2CaO
Pt(2):CaO+H2O\(\underrightarrow{ }\)Ca(OH)2
npứ:0,2 \(\leftarrow\)0,2
theo pt(1) nca=ncao\(\Rightarrow\)nca=ncao=0,2mol
\(\Rightarrow\)mca=0,2.40=8g
Đúng 0
Bình luận (0)
2Ca + O2 --to--➢ 2CaO (1)
CaO + H2O → Ca(OH)2 (2)
\(n_{Ca\left(OH\right)_2}=\dfrac{14,8}{74}=0,2\left(mol\right)\)
Theo PT2: \(n_{CaO}=n_{Ca\left(OH\right)_2}=0,2\left(mol\right)\)
\(n_{CaO\left(2\right)}=n_{CaO\left(1\right)}\)
Theo PT1: \(n_{Ca}=n_{CaO}=0,2\left(mol\right)\)
\(\Rightarrow m=m_{Ca}=0,2\times40=8\left(g\right)\)
Đúng 0
Bình luận (0)
Bài 1 : Cho m gam Na2CO3 tác dụng với dung dịch CaCl2 lấy dư thu được 20 gam kết tủa . Giá trị của m bao nhiêu ?
Bài 2 : Đốt cháy hoàn toàn 3,6 gam cacbon bằng lượng oxi lấy dư thu được V lít (đktc) khí CO2 . Giá trị của V là bao nhiêu ?
Bài 3 : Sục hết 1,568 lít khí CO2 (đktc) vào 900 ml dung dịch NaOH 0,1M thu được dung dịch A . Cho 100ml dung dịch B gồm BaCl2 0,4M và Ba(OH)2 xM vào dung dịch A được 4,925 gam kết tủa vào dung dịch C . Giá trị của x bằng
Đọc tiếp
Bài 1 : Cho m gam Na2CO3 tác dụng với dung dịch CaCl2 lấy dư thu được 20 gam kết tủa . Giá trị của m bao nhiêu ?
Bài 2 : Đốt cháy hoàn toàn 3,6 gam cacbon bằng lượng oxi lấy dư thu được V lít (đktc) khí CO2 . Giá trị của V là bao nhiêu ?
Bài 3 : Sục hết 1,568 lít khí CO2 (đktc) vào 900 ml dung dịch NaOH 0,1M thu được dung dịch A . Cho 100ml dung dịch B gồm BaCl2 0,4M và Ba(OH)2 xM vào dung dịch A được 4,925 gam kết tủa vào dung dịch C . Giá trị của x bằng
Em đăng tách câu hỏi ra nhé!
---
Bài 1:
Na2CO3 + CaCl2 -> 2 NaCl + CaCO3
m(kt)=mCaCO3=20(g)
-> nCaCO3=0,2(mol)
-> nNa2CO3=0,2(mol)
=> m= mNa2CO3=0,2.106=21,2(g)
Bài 2:
nC=3,6/12=0,3(mol)
C+ O2 -to-> CO2
nCO2=nC=0,3(mol)
=>V=V(CO2,đktc)=0,3.22,4=6,72(l)
Đúng 1
Bình luận (0)
Hoà tan hoàn toàn hỗn hợp X gồm 3 kim loại kiềm vào nước thu được 4,48 lít khí H2 (đktc). Nếu cũng cho lượng X như trên tác dụng với O2 dư thì thu được 3 oxit và thấy khối lượng chất rắn tăng m gam. Giá trị của m là: A. 3,2. B. 1,6. C. 4,8. D. 6,4.
Đọc tiếp
Hoà tan hoàn toàn hỗn hợp X gồm 3 kim loại kiềm vào nước thu được 4,48 lít khí H2 (đktc). Nếu cũng cho lượng X như trên tác dụng với O2 dư thì thu được 3 oxit và thấy khối lượng chất rắn tăng m gam. Giá trị của m là:
A. 3,2.
B. 1,6.
C. 4,8.
D. 6,4.
Đáp án A
Vì khối lượng hỗn hợp X sử dụng ở hai trường hợp là như nhau và hóa trị của các kim loại kiềm luôn là I không đổi nên số mol electron trao đổi ở hai trường hợp bằng nhau.
Áp dụng định luật bảo toàn mol electron ta có:
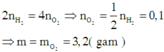
Đúng 0
Bình luận (0)
Nhiệt phân hoàn toàn m (g) KMnO4 thu được 3,36 lít khí O2(đktc).
a. Tìm m?
b. Nếu cho lượng oxi trên tác dụng với 8,96 lít khí H2. Tính khối lượng nước tạo thành. Biết phản ứng xảy ra hoàn toàn
a)nO2=\(\dfrac{3.36}{22.4}\)=0,15(mol)
2KMnO4(to)→K2MnO4+MnO2+O2
Theo PT: nKMnO4=2nO2=0,3(mol)
→m=mKMnO4=0,3.158=47,4(g)
b)nH2=\(\dfrac{8.96}{22.4}\)=0,4(mol)
2H2+O2(to)→2H2O
Vì \(\dfrac{nH_2}{2}\)<nO2→O2nH2 dư
Theo PT: nH2O=nH2=0,4(mol)
→mH2O=0,4.18=7,2(g)
Đúng 1
Bình luận (0)



























