Quan sát Hình 4.1 và 4.2, so sánh điểm giống nhau và khác nhau giữa mô hình Rutherford – Bohr với mô hình hiện đại mô tả sự chuyển động của electron trong nguyên tử.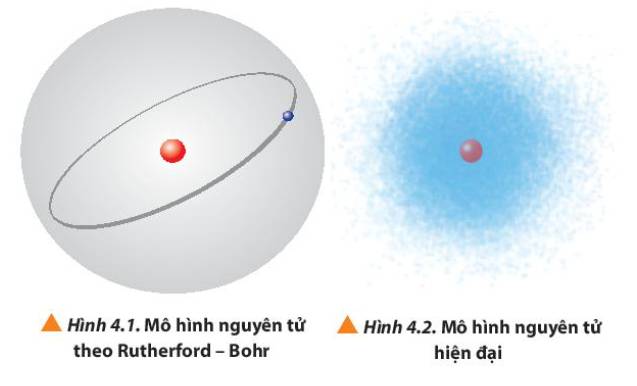

Những câu hỏi liên quan
Trả lời những câu hỏi sau đây liên quan đến mô hình Rutherford – Bohr và mô hình hiện đại về nguyên tử.a) Vì sao còn gọi mô hình Rutherford – Bohr là mô hình hành tinh nguyên tử?b) Theo mô hình hiện đại, orbital p có hình số tám nổi với hai phần (còn gọi là hai thùy) giống hệt nhau. Xác suất tìm thấy electron ở mỗi thùy là khoảng bao nhiêu phần trăm?c) So sánh sự giống và khác nhau giữa mô hình Rutherford – Bohr và mô hình hiện đại về nguyên tử.
Đọc tiếp
Trả lời những câu hỏi sau đây liên quan đến mô hình Rutherford – Bohr và mô hình hiện đại về nguyên tử.
a) Vì sao còn gọi mô hình Rutherford – Bohr là mô hình hành tinh nguyên tử?
b) Theo mô hình hiện đại, orbital p có hình số tám nổi với hai phần (còn gọi là hai thùy) giống hệt nhau. Xác suất tìm thấy electron ở mỗi thùy là khoảng bao nhiêu phần trăm?
c) So sánh sự giống và khác nhau giữa mô hình Rutherford – Bohr và mô hình hiện đại về nguyên tử.
a) Mô hình Rutherford – Bohr còn gọi là mô hình hành tinh nguyên tử vì trong mô hình Rutherford – Bohr electron quay xung quanh hạt nhân theo các quỹ đạo giống như các hành tinh quay xung quanh Mặt Trời.
b) Theo mô hình hiện đại, xác suất tìm thấy electron ở mỗi thùy trong AO p là khoảng 90%.
c)

Đúng 0
Bình luận (0)
Nguyên tử Li (Z = 3) có 2 electron ở lớp K và 1 electron ở lớp L. So sánh năng lượng của electron giữa hai lớp theo mô hình Rutherford – Bohr.
Theo mô hình Rutherford – Bohr: Electron ở càng xa hạt nhân thì có năng lượng càng cao.
⇒ Lớp L ở xa hạt nhân hơn nên electron ở lớp L có năng lượng cao hơn.
Đúng 0
Bình luận (0)
Khái niệm AO xuất phát từ mô hình Rutherford – Bohr hay mô hình hiện đại về nguyên tử?
Khái niệm AO (orbital nguyên tử) xuất phát từ mô hình hiện đại về nguyên tử
Đúng 0
Bình luận (0)
Các nguyên tố chu kì 2 có bao nhiêu lớp electron? Vẽ mô hình nguyên tử theo Rutherford – Bohr của Li và F để giải thích về sự khác biệt bán kính nguyên tử.
- Các nguyên tố chu kì 2 có 2 lớp electron.
- Mô hình nguyên tử của Li (Z = 3) và F (Z = 9) theo Rutherford – Bohr như sau:

- Nguyên tố Li và F đều có 2 lớp electron nên cùng chu kì 2, số đơn vị điện tích hạt nhân của Li nhỏ hơn F. Vì vậy bán kính nguyên tử Li lớn hơn nguyên tử F.
Đúng 0
Bình luận (0)
Hãy mô tả mô hình hoạt động của thư điện tử. Mô hình này có điểm gì giống và khác với mô hình chuyển thư truyền thống?
– Mô hình hoạt động của thư điện tử là:
+ Người gửi viết thư và ghi địa chỉ người nhận;
+ Người dùng gửi thư cho máy chủ thư điện tử;
+ Máy chử thư điện tử chuyển vận thư điện tử nhờ Internet;
+ Máy chủ thư điện tử nhận thư và gửi cho người nhận.
– Những điểm giống và khác với mô hình thư truyền thống
+ Giống nhau: Việc gửi và nhận thư đều qua 4 bước;
+ Khác nhau: Mô hình chuyển thư truyền thống được thực hiện bằng các phương tiện khác nhau, còn thư điện tử được thực hiện bằng Internet.
Đúng 0
Bình luận (0)
Hãy mô tả mô hình hoạt động của thư điện tử. Mô hình này có điểm gì giống và khác với mô hình chuyển thư truyền thống?
- Mô hình hoạt động của thư điện tử là:
+ Người gửi viết thư và ghi địa chỉ người nhận;
+ Người dùng gửi thư cho máy chủ thư điện tử;
+ Máy chử thư điện tử chuyển vận thư điện tử nhờ Internet;
+ Máy chủ thư điện tử nhận thư và gửi cho người nhận.
- Những điểm giống và khác với mô hình thư truyền thống
+ Giống nhau: Việc gửi và nhận thư đều qua 4 bước;
+ Khác nhau: Mô hình chuyển thư truyền thống được thực hiện bằng các phương tiện khác nhau, còn thư điện tử được thực hiện bằng Internet.
Tìm hiểu mối quan hệ giữa số electron ở lớp ngoài cùng của nguyên tử các nguyên tố với số thứ tự của nhómChuẩn bị: 4 mô hình sắp xếp electron ở vỏ nguyên tử của Li, Na, F, Cl theo mẫu mô tả trong Hình 4.4.Quan sát các mô hình đã chuẩn bị, thảo luận và trả lời câu hỏi:1. Hãy cho biết nguyên tử các nguyên tố nào có cùng số electron ở lớp ngoài cùng2. Hãy so sánh số electron lớp ngoài cùng của nguyên tử các nguyên tố với số thứ tự nhóm của các nguyên tố đó
Đọc tiếp
Tìm hiểu mối quan hệ giữa số electron ở lớp ngoài cùng của nguyên tử các nguyên tố với số thứ tự của nhóm
Chuẩn bị: 4 mô hình sắp xếp electron ở vỏ nguyên tử của Li, Na, F, Cl theo mẫu mô tả trong Hình 4.4.
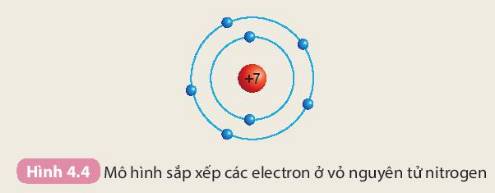
Quan sát các mô hình đã chuẩn bị, thảo luận và trả lời câu hỏi:
1. Hãy cho biết nguyên tử các nguyên tố nào có cùng số electron ở lớp ngoài cùng
2. Hãy so sánh số electron lớp ngoài cùng của nguyên tử các nguyên tố với số thứ tự nhóm của các nguyên tố đó
1:
Nguyên tử Li, Na có cũng số electron ở lớp ngoài cùng
Nguyên tử F, Cl có cũng số electron ở lớp ngoài cùng
2: Số electron lớp ngoài cùng của nguyên tử các nguyên tố chính là số thứ tự nhóm của các nguyên tố
Đúng 0
Bình luận (0)
Tìm hiểu mối quan hệ giữa số lớp electron của nguyên tử các nguyên tố với số thứ tự của chu kìChuẩn bị: 6 mô hình sắp xếp electron ở vỏ nguyên tử của sáu nguyên tố H, He, Li, Be, C, N theo mẫu được mô tả trong Hình 4.4Quan sát các mô hình đã chuẩn bị, thảo luận và thực hiện các yêu cầu sau:1. Hãy cho biết số lớp electron của nguyên tử các nguyên tố trên.2. So sánh số lớp electron của nguyên tử các nguyên tố trên với số thứ tự chu kì của các nguyên tố đó.
Đọc tiếp
Tìm hiểu mối quan hệ giữa số lớp electron của nguyên tử các nguyên tố với số thứ tự của chu kì
Chuẩn bị: 6 mô hình sắp xếp electron ở vỏ nguyên tử của sáu nguyên tố H, He, Li, Be, C, N theo mẫu được mô tả trong Hình 4.4
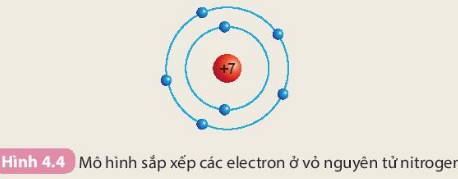
Quan sát các mô hình đã chuẩn bị, thảo luận và thực hiện các yêu cầu sau:
1. Hãy cho biết số lớp electron của nguyên tử các nguyên tố trên.
2. So sánh số lớp electron của nguyên tử các nguyên tố trên với số thứ tự chu kì của các nguyên tố đó.
1. Nguyên tử nguyên tố H , nguyên tử nguyên tố He có 1 lớp e
Nguyên tử nguyên tố Li, Be, C, N có 2 lớp e.
2. STT chu kì của nguyên tử nguyên tố H, He (1) < STT chu kì của nguyên tử nguyên tố Li, Be, C, N (2)
Đúng 0
Bình luận (0)
Quan sát Hình 8.3, mô tả sự giống và khác nhau của phương pháp hàn hồ quang tay và hàn hơi.
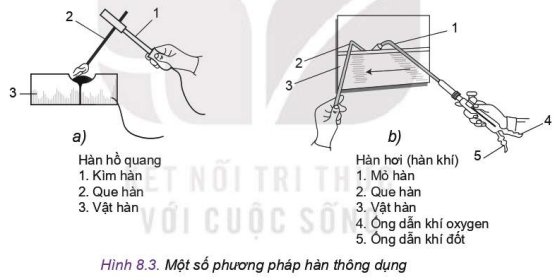
- Giống nhau: có phần 2 và 3 là que hàn và vật hàn
- Khác nhau:
+ Hàn hồ quang: có ba phần, trong đó phần 1 là kim hàn
+ Hàn hơi: có năm phần, trong đó phần 1 là mỏ hàn, phần 4 là ống dẫn khí oxygen và phần 5 là ống dẫn khí đốt
Đúng 0
Bình luận (0)











