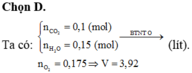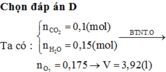1. Đốt cháy hoàn toàn 1 gam C2H2(g) ở điều kiện chuẩn, thu được CO2(g) và H2O(l), giải phóng 49,98 kJ. Tính biến thiên enthalpy chuẩn của phản ứng đốt cháy 1 mol C2H2.

Những câu hỏi liên quan
Đốt cháy hoàn toàn 1 gam C2H2(g) ở điều kiện chuẩn, thu được CO2(g) và H2O(l), giải phóng 49,98 kJ. Tính biến thiên enthalpy chuẩn của phản ứng đốt cháy 1 mol C2H2.
nC2H2 = 1/26 (mol)
Đốt cháy 1/26 mol C2H2 tỏa ra 49,98 kJ
=> Đốt cháy 1 mol C2H2 tỏa ra x kJ
=> x = 1 x 49,98 : (1/26) = 1299,48 kJ
=> ${\Delta _r}H_{298}^0$ = -1299,48 kJ (vì đây là phản ứng tỏa nhiệt nên enthalpy mang giá trị âm)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 1,00 gam khí C2H2 thu được CO2(k) và H2O(l) giải phóng 50,01 kJ. Tính biến thiên enthalpy của phản ứng đốt cháy 1 mol khí C2H2, từ đó cho biết vì sao C2H2 được sử dụng trong đèn xì hàn cắt kim loại mà không dùng mêtan.
\(\Delta_rH=-\dfrac{50,01kJ}{\dfrac{1}{26}mol}=-1300,26kJ\cdot mol^{-1}\)
Mặt khác, khi đốt 1 mol methane chỉ toả ra lượng nhiệt khoảng 890,2 kJ, thấp hơn nhiều so với acetylene nên acetylene được dùng trong đèn xì.
Đúng 1
Bình luận (0)
d) Xác định biến thiên enthalpy chuẩn của phản ứng đốt cháy 1 mol ethane. Biết nhiệt tạo thành
chuẩn của C2H6 (l), CO2 (g) và H2O (l) tương ứng là -84,7 kJ/mol, -393,5 kJ/mol và -285,8
kJ/mol.
\(C_2H_6+\dfrac{7}{2}O_2->2CO_2+3H_2O\\ \Delta_rH^o_{298}=2\left(-393,5\right)+3\left(-285,8\right)-\left(-84,7\right)\\ \Delta_rH^o_{298}=-1559,7kJ\)
Đúng 1
Bình luận (2)
Đốt cháy hoàn toàn 5,8 g ankan X, sau phản ứng thu được 8,96 lít CO2 điều kiện tiêu chuẩn và m gam H2O a. Tìm CTPT của X b. Tính mH20 c. Tính VO2(đktc) cần dùng
a) \(n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Bảo toàn C: nC = 0,4 (mol)
=> \(n_H=\dfrac{5,8-0,4.12}{1}=1\left(mol\right)\)
Xét nC : nH = 0,4 : 1 = 2 : 5
=> CTPT: (C2H5)x
Mà CTPT của X có dạng CnH2n+2
=> x = 2
=> CTPT: C4H10
b)
PTHH: 2C4H10 + 13O2 --to--> 8CO2 + 10H2O
0,65<-------0,4------->0,5
=> \(m_{H_2O}=0,5.18=9\left(g\right)\)
c) \(V_{O_2}=0,65.22,4=14,56\left(l\right)\)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn hỗn hợp gồm các hiđrocacbon thu được 2,24 lít (đktc) CO2 và 2,7 gam H2O. Thể tích oxi đã tham gia phản ứng cháy ở điều kiện tiêu chuẩn là A. 5,6 lít B. 2,8 lít C. 4,48 lít D. 3,92 lít.
Đọc tiếp
Đốt cháy hoàn toàn hỗn hợp gồm các hiđrocacbon thu được 2,24 lít (đktc) CO2 và 2,7 gam H2O. Thể tích oxi đã tham gia phản ứng cháy ở điều kiện tiêu chuẩn là
A. 5,6 lít
B. 2,8 lít
C. 4,48 lít
D. 3,92 lít.
Đốt cháy hoàn toàn hỗn hợp gồm các hidrocacbon thu được 2,24 lít (đktc) CO2 và 2,7 gam H2O. Thể tích oxi đã tham gia phản ứng cháy ở điều kiện tiêu chuẩn là A. 5,6 lít B. 2,8 lít C. 4,48 lít. D. 3,92 lít
Đọc tiếp
Đốt cháy hoàn toàn hỗn hợp gồm các hidrocacbon thu được 2,24 lít (đktc) CO2 và 2,7 gam H2O. Thể tích oxi đã tham gia phản ứng cháy ở điều kiện tiêu chuẩn là
A. 5,6 lít
B. 2,8 lít
C. 4,48 lít.
D. 3,92 lít
Đốt cháy hoàn toàn hỗn hợp gồm các hidrocacbon thu được 2,24 lít (đktc) CO2 và 2,7 gam H2O. Thể tích oxi đã tham gia phản ứng cháy ở điều kiện tiêu chuẩn là A. 5,6 lít. B. 2,8 lít. C. 4,48 lít. D. 3,92 lít.
Đọc tiếp
Đốt cháy hoàn toàn hỗn hợp gồm các hidrocacbon thu được 2,24 lít (đktc) CO2 và 2,7 gam H2O. Thể tích oxi đã tham gia phản ứng cháy ở điều kiện tiêu chuẩn là
A. 5,6 lít.
B. 2,8 lít.
C. 4,48 lít.
D. 3,92 lít.
Methane là thành phần chính của khí thiên nhiên. Xét phản ứng đốt cháy methane:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) ΔrH298
o = -890,3 kJ
Biết nhiệt tạo thành chuẩn của CO2(g) và H2O(l) tương ứng là –393,5 và –285,8 kJ/mol. Hãy tính
nhiệt tạo thành chuẩn của khí methane.
\(\Delta_fH^{^{ }o}_{298}\left[CH_4\right]=-\left(-890,3-\left(-393,5\right)-\left(-285,8\right)\right)\\ \Delta_fH^{^{ }o}_{298}\left[CH_4\right]=211kJ\cdot mol^{-1}\)
Đúng 1
Bình luận (0)
đốt cháy hoàn toàn m(g) C2H5OH =2,24 (l) O2 ở điều kiện tiêu chuẩn .Thu được m1 (g) hỗn hợp bột CO2 và H2O . Tính giá trị của m và m1