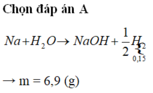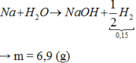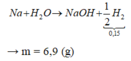Cho 8,05 gam Na tác dụng với m gam rượu etylic thu được 3,36 lít khí hiđro (đktc). Tìm giá trị của m.
Ta có: \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PT: \(2Na+2C_2H_5OH\rightarrow2C_2H_5ONa+H_2\)
Theo PT: \(n_{C_2H_5OH}=2n_{H_2}=0,3\left(mol\right)\)
\(\Rightarrow m_{C_2H_5OH}=0,3.46=13,8\left(g\right)=m\)
Đúng 3
Bình luận (0)
Cho m gam Na tác dụng với nước dư thu được 3,36 lít khí (đktc). Giá trị của m là
A. 6,90
B. 3,45
C. 9,20
D. 4,60
Cho m gam Na tác dụng với nước dư thu được 3,36 lít khí (đktc). Giá trị của m là
A. 3,45
B. 6,90
C. 9,20
D. 4,60
Cho m gam Na tác dụng với nước dư thu được 3,36 lít khí (đktc). Giá trị của m là
A. 3,45.
B. 6,90.
C. 9,20.
D. 4,60.
Cho 8,5 gam hỗn hợp Na và K tác dụng hết với nước thu được 3,36 lít khí
H
2
(đktc) và dung dịch X. Cho X tác dụng vừa đủ với dung dịch
F
e
2
S
O
4
3
thu được m gam kết tủa. Giá trị của m là A. 5,35 B. 16,05 C. 10,70 D. 21,40
Đọc tiếp
Cho 8,5 gam hỗn hợp Na và K tác dụng hết với nước thu được 3,36 lít khí H 2 (đktc) và dung dịch X. Cho X tác dụng vừa đủ với dung dịch F e 2 S O 4 3 thu được m gam kết tủa. Giá trị của m là
A. 5,35
B. 16,05
C. 10,70
D. 21,40
Cho 8,50 gam hỗn hợp Na và K tác dụng hết với nước thu được 3,36 lít khí H2 (đktc) và dung dịch X. Cho X tác dụng vừa đủ với dung dịch Fe2(SO4)3 thu được m gam kết tủa. Giá trị của m là: A.5,35. B.16,05. C. 10,70. D. 21,40.
Đọc tiếp
Cho 8,50 gam hỗn hợp Na và K tác dụng hết với nước thu được 3,36 lít khí H2 (đktc) và dung dịch X. Cho X tác dụng vừa đủ với dung dịch Fe2(SO4)3 thu được m gam kết tủa. Giá trị của m là:
A.5,35.
B.16,05.
C. 10,70.
D. 21,40.
Đáp án C
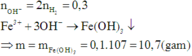
Nhận xét:Ở bài này, giả thiết cho thừa dữ kiện về tổng khối lượng hai kim loại. Đề bài sẽ hay hơn khi thay một trong hai kim loại kiềm trong hỗn hợp bằng kim loại Ba, khi đó kết tủa tạo thành gồm Fe(OH)3 và BaSO4. Để tính n F e ( O H ) 3 ta vẫn có cách làm như trên, tuy nhiên để tính được n B a S O 4 thì ta cần biết nBa , khi đó ta cần lập và giải hệ 2 phương trình bậc nhất 2 ẩn là nBa và nNa (hoặc nK ) theo giả thiết về khối lượng và n H 2 .
Đúng 0
Bình luận (0)
Cho m gam dung dịch rượu etylic nồng độ 29,87% tác dụng hết với Na (dư) thu được 11,76 lít khí H2 (đktc). Biết khối lượng riêng của rượu etylic là 0,8 g/ml. Độ rượu của dung dịch trên là
m C2H5OH = m.29,87% = 0,2987m(gam)
=> n C2H5OH = 0,2987m/46 (mol)
m H2O = m - 0,2987m = 0,7013m(gam)
=> n H2O = 0,7013m/18(mol)
$2C_2H_5OH + 2Na \to 2C_2H_5ONa + H_2$
$2Na + 2H_2O \to 2NaOH + H_2$
n H2 = 1/2 n C2H5OH + 1/2 H2O = 11,76/22,4 = 0,525(mol)
=> 1/2 . 0,2987m/46 + 1/2 . 0,7013m/18 = 0,525
=> m = 23,1(gam)
Suy ra :
m C2H5OH = 0,2987.23,1 = 6,9(gam)
V C2H5OH = 6,9/0,8 = 8,625(ml)
m H2O = 0,7013.23,1 = 16,2(gam)
V H2O = 16,2/1 = 16,2(ml)
Vậy :
Đr = V C2H5OH / V(dd) .100 = 8,625/(8,625 + 16,2) .100 = 34,74o
Đúng 2
Bình luận (1)
Hòa tan m gam rượu etylic ( D = 0,8 g/ml) vào 108 ml nước ( D= 1 g/ml) tạo thành dung dịch A. Cho dung dịch A tác dụng với kim loại Na dư, thu được 85,12 lít khí H2 (đktc). Tính giá trị m và nồng độ mol của rượu etylic
nH2 = 85,12 : 22,4 = 3,8 (mol) ; nH2O = VH2O.D = 108 (g) => nH2O = 108/18 = 6 (mol)
PTHH:
2Na + 2C2H5OH → 2C2H5ONa + H2↑
x → 0,5x (mol)
2Na + 2H2O → 2NaOH + H2↑
6 → 3 (mol)
Ta có: nH2 = 0,5x + 3 = 3,8
=> x = 1,6 (mol) = nC2H5OH
mC2H5OH = 1,6.46 = 73,6 (g)
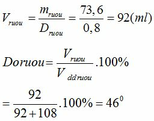
Đúng 0
Bình luận (0)
Cho 22,4 lít khí etilen (đktc) tác dụng với nước có axit sunfuric làm xúc tác, thu được 13,8 gam rượu etylic. Hiệu suất phản ứng cộng nước của etilen là
A. 30%.
B. 40%.
C. 50%.
D. 60%.
Đáp án: A
n C 2 H 4 = 22 , 4 22 , 4 = 1 m o l
PTHH: C 2 H 4 + H 2 O → H 2 S O 4 L o a n g C 2 H 5 O H
1 mol → 1 mol
=> khối lượng rượu etylic thu được theo lí thuyết là: 1.46 = 46 gam
Ta có khối lượng rượu etylic thu được thực tế là 13,8 gam
=> hiệu suất của phản ứng cộng nước của etilen là:
H = m T T m L T . 100 % = 13 , 8 46 . 100 % = 30 %
Đúng 0
Bình luận (0)
1.Đốt cháy hết m gam chất A cần dùng 3,36 lít oxi ở đktc, thu được 4,4 gam CO2 và 1,8 gam H2O. Giá trị đúng của m là bao nhiêu?
2.Cho 1,2 gam magie tác dụng với dung dịch axit sunfuric H2SO4 loãng, dư. Thể tích khí hiđro (đktc) thu được là bao nhiêu?
1) \(n_{O_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Theo ĐLBTKL: m = 4,4 + 1,8 - 0,15.32 = 1,4 (g)
2)
\(n_{Mg}=\dfrac{1,2}{24}=0,05\left(mol\right)\)
PTHH: Mg + H2SO4 --> MgSO4 + H2
0,05------------------------->0,05
=> VH2 = 0,05.22,4 = 1,12 (l)
Đúng 4
Bình luận (0)
mO2 = ( 3,36 : 22,4 ) . 32 = 4,8 (g)
ADDLBTKL ta co :
mA + mO2 = mCO2 + mH2O
=> mA = mCO2 + mH2O - mO2
= 4,4 + 1,8 - 4,8 = 1,4 (g)
=> m= 1,4 (g)
2
nMg = 1,2 : 24 = 0,05 (mol)
pthh : Mg +H2SO4 ---> MgSO4 + H2
0,05--------------------------->0,05(mol)
=> VH2 = 0,05 .22,4 = 1,12 (l)
Đúng 0
Bình luận (0)