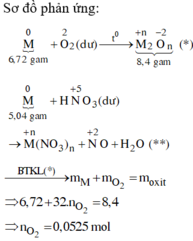cho 8,4 gam MgCO3 tác dụng hết với dung dịch HCL .Thể tích khí C02 thu được (đktc) là : a)22,4 lít ; b)4,48 lít ;c)6,72 lít ;d)2.24 lít

Những câu hỏi liên quan
cho 12,6 gam MgCO3 tác dụng với một lượng vừa đủ dung dịch HCl 2M . Thể tích khí CO2 thu được ở đktc A.3,36 lít B.2,24 lít C.4,48 lít D.5,6 lít
\(n_{MgCO_3}=\dfrac{12,6}{84}=0,15\left(mol\right)\)
\(MgCO_3+2HCl\rightarrow MgCl_2+H_2O+CO_2\)
0,15 0,15
\(V_{CO_2}=0,15.22,4=3,36\left(l\right)\)
--> A
Đúng 0
Bình luận (0)
Cho 5,6 gam Fe tác dụng 100 ml dung dịch HCl 1M. Thể tích khí H₂ thu được (đktc) là bao nhiêu? Biết H = 1 ; Cl = 35,5 ; Fe = 56. A,1,12 lít. B,2,24 lít.C,1 lít.D,22,4 lít.
Xem chi tiết
\(n_{Fe}=\dfrac{5.6}{56}=0.1\left(mol\right)\)
\(n_{HCl}=0.1\cdot1=0.1\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(LTL:0.1>\dfrac{0.1}{1}\Rightarrow Fedư\)
\(n_{H_2}=\dfrac{1}{2}\cdot0.1=0.05\left(mol\right)\)
\(V=0.05\cdot22.4=1.12\left(l\right)\)
Đúng 4
Bình luận (0)
Cho m gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư thu được 8,96 lít khí. Mặt khác, cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích khí đo ở đktc. Giá trị của m là được 8,96 lít khí. Mặt khác, cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích khí đo ở đktc. Giá trị của m là A. 7,80. B. 14,55. C. 6,45. D. 10,2.
Đọc tiếp
Cho m gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư thu được 8,96 lít khí. Mặt khác, cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích khí đo ở đktc. Giá trị của m là được 8,96 lít khí. Mặt khác, cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích khí đo ở đktc. Giá trị của m là
A. 7,80.
B. 14,55.
C. 6,45.
D. 10,2.
Một hỗn hợp bột X gồm sắt và kim loại M có hóa trị không đổi. Nếu hòa tan hết m (gam) hỗn hợp X trong dung dịch HCl thì thu được 7,84 lít khí H2 (đktc). Nếu cho m (gam) hỗn hợp X tác dụng hoàn toàn với khí clo thì thể tích clo cần dùng là 8,4 lít (đktc). Biết tỷ lệ số nguyên tử Fe và kim loại M trong hỗn hợp tương ứng là 1: 4. a) Viết các phương trình hóa học xảy ra. b) Tính thể tích khí Clo (đktc) đã hóa hợp với kim loại M. c) Xác định kim loại M nếu biết rằng m (gam) có giá trị là 8,2 (...
Đọc tiếp
Một hỗn hợp bột X gồm sắt và kim loại M có hóa trị không đổi. Nếu hòa tan hết m (gam) hỗn hợp X trong dung dịch HCl thì thu được 7,84 lít khí H2 (đktc). Nếu cho m (gam) hỗn hợp X tác dụng hoàn toàn với khí clo thì thể tích clo cần dùng là 8,4 lít (đktc). Biết tỷ lệ số nguyên tử Fe và kim loại M trong hỗn hợp tương ứng là 1: 4. a) Viết các phương trình hóa học xảy ra. b) Tính thể tích khí Clo (đktc) đã hóa hợp với kim loại M. c) Xác định kim loại M nếu biết rằng m (gam) có giá trị là 8,2 (gam). d) Tính thể tích khí H2 thu được (đktc) khi hòa tan m (gam) hỗn hợp X trong dung dịch NaOH dư.
Cho 6,5g kẽm tác dụng vừa hết với 200g dung dịch HCl :
a) Tính thể tích khí H2 (đktc) và khối lượng muối thu được.
b) Tính nồng độ % của dung dịch HCl đã dùng.
c) Cho lượng khí hiđro ở trên tác dụng với 3,36 lít oxi (đktc) thì thu được bao nhiêu gam nước?
a) \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,1-->0,2------>0,1-->0,1
=> VH2 = 0,1.22,4 = 2,24 (l)
mZnCl2 = 0,1.136 = 13,6 (g)
b) \(C\%_{dd.HCl}=\dfrac{0,2.36,5}{200}.100\%=3,65\%\)
c) \(n_{O_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: 2H2 + O2 --to--> 2H2O
Xét tỉ lệ: \(\dfrac{0,1}{2}< \dfrac{0,15}{1}\) => H2 hết, O2 dư
PTHH: 2H2 + O2 --to--> 2H2O
0,1--------------->0,1
=> mH2O = 0,1.18 = 1,8 (g)
Đúng 1
Bình luận (0)
Cho 22,4 gam một kim loại hóa trị II tác dụng hết với dung dịch HCl, sau phản ứng thu được 8,96 lít khí hidro (đktc). Tìm tên kim loại
Cho m gam amin đơn chức bậc 1 X tác dụng với dung dịch HCl vửa đủ thu được m + 3,65 gam muối. Đốt cháy hoàn toàn m gam X cần 8,4 lít khí
O
2
(đktc). X có thể là A.
C
H
3
N
H
2
.
B.
C
2
H
5
N
H
2...
Đọc tiếp
Cho m gam amin đơn chức bậc 1 X tác dụng với dung dịch HCl vửa đủ thu được m + 3,65 gam muối. Đốt cháy hoàn toàn m gam X cần 8,4 lít khí O 2 (đktc). X có thể là
A. C H 3 N H 2 .
B. C 2 H 5 N H 2 .
C. C 3 H 7 N H 2 .
D. C 4 H 9 N H 2
Sử dụng tăng giảm khối lượng: n H C l = m + 3 , 65 − m 36 , 5 = 0 , 1 m o l
Vì amin đơn chức => n a m i n = 0 , 1 m o l
Dựa vào 4 đáp án => amin no, mạch hở, đơn chức
Gọi n C O 2 = x m o l ; n H 2 O = y m o l
Vì đốt cháy amin no, mạch hở, đơn chức: n H 2 O − n C O 2 = 1 , 5. n a m i n
=> y – x = 0,1 (1)
Bảo toàn nguyên tử O: 2 n O 2 = 2 n C O 2 + n H 2 O = > 2 x + y = 0 , 75 2
Từ (1) và (2) => x = 0,2; y = 0,35
→ số C trong X = n C O 2 / n X = 0 , 2 / 0 , 1 = 2
=> X là C 2 H 7 N
Đáp án cần chọn là: B
Đúng 0
Bình luận (0)
Đốt cháy 6,72 gam kim loại M với oxi dư thu được 8,4 gam oxit. Nếu cho 5,04 gam M tác dụng hết với dung dịch HNO3 dư thu được dung dịch X và khí NO (là sản phẩm khử suy nhất). Thể tích khí NO (đktc) thu được là A. 1,176 lít. B. 2,016 lít. C. 2,24 lít. D. 1,344 lít.
Đọc tiếp
Đốt cháy 6,72 gam kim loại M với oxi dư thu được 8,4 gam oxit. Nếu cho 5,04 gam M tác dụng hết với dung dịch HNO3 dư thu được dung dịch X và khí NO (là sản phẩm khử suy nhất). Thể tích khí NO (đktc) thu được là
A. 1,176 lít.
B. 2,016 lít.
C. 2,24 lít.
D. 1,344 lít.
Cho m gam hỗn hợp A gồm: Al, Na, Mg tác dụng với nước dư thu được 2,24 lít khí H2. Nếu lấy 2m gam hỗn hợp A tác dụng với dung dịch NaOH dư thu được 8,96 lít khí H2. Nếu lấy 3m gam hỗn hợp A tác dụng với dung dịch HCl vừa đủ thu được 22,4 lít khí H2. Biết các thể tích khí đo ở đktc, tính m và phần trăm về khối lượng của từng kim loại trong A
Đặt x,y, z lần lượt là số mol của Na,Al,Mg trong m gam hỗn hợp A
m gam A + H2O dư
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
x--------------------x--------->0,5x
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
x<------x-------------------------------------->1,5x
=> \(0,5x+1,5x=\dfrac{2,24}{22,4}=0,1\left(mol\right)\) (1)
2m gam A + NaOH
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
2x------------------------------->x
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
2y---------------------------------------------->3y
=> \(x+3y=\dfrac{8,96}{22,4}=0,4\left(mol\right)\) (2)
3m gam A + HCl
\(Na+HCl\rightarrow NaCl+\dfrac{1}{2}H_2\)
3x--------------------------->1,5x
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
3y----------------------------->4,5y
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
3z----------------------------->3z
=> \(1,5x+4,5y+3z=\dfrac{22,4}{22,4}=1\left(mol\right)\) (3)
Từ (1), (2), (3) =>\(\left\{{}\begin{matrix}x=0,05\\y=\dfrac{7}{60}\\z=\dfrac{2}{15}\end{matrix}\right.\)
=> \(m_{Na}=0,05.23=1,15\left(g\right)\)
\(m_{Al}=\dfrac{7}{60}.27=3,15\left(g\right)\)
\(m_{Mg}=\dfrac{2}{15}.24=3,2\left(g\right)\)
=> \(m=1,15+3,15+3,2=7,5\left(g\right)\)
=> \(\%m_{Na}=\dfrac{1,15}{7,5}.100=15,33\%\)
\(\%m_{Al}=\dfrac{3,15}{7,5}.100=42\%\)
\(\%m_{Mg}=\dfrac{3,2}{7,5}.100=42,67\%\)
Đúng 2
Bình luận (0)
: Cho m gam hỗn hợp A gồm: Al, Na, Mg tác dụng với nước dư thu được 2,24 lít khí H2. Nếu lấy 2m gam hỗn hợp A tác dụng với dung dịch NaOH dư thu được 8,96 lít khí H2. Nếu lấy 3m gam hỗn hợp A tác dụng với dung dịch HCl vừa đủ thu được 22,4 lít khí H2. Biết các thể tích khí đo ở đktc, tính m và phần trăm về khối lượng của từng kim loại trong A
\(2Na+2H2O\rightarrow2NaOH+H2\left(1\right)\)
\(2Al+2NaOH+2H2O\rightarrow2NaAlO2+3H2\left(2\right)\)
\(2Al+6HCl\rightarrow2AlCl3+3H2\left(3\right)\)
\(2Na+2HCl\rightarrow2NaCl+H2\left(4\right)\)
\(Mg+2HCl\rightarrow MgCl2+H2\left(5\right)\)
\(n_{H2\left(1\right)}=0,1\left(mol\right)\rightarrow n_{Na}=0,2\left(mol\right)\rightarrow m_{Na}=4,6\left(g\right)\)
\(n_{H2\left(2\right)}=0,4\left(mol\right)\Rightarrow n_{Al}=\dfrac{4}{15}\left(mol\right)\Rightarrow m_{Al}=7,2\left(g\right)\)
\(\Rightarrow n_{H2\left(3\right)}=\dfrac{3}{2}n_{Al}=0,4\left(mol\right)\)
\(n_{H2\left(4\right)}=\dfrac{1}{2}n_{Na}=0,1\left(mol\right)\)
\(\Rightarrow n_{H2\left(5\right)}=1-0,4-0,1=0,5\left(mol\right)\)
\(\Rightarrow n_{Mg}=0,5\left(mol\right)\Rightarrow m_{Mg}=12\left(g\right)\)
\(\Rightarrow m=12+4,6+7,2=23,8\left(g\right)\)
\(\%m_{Na}=\dfrac{4,6}{23,8}.100\%=19,33\%\)
\(\%m_{Al}=\dfrac{7,2}{23,8}.100\%=30,25\%\)
\(\%m_{Mg}=100-19,33-30,25=50,42\%\)
Chúc bạn học tốt
Đúng 2
Bình luận (1)