Cho 10,8 g Al tác dụng với dung dịch có chứa 49g HCl
a. Tính thể tích khí thoát ra (đktc)?
b. Tính khối lượng các chất sau phản ứng?
c. Nhúng quỳ tím vào dung dịch sau phản ứng quỳ tím có đổi màu ko? Vì sao?
cho 22,4g sắt tác dụng với dung dịch loãng có chứa 49g axit H2SO4
a/ tính thể tích khí H2 thu được ở đktc
b/ dung dịch sau phản ứng làm quỳ tím đổi màu không
a) \(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\); \(n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
Xét tỉ lệ: \(\dfrac{0,4}{1}< \dfrac{0,5}{1}\) => Fe hết, H2SO4 dư
PTHH: Fe + H2SO4 --> FeSO4 + H2
0,4--->0,4-------->0,4--->0,4
=> VH2 = 0,4.22,4 = 8,96 (l)
b) Do trong dd sau pư có H2SO4 dư nên dd làm quỳ tím chuyển màu đỏ
\(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\\ n_{H_2SO_{\text{ 4 }}}=\dfrac{49}{98}=0,5\left(mol\right)\\ pthh:Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
LTL: 0,4<0,5 => Fe hết H2SO4 dư
theo pthh : nH2 = nFe =0,4(mol)
=> \(V_{H_2}=0,4.22,4=8,96\left(l\right)\)
dd là muối => nhưng có H2SO4 dư nên qt CHUYỂN đỏa
Cho 200 ml dung dịch NaOH 0,5M tác dụng với 300ml dung dịch H2SO4 1M. a) Tính nồng độ mol các chất trong dung dịch sau phản ứng. b) Cho quỳ tím vào dung dịch sau phản ứng, quỳ tím có bị đổi màu không? Vì sao?
\(a)n_{NaOH}=0,5.0,2=0,1mol\\ n_{H_2SO_4}=0,3.1=0,3mol\\2 NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\\ \Rightarrow\dfrac{0,1}{2}< \dfrac{0,3}{1}\Rightarrow H_2SO_4.dư\\ 2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
0,1 0,05 0,05 0,1
\(C_M\) \(_{Na_2SO_4}=\dfrac{0,05}{0,2+0,3}=0,1M\)
\(C_M\) \(_{H_2SO_4}=\dfrac{0,3-0,05}{0,2+0,3}=0,5M\)
b) Vì H2SO4 dư nên quỳ tím hoá đỏ.
cho 200(g) BaCl2 10,4(%) tác dụng vừa đủ với dung dịch H2SO4 (41,9%). a) viết phương trình phản ứng xảy ra. b) nếu cho quỳ tím cho vào dung dịch sau phản ứng quỳ tím có màu gì? c) tính khối lượng chất kết tủa tạo thành. d) tính khối lượng dung dịch H2SO4 4,9(%) đã dùng. e) tính nồng độ phần trăm dung dịch sau phản ứng
\(n_{BaCl_2}=\dfrac{200.10,4\%}{208}=0,1\left(mol\right)\\ a,BaCl_2+H_2SO_4\rightarrow BaSO_4+2HCl\\ b,Qu\text{ỳ}-t\text{í}m-ho\text{á}-\text{đ}\text{ỏ}-do-c\text{ó}-\text{ax}it-HCl\\ c,n_{BaSO_4}=n_{H_2SO_4}=n_{BaCl_2}=0,1\left(mol\right)\\ m_{k\text{ết}-t\text{ủa}}=m_{BaSO_4}=233.0,1=23,3\left(g\right)\\ d,m_{\text{dd}H_2SO_4}=\dfrac{0,1.98}{4,9\%}=200\left(g\right)\\ e,m_{\text{dd}HCl}=200+200-23,3=376,7\left(g\right)\\ n_{HCl}=0,1.2=0,2\left(mol\right)\\ C\%_{\text{dd}HCl}=\dfrac{0,2.36,5}{376,7}.100\approx1,938\%\)
Cho kim loại Na tác dụng với nước thu được 3,36 lít H2(đktc)
A)tính khối lượng Na đã phản ứng và khối lượng sản phẩm tạo thành
B)nếu cho quỳ tím vào dung dịch sau phản ứng, quỳ tím có đổi màu không?
C)với thể tích khí trên có thể khử được bao nhiêu g sắt (III) oxit
a. PTPƯ : 2Na + 2H2O ---> 2NaOH + H2
+ nH2 = 0,15 mol
+ nNa = 2 nH2 =0,3 mol
=> mNa =n.M= 6,9 g
+ nNaOH = nNa = 0,3 mol
=> mNaOH = n. M= 0,3 . 40= 12 gam
b. Quỳ tím hóa xanh
cho13,65 gam kali vào nước dư ,hãy tính
A,thể tích khí H2 thu được sau phản ứng
B,khối lượng KOH thu được sau phản ứng
C,nếu đem quỳ tím nhúng vào dung dịch trên ,theo em quỳ tím sang màu gì
giúp mình với
a,Số mol của 13,65 gam kali là:
\(n_K=\dfrac{m}{M}=\dfrac{13,65}{39}=0,35\left(mol\right)\)
\(2K+2H_2O\rightarrow2KOH+H_2\uparrow\)
2 : 2 : 2 : 1 (mol)
0,35-> 0,35 : 0,35 : 0,175 (mol)
Thể tích của 0,175 mol H2:
\(V_{H_2}=n.22,4=0,175.22,4=3,92\left(l\right)\)
Khối lượng của 0,35 mol KOH:
\(m_{KOH}=n.M=0,35.56=19,6\left(g\right)\)
c, dung dich KOH sau phản ứng có tính bazơ nên khi nhúng giấy quỳ tím vào thì quỳ tím hoá xanh
tóm tắt:
\(m_K=13,65\left(g\right)\)
------------------------
A, \(V_{H_2}=?\left(l\right)\)
B,\(m_{KOH}=?\left(g\right)\)
Đốt 4,6g Na trong bình chứa 2240ml O2 (ở đktc). Nếu sản phẩm sau phản ứng cho tác dụng với H2O thì có H2 bay ra không? Nếu cho giấy quỳ tím vào dung dịch sau phản ứng thì quỳ tím có đổi màu không?
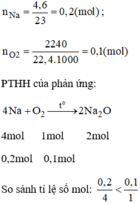
Vậy O 2 dư.
Sau phản ứng Na không dư nên không có khí H 2 bay ra, quỳ tím chuyển sang màu xanh vì:
N a 2 O + H 2 O → 2 N a O H
Cho kim loại sodium tác dụng với nước sau phản ứng thu được 6,1975 lít khí hydrogen (đkc)
a) Viết PTHH, cho biết loại phản ứng? Nêu hiện tượng
b) Cho quỳ tím vào dung dịch sau phản ứng, cho biết sự đổi màu của giấy quỳ tím?
c) Tính khối lượng sodium đã phản ứng
d) Tính và đọc tên sản phẩm tạo thành
(Na=23,O=16,H=1)
a) Na nóng chảy, chạy trên mặt nước, tan dần và có khí không màu thoát ra
PTHH: 2Na + 2H2O --> 2NaOH + H2 (pư oxi hóa-khử)
b) Sau pư, thu được dd bazo nên quỳ tím chuyển màu xanh
c) \(n_{H_2}=\dfrac{6,1975}{24,79}=0,25\left(mol\right)\)
PTHH: 2Na + 2H2O --> 2NaOH + H2
0,5<----------------0,5<---0,25
=> mNa = 0,5.23 = 11,5 (g)
d) Sản phẩm tạo thành là NaOH (sodium hydroxide) và H2(hydrogen)
mNaOH = 0,5.40 = 20 (g)
mH2 = 0,25.2 = 0,5 (g)
Cho 13g kẽm vào dung dịch chứa 18,25 HCI a.Tính thể tích hiđro (đktc) thu được ? b.Nếu nhúng quỳ tím vào dung dịch thu được thì quỳ tím chuyển sang màu gì ? c.Cho toàn bộ lượng hiđro trên qua 24g CuO đun nóng, sau phản ứng thu được chất rắn X. Tính khối lượng của X.
a, \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
\(n_{HCl}=\dfrac{18,25}{36,5}=0,5\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Xét tỉ lệ: \(\dfrac{0,2}{1}< \dfrac{0,5}{2}\), ta được HCl dư.
Theo PT: \(n_{H_2}=n_{Fe}=0,2\left(mol\right)\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b, - Nhúng quỳ tím vào dd thấy quỳ chuyển đỏ do HCl dư.
c, \(n_{CuO}=\dfrac{24}{80}=0,3\left(mol\right)\)
PT: \(H_2+CuO\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,2}{1}< \dfrac{0,3}{1}\), ta được CuO dư.
Theo PT: \(n_{CuO\left(pư\right)}=n_{Cu}=n_{H_2}=0,2\left(mol\right)\Rightarrow n_{CuO\left(dư\right)}=0,3-0,2=0,1\left(mol\right)\)
⇒ mX = mCu + mCuO dư = 0,2.64 + 0,1.80 = 20,8 (g)
| Cho 50 gam dung dịch natri hidroxit 20% tác dụng với 84 gam dung dịch axit |
| nitric 15%. |
| a- Viết PTHH |
| b- Cho quỳ tím vào dung dịch thu được sau phản ứng, quỳ tím có màu gì? Vì |
| sao? |
| c- Tính nồng độ % các chất trong dung dịch thu được sau phản ứng ? |
| Cho: Na = 23 O = 15 H = 1 N = 14 |
\(n_{NaOH}=\dfrac{50\cdot20\%}{40}=0.25\left(mol\right)\)
\(n_{HNO_3}=\dfrac{84\cdot15\%}{63}=0.2\left(mol\right)\)
\(NaOH+HNO_3\rightarrow NaNO_3+H_2O\)
Lập tỉ lệ :
\(\dfrac{0.25}{1}>\dfrac{0.2}{1}\Rightarrow NaOHdư\)
Vì : NaOH dư nên quỳ tím sẽ hóa xanh.
\(m_{dd}=50+84=134\left(g\right)\)
\(n_{NaNO_3}=0.2\left(mol\right)\)
\(n_{NaOH\left(dư\right)}=0.25-0.2=0.05\left(mol\right)\)
\(C\%_{NaNO_3}=\dfrac{0.2\cdot85}{134}\cdot100\%=12.68\%\)
\(C\%_{NaOH\left(dư\right)}=\dfrac{0.05\cdot40}{134}\cdot100\%=1.49\%\)