lấy V1 ml dd C2H5OH (trong đó chiếm 96% thể tích) pha với V2 ml nước cất thu được 1800ml dd C2H5OH sử dụng sát khuẩn trong y tế
Tính giá trị của V1
Tính tỉ lệ V1 : V2
a/ Trộn V1 (ml) dd HNO3 (pH = 1) với V2 (ml) dd HNO3 (pH = 3) để được dd có pH = 2.
b/ Pha thêm V1(ml) nước vào V2 (ml) dd NaOH (pH = 13) để được dd có pH = 12
Trộn v1 ml dd HCl 10M với V2 ml nước được 40ml dd HCl 2M . Tính v1 và v2?
nHCl(cuối)=0,04.2=0,08(mol)
Ta có: 10V1=0,08
<=>V1=0,008(l)=8(ml)
Mặt khác: V1+V2=40
<=>8+V2=40
<=>V2=32(ml)
Vậy: V1=8(ml); V2=32(ml)
Chúc em học tốt!
Trộn lẫn V1 ml dd NaOH 3% có D=1,05g/ml và V2 ml dd NaOH 10%, D= 1,12g/ml để pha chế được 2 lít dd NaOH 8% có khối lượng riêng là 1,1g/ml. Tính V1 và V2
1.
Nồng độ mol/lit của đ NaOH(1)=\(\dfrac{3.10.1,05}{40}\)=0.7875
......................................... khi trộn là: =\(\dfrac{8.10.1,1}{40}\)=2.2
Áp dụng quy tắc đường chéo ta có
Vdd1/(2-Vdd1)=0.42477
---> Vdd1=0.6l
Vdd2=1.4l
Để pha được 500 ml (V2 = 500 )dung dịch Kcl 0,9M cần lấy V ml (V1) dung dịch Kcl 3Mpha chế với nước cất .Giá trị của V là
\(C_1\cdot V_1=C_2V_2\Leftrightarrow0,5\cdot0,9=3V\Rightarrow V=0,15l\left(150ml\right)\)
Hòa tan hỗn hợp gồm FeO, Fe2O3 và F3O4 (có số mol bằng nhau) bằng dd H2SO4 20% (lượng axit lấy dư 50% so với lượng phản ứng vừa đủ), thu được dd A. Chia A thành bốn phần bằng nhau, mỗi phần có khối lượng 79,3 gam. Phần I tác dụng vừa đủ với V1 ml dung dịch KMnO4 0,05M. Phần II tác dụng vừa đủ với V2 ml dd brom 0,05M. Phần III tác dụng vừa đủ với V3 ml dd HI 0,05M. Cho Na2CO3 từ từ đến dư vào phần IV được V4 lít khí và m gam kết tủa. Giả thiết các phản ứng xảy ra hoàn toàn. Các thể tích khí đo ở đktc. Xác định các giá trị V1, V2, V3, V4.
m dd A = 4 . 79,3 = 317,2g
Qui đổi hỗn hợp FeO, Fe2O3, Fe3O4về Fe3O4 có số mol là a
Ta có 232a + (a . 4 . 1,5 . 98) : 0,2 = 317,2
=> a = 0,1 mol
Dd ban đầu
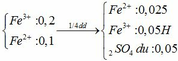
Phần 1:
8H2SO4 + 2KMnO4 + 10FeSO4 → 5Fe2(SO4)3 + 8H2O + 2MnSO4 + K2SO4
0,05 0,025
=> FeSO4 phản ứng hết
=> nKMnO4 = 0,005mol
=> V1= 0,1 lít = 100ml
Phần 2:
2Fe2+ + Br2 → 2Fe3+ + 2Br-
0,025 0,0125
=> V2 = 0,25 lít = 250ml
Phần 3:
2Fe3+ + 2I- → 2Fe2+ + I2
0,05 0,05
=> V3 = 1 lít = 1000ml
Phần 4:
Fe2+ + CO32- → FeCO3↓
0,025 0,025 0,025
2Fe3+ + 3CO32- + 3H2O → 2Fe(OH)3 + 3CO2
0,05 0,075 0,05 0,075
2H+ + CO32- →CO2 + H2O
0,1 0,05 0,05
=> nCO2 = 0,125
=> V4 = 2,8 lít
m kết tủa = mFeCO3 + mFe(OH)3 = 8,25g
Dung dịch A gồm NaOH 0,08M và Ba(OH)2 0,02M. Dung dịch B gồm HCl 0,05M và H2SO4 0,06M
Trộn V1 ml dd A với V2 ml dd B thu được dd có pH = 7. Tính tỉ lệ V1 : V2
\(pH=7\Rightarrow n_{H^+}=n_{OH^-}\)
\(\Leftrightarrow\left(0,05+0,06.2\right)\text{}V_2=\left(0,08+0,02.2\right)V_1\)
\(\Rightarrow V_1:V_2=17:12\)
Bài 3. Dung dịch A gồm NaOH 0,08M và Ba(OH)2 0,02M. Dung dịch B gồm HCl 0,05M và H2SO4 0,06M
Trộn V1 ml dd A với V2 ml dd B thu được dd có pH = 13. Tính tỉ lệ V1 : V2
\(n_{OH^-}=0,12V_1\)
\(n_{H^+}=0,17V_2\)
\(n_{OH^-dư}=\left(V_1+V_2\right).10^{-1}\)
Ta có:
\(n_{OH^-dư}+n_{H^+}=n_{OH^-}\)
\(\Leftrightarrow\left(V_1+V_2\right).10^{-1}=0,12V_1\)
\(\Leftrightarrow0,1V_1=0,02V_2\)
\(\Rightarrow\dfrac{V_1}{V_2}=\dfrac{1}{5}\)
trộn V1 ml NaOH (D1=1,3G/mol) với V2 dd KOH (D2=1,05g/mol) thu được 600ml dd KOH(D=1,15g/mol) tính giá trị V1 và V2
Áp dụng phương pháp đường chéo
\(\Rightarrow\frac{V1}{V2}=\frac{2}{3}\left(1\right)\)
Mặt khác : \(V1+V2=600\left(ml\right)\left(2\right)\)
Từ (1) và (2)\(\Rightarrow\left\{{}\begin{matrix}V1=240ml\\V2=360ml\end{matrix}\right.\)
Nhỏ từ từ 3 V1 ml dung dịch Ba(OH)2 (dd X) vào V1 ml dung dịch Al2(SO4)3 (dd Y) thì phản ứng vừa đủ và ta thu được kết tủa lớn nhất là m gam. Nếu trộn V2 ml dung dịch X ở trên vào V1 ml dung dịch Y thì kết tủa thu được có khối lượng bằng 0,9m gam. So sánh tỉ lệ V2 / V1 thấy
A. V2 / V1 = 2,7 hoặc V2 / V1 = 3,55
B. V2 / V1 = 2,5 hoặc V2 / V1 = 3,25
C. V2 / V1 = 2,7 hoặc V2 / V1 = 3,75
D. V2 / V1 = 2,5 hoặc V2 / V1 = 3,55