Bài 5: Cho 2,24 lit khí hiđro tác dung với 1,68 lit khí oxi . Tính khối lượng nước thu được. ( Thể tích các khí đo ở đktc).

Những câu hỏi liên quan
Bài 10: Đốt cháy 2,8 lit khí hiđro trong không khía) Tính thể tích và khối lượng của khí oxi cần dùng?b) Tính khối lượng nước thu được (Thể tích các khí đo ở đktc).Bài 11: Cho 22,4 lit khí hiđro tác dung với 16,8 lit khí oxi . Tính khối nước thu được. ( Thể tích các khí đo ở đktc).Bài 12: Khử hoàn toàn 48 gam đồng (II) oxit bằng khí H2 ở nhiệt độ caoa) Tính số gam đồng kim loại thu được?b) Tính thể tích khí H2 (đktc) cần dùng?
Đọc tiếp
Bài 10: Đốt cháy 2,8 lit khí hiđro trong không khí
a) Tính thể tích và khối lượng của khí oxi cần dùng?
b) Tính khối lượng nước thu được (Thể tích các khí đo ở đktc).
Bài 11: Cho 22,4 lit khí hiđro tác dung với 16,8 lit khí oxi . Tính khối nước thu được. ( Thể tích các khí đo ở đktc).
Bài 12: Khử hoàn toàn 48 gam đồng (II) oxit bằng khí H2 ở nhiệt độ cao
a) Tính số gam đồng kim loại thu được?
b) Tính thể tích khí H2 (đktc) cần dùng?
10) lập pthh của pư
2H2 + O2 → 2H20
2mol 1mol 2mol
0,125mol 0,0625mol 0,125mol
số mol của H2
nH2= 2,8 : 22,4 =0,125mol
thể tích khí H2
vH2= 0,0624 .22,4 =1,4 lít
khối lượng khí o2
mO2 = 0,0625 . 32= 2 gam
b) khối lượng H20 thu được
mH2O =0,125 . 18 = 2,25 gam
Đúng 0
Bình luận (0)
11) số mol h2
nH2= 22,4 : 2,24 = 10 mol
soosmol của O2
nO2= 16,8 : 22,4 = 0,75 mol
lập pthh của pư
2H2 + 02 → 2 H20
2mol 1mol 2mol
10mol 0,75mol 1,5mol
xét tỉ lệ
\(\frac{nH2}{2}\) = \(\frac{10}{2}\) = 5 > \(\frac{nO2}{1}\)= \(\frac{0,75}{1}\)= 0,75
vậy H2 dư sau pư tính theo O2
số mol H2 dư = ( 0.75 .2) : 1= 1,5 mol
số mol H2 dư = 5 - 1,5=3,5mol
khối lượng H2 dư
m= 3,5 .2=7 gam
khối lượng nước thu được
m=1,5 .2 =3gam
Đúng 0
Bình luận (1)
Khử+16+g+Sắt+(III)+oxit+Fe2O3+bằng+khí+Hiđro++a.+Tính+thể+tích+khí+Hiđro+(ở+đktc)+cần+dùng++b.+Tính+khối+lượng+kim+loại+thu+được+sau+phản+ứng++c.+Nếu+đốt+cháy+kim+loại+đó+trong+khí+oxi+thu+được+khối+lượng+sản+phẩm+là+bao+nhiếu+gam+?++-GIÚP+MÌNH+VỚI+T_T
Đúng 0
Bình luận (1)
Bài 10: Đốt cháy 2,8 lit khí hiđro trong không khía) Tính thể tích và khối lượng của khí oxi cần dùng?b) Tính khối lượng nước thu được (Thể tích các khí đo ở đktc).Bài 11: Cho 22,4 lit khí hiđro tác dung với 16,8 lit khí oxi . Tính khối nước thu được. ( Thể tích các khí đo ở đktc).Bài 12: Khử hoàn toàn 48 gam đồng (II) oxit bằng khí H2 ở nhiệt độ caoa) Tính số gam đồng kim loại thu được?b) Tính thể tích khí H2 (đktc) cần dùng?
Đọc tiếp
Bài 10: Đốt cháy 2,8 lit khí hiđro trong không khí
a) Tính thể tích và khối lượng của khí oxi cần dùng?
b) Tính khối lượng nước thu được (Thể tích các khí đo ở đktc).
Bài 11: Cho 22,4 lit khí hiđro tác dung với 16,8 lit khí oxi . Tính khối nước thu được. ( Thể tích các khí đo ở đktc).
Bài 12: Khử hoàn toàn 48 gam đồng (II) oxit bằng khí H2 ở nhiệt độ cao
a) Tính số gam đồng kim loại thu được?
b) Tính thể tích khí H2 (đktc) cần dùng?
Bài 10: nH2= 0,125 mol
2H2 + O2 → 2H2O
0,125 mol 0,0625 mol 0,125 mol
a) VO2= 0,0625 x 22,4= 1,4 (l) ; mO2= 0,0625 x 32= 2 (g)
b) mH2O= 0,125 x 18 = 2,25 (g)
Đúng 0
Bình luận (1)
Bài 11: nH2= 22,4/22,4 = 1 mol; nO2= 16,8/22,4 =0,75 mol
2H2 + O2 → 2H2O
Ban đầu: 1 mol 0,75 mol
PƯ: 1 mol 0,5 mol 1 mol
Còn lại: 0 mol 0,25 mol 1 mol
mH2O= 1 x 18= 18 (g)
Đúng 0
Bình luận (0)
nCuO= 0,6 mol;
CuO + H2 → Cu + H2O
0,6 mol 0,6 mol 0,6 mol
a) mCu= 0,6 x 64= 38,4 (g)
b) VH2= 0,6 x 22,4= 13,44 (l)
Đúng 0
Bình luận (0)
Cho 3,36 lit khí H2 tác dụng với 1,12 lit khí O2( các thể tích đo ở đktc). Sau phản ứng thu được sản phẩm là H2O.
a) Chất nào còn dư? Dư bao nhiêu lit?
b) Tính khối lượng H2O thu được.
a, Theo gt ta có: $n_{H_2}=0,15(mol);n_{O_2}=0,05(mol)$
$2H_2+O_2\rightarrow 2H_2O$
Sau phản ứng $H_2$ còn dư. Và dư 0,05.22,4=1,12(l)
b, Ta có: $n_{H_2O}=2.n_{O_2}=0,1(mol)\Rightarrow m_{H_2O}=1,8(g)$
Đúng 3
Bình luận (0)
nH2 = 3.36/22.4 = 0.15 (mol)
nO2 = 1.12/22.4 = 0.05 (mol)
2H2 + O2 -to-> 2H2O
0.1___0.05_____0.1
VH2 (dư) = ( 0.15 - 0.1) * 22.4 = 1.12 (l)
mH2O = 0.1*18 = 1.8 (g)
Đúng 2
Bình luận (0)
Dùng 44,8 lit không khí phản ứng với 1,344 lit khí propan (C3H8). Tính: a/ Thể tích chất dư. Biết thể tích các khí đo ở đkc và thể tích khí Oxi chiếm 1/5 thể tích không khí b/ Khối lượng CO2 và H2O thu được
V(O2)= 20%.Vkk=20%. 44,8= 8,92(l) => nO2=0,4(mol)
nC3H8= 1,344/22,4= 0,06(mol)
PTHH: C3H8 + 5 O2 -to-> 3 CO2 + 4 H2O
Ta có: 0,06/1 < 0,4/5
=> O2 dư, C3H8 hết, tính theo nC3H8
=> nO2(p.ứ)= 0,06.5=0,3(mol)=> nO2(dư)=0,4-0,3=0,1(mol)
=> V(O2,dư)=0,1.22,4=2,24(l)
b) nCO2=3.0,06=0,18(mol)
=>mCO2=0,18 . 44=7,92(g)
nH2O=0,06.4=0,24(mol)
=>mH2O=0,24.18=4,32g)
Chúc em học tốt!
Đúng 1
Bình luận (0)
Cho 4,48 lít khí hiđro tác dụng với khí oxi. Biết các thể tích khí đo ở đktc. Tính a/ số gam nước thu được b/ thể tích khí oxi cần dùng
Số mol của 4,48 lít H2:
\(n_{H_2}=\dfrac{V}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH:
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
tỉ lệ: 2 : 1 : 2
0,2-> 0,1 : 0,2( mol)
a/ số gam của 0,2 mol nước:
\(m_{H_2O}=n.M=0,2.=3,6\left(g\right)\)
b/ thể tích của 0,1 mol khí O2:
\(V_{O_2}=n.22,4=0,1.22,4=2,24\left(l\right)\)
Đúng 1
Bình luận (0)
Đốt cháy3,36 lit khí hidro trong lọ chứa3,36 lit khí oxi(các khí đo ở đktc).
a) Chất nào dư? Dư bao nhiêu?
b) Tính khối lượng nước thu được.
nH = \(\frac{3,36}{22,4}=0,15\)(mol)
nO2 = \(\frac{3,36}{22,4}=0,15\)
PTHH: 4H2 + O2 = 2H2O
Tỉ lệ: 4 1 2
Theo PTHH và đề bài, ta có:
\(\frac{0,15}{4}< \frac{0,15}{1}\)
=> H2 hết, O2 dư
b) PTHH: 4H2 + O2 = 2H2O
nH2O = 0,15 : 4 x 2 = 0,075
mH2O = 0,075 x 18 = 1,35 (g)
Cho 11,2 lít khí hiđro (đktc) tác dụng hết với khí oxi thu được nước . Tính thể tích khí oxi tham gia phản ứng (đktc). Tính khối lượng nước tạo thành.
nH2=11,2/22,4=0,5(mol)
2H2+O2->2H2O
0,5 0,25 0,5
V(O2)=0,25*22,4=5,6(lít)
mH2O=0,5*18=9(g)
Đúng 1
Bình luận (0)
Dẫn 6,72 lit hỗn hợp khí X gồm propan, etilen và axetilen đi qua dung dịch brom dư, thấy còn 1,68 lít khí không hấp thụ. Nếu dẫn 6,72 lit hỗn hợp khí X trên qua dung dịch AgNO3/NH3 thấy có 24,24 gam kết tủa. Các thể tích khí đo ở đktc. Tính thành phần phần trăm theo thể tích và theo khối lượng của mỗi khí trong hỗn hợp.
1,68 lit khí không bị dung dịch Br2 hấp thụ là propan
![]()
![]()
![]()
![]()
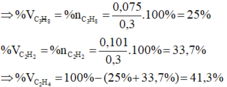
![]()
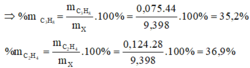
![]()
Đúng 1
Bình luận (0)
Cho 2,24 lit khí hidro cháy trong không khí ( ở nhiệt độ thích hợp )
. a, viết phương trình hóa học của phản ứng
b, số gam nước thu được sau phản ứng
c, tính thể tích không khí cần dùng ( các thể tích đo ở ĐKTC )
a, PT: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
b, Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{H_2O}=n_{H_2}=0,1\left(mol\right)\Rightarrow m_{H_2O}=0,1.18=1,8\left(g\right)\)
c, \(n_{O_2}=\dfrac{1}{2}n_{H_2}=0,05\left(mol\right)\Rightarrow V_{O_2}=0,05.22,4=1,12\left(l\right)\)
\(\Rightarrow V_{kk}=5V_{O_2}=5,6\left(l\right)\)
Đúng 2
Bình luận (1)
a. PTHH: 2H2 + O2 → 2H2O (không có nhập to được)
b. Số mol H2:
\(n_{H_2}=\dfrac{V}{22,4}=\dfrac{2,24}{22,4}=0,1\) (mol)
PT: 2H2 + O2 → 2H2O
Theo PT: 2 1 2 mol
Theo đề: 0,1 → 0,05 → 0,1 mol
Số gam nước thu được:
\(m_{H_2O}=n\cdot M=0,1\cdot18=1,8\left(g\right)\)
Thể tích không khí cần dùng:
\(V_{kk}=V_{O_2}=n\cdot22,4=1,12\left(l\right)\)
Đúng 1
Bình luận (0)
a. PTHH: \(2H_2+O_2-->2H_2O\)
b.\(n_{H_2}=\dfrac{V}{22,4}=\dfrac{2,24}{22,4}=0,1mol\)
\(=>n_{H_2O}=n_{H_2}=0,1mol\)\(=>m_{H_2O}=n.M=0,1.18=1,8g\)
c.\(n_{O_2}=\dfrac{1}{2}n_{H_2}=\dfrac{1}{2}.0,1=0,05mol\)
\(=>V_{O_2}=n.22,4=0,05.22,4=1,12l\text{í}t\left(dktc\right)\)
Đúng 1
Bình luận (0)




























