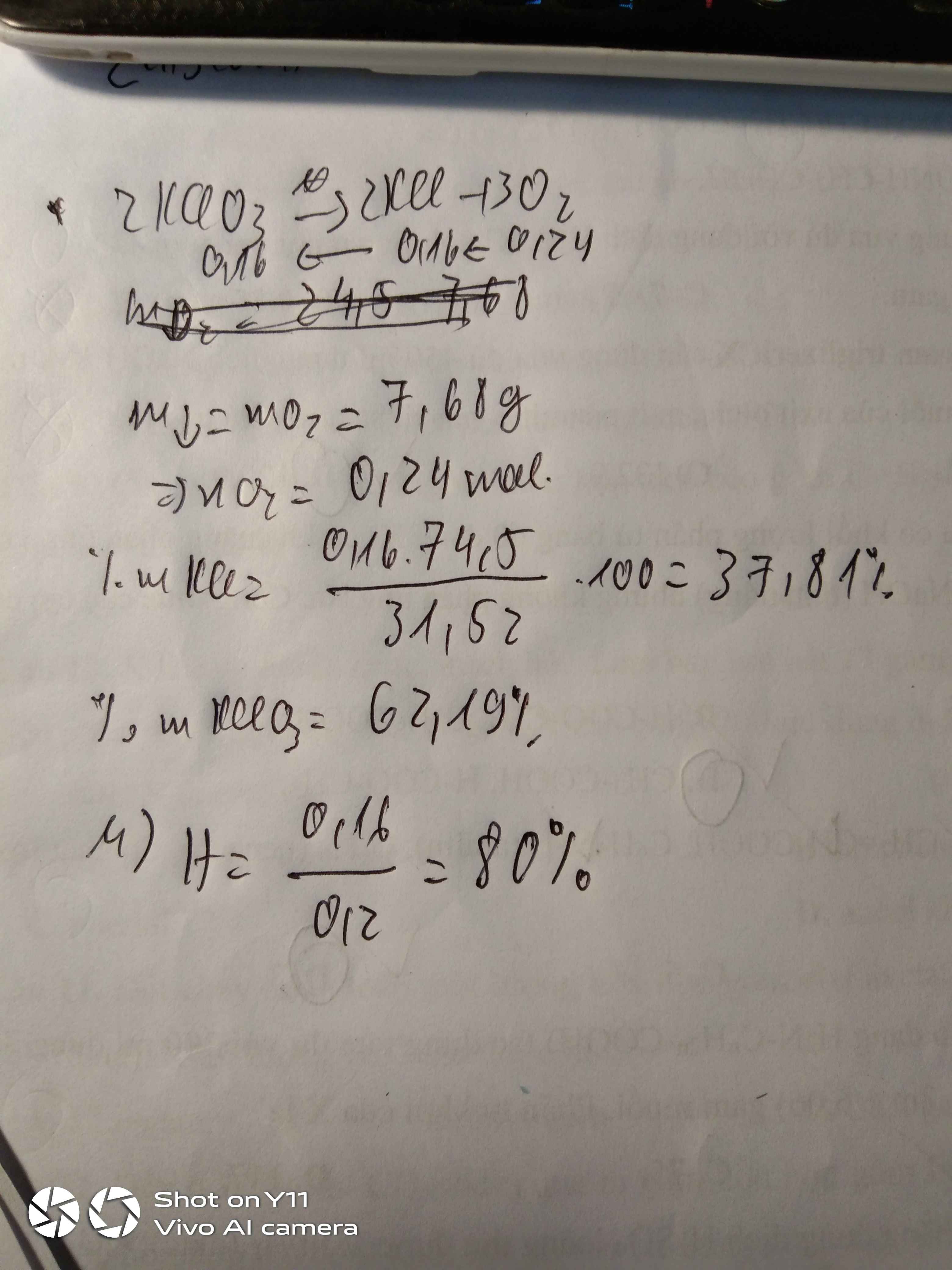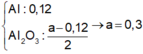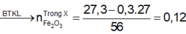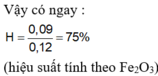Nhiệt phân 15,8 gam KMnO4 thu được hỗn hợp chất rắn X có khối lượng 14,52 gam. Tính hiệu suất phản ứng?

Những câu hỏi liên quan
1. Nhiệt phân 15,8 gam KMnO4
a, Nếu phản ứng 100% tính khối lượng chất rắn thu được sau phản ứng?
b, nếu hiệu suất phản ứng 80% tính khối lượng chất rắn thu được sau phản ứng
c, Tính hiệu suất phản ứng biết sau phản ứng thu được 14,68 gam chất rắn
$2KMnO_4\xrightarrow{t^o}K_2MnO_4+MnO_2+O_2$
$a\bigg)$
$n_{KMnO_4}=\frac{15,8}{158}=0,1(mol)$
Chất rắn sau p/ứ là $K_2MnO_4,MnO_2$
Theo PT: $n_{K_2MnO_4}=n_{MnO_2}=0,05(mol)$
$\to m_{\rm chất\, rắn}=0,05.197+0,05.87=14,2(g)$
$b\bigg)$
Vì $H=80\%\to n_{KMnO_4(p/ứ)}=0,1.80\%=0,08(mol)$
$\to n_{KMnO_4(dư)}=0,02(mol)$
Chất rắn sau p/ứ là $KMnO_4(dư):0,02;K_2MnO_4:0,04;MnO_2:0,04$
$\to m_{\rm chất\, rắn}=0,02.158+0,04.197+0,04.87=14,52(g)$
$c\bigg)$
Bảo toàn KL có:
$m_{O_2}=m_{KMnO_4}-m_{CR}$
$\to m_{O_2}=15,8-14,68=1,12(g)\to n_{O_2}=0,035(mol)$
Theo PT: $n_{KMnO_4(p/ứ)}=2n_{O_2}=0,07(mol)$
$\to H=\dfrac{0,07}{0,1}.100\%=70\%$
Đúng 1
Bình luận (0)
$2KMnO_4\xrightarrow{t^o}K_2MnO_4+MnO_2+O_2$
$a\bigg)$
$n_{KMnO_4}=\frac{15,8}{158}=0,1(mol)$
Chất rắn sau p/ứ là $K_2MnO_4,MnO_2$
Theo PT: $n_{K_2MnO_4}=n_{MnO_2}=0,1(mol)$
$\to m_{\rm chất\, rắn}=0,1.197+0,1.87=28,4(g)$
$b\bigg)$
Vì $H=80\%\to n_{KMnO_4(p/ứ)}=0,1.80\%=0,08(mol)$
$\to n_{KMnO_4(dư)}=0,02(mol)$
Chất rắn sau p/ứ là $KMnO_4(dư):0,02;K_2MnO_4:0,08;MnO_2:0,08$
$\to m_{\rm chất\, rắn}=0,02.158+0,08.197+0,08.87=25,88(g)$
$c\bigg)$
Bảo toàn KL có:
$m_{O_2}=m_{KMnO_4}-m_{CR}$
$\to m_{O_2}=15,8-14,68=1,12(g)\to n_{O_2}=0,035(mol)$
Theo PT: $n_{KMnO_4(p/ứ)}=2n_{O_2}=0,07(mol)$
$\to H=\dfrac{0,07}{0,1}.100\%=70\%$
Nhiệt phân 24,5 gam kali clorat KClO3 một thời gian thu được hỗn hợp rắn X có khối lượng giảm 7,68 gam so với khối lượng chất ban đầu .
a) Tính phần trăm khối lượng của mỗi chất trong hỗn hợp rắn X
b) Tính hiệu suất phản ứng nhiệt phân.
Nhiệt phân 79 gam thuốc tím. Sau phản ứng thu được hỗn hợp chất rắn X có khối lượng là 72,6 gam.
a. Tính hiệu suất của phản ứng.
Tính thành phần % khối lượng mỗi chất trong hỗn hợp X
\(n_{KMnO_4\left(pư\right)}=a\left(mol\right)\)
\(2KMnO_4\underrightarrow{^{^{t^0}}}K_2MnO_4+MnO_2+O_2\)
\(a............0.5a.........0.5a....0.5a\)
Bảo toàn khối lượng :
\(m_{O_2}=79-72.6=6.4\left(g\right)\)
\(\Rightarrow a=\dfrac{6.4}{32}:0.5=0.4\left(mol\right)\)
\(H\%=\dfrac{0.4\cdot158}{79}\cdot100\%=80\%\)
\(b.\)
\(m_{K_2MnO_4}=0.2\cdot197=39.4\left(g\right)\)
\(m_{MnO_2}=0.2\cdot87=17.4\left(g\right)\)
\(\%K_2MnO_4=\dfrac{39.4}{72.6}\cdot100\%=54.27\%\)
\(\%MnO_2=\dfrac{17.4}{72.6}\cdot100\%=23.97\%\)
\(\%KMnO_{4\left(dư\right)}=100-54.27-23.97=21.76\%\)
Đúng 3
Bình luận (0)
a)
Bảo toàn khối lượng : $m_{O_2} = 79 - 72,6 = 6,4(gam)$
$n_{O_2} = \dfrac{6,4}{32} = 0,2(mol)$
$2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2$
$n_{KMnO_4} = 2n_{O_2} = 0,4(mol)$
$H = \dfrac{0,4.158}{79}.100\% = 80\%$
b)
$n_{K_2MnO_4} = n_{MnO_2} = n_{O_2} = 0,2(mol)$
$\%m_{K_2MnO_4} = \dfrac{0,2.197}{72,6}.100\% = 54,27\%$
$\%m_{MnO_2} = \dfrac{0,2.87}{72,6}.100\% = 23,97\%$
$\%m_{KMnO_4} = 100\% -54,27\% - 23,97\% = 21,76\%$
Đúng 2
Bình luận (1)
Nung nóng 79 gam KMnO4 một thời gian thu được hỗn hợp chất rắn A nặng 74,2 gam.1) Tính hiệu suất phản ứng nhiệt phân.2) Cho A tác dụng với lượng dư axit HCl đặc, dẫn toàn bộ lượng khí tạo ra đi qua ống sứ đựng 29,6 gam hỗn hợp B gồm Fe, Cu. Sau khi các phản ứng hoàn toàn, thấy khối lượng chất rắn trong ống là 75,75 gam. Xác định % khối lượng mỗi chất có trong chất rắn còn lại trong ống sứ.
Đọc tiếp
Nung nóng 79 gam KMnO4 một thời gian thu được hỗn hợp chất rắn A nặng 74,2 gam.
1) Tính hiệu suất phản ứng nhiệt phân.
2) Cho A tác dụng với lượng dư axit HCl đặc, dẫn toàn bộ lượng khí tạo ra đi qua ống sứ đựng 29,6 gam hỗn hợp B gồm Fe, Cu. Sau khi các phản ứng hoàn toàn, thấy khối lượng chất rắn trong ống là 75,75 gam. Xác định % khối lượng mỗi chất có trong chất rắn còn lại trong ống sứ.
2KMnO4--->MnO2+O2+K2MnO4 (1)
theo bài ra ta có
nKMnO4= \(\frac{79}{158}=0,5\)(mol)
hỗn hợp chất rắn A gồm MnO2 và K2MnO4
theo phương trình (1) ta có
nMnO2= \(\frac{1}{2}x0,5\)= 0,25 (mol)
---> mMnO2= 0.25 x 87=21,75 (g)
nK2MnO4= \(\frac{1}{2}x0,5\)= 0,25 (mol)
----> m K2MnO4= 0,25 x 197=49,25 (g)
--->mA= 21,75+49,25=71 (g)
---> H%= \(\frac{71}{74,2}x100\%\approx95,69\%\)
2)
2) K2MnO4+8 HCl đặc----> 2Cl2+4H2O+2KCl+MnCl2 (2)
MnO2+4 HCl đặc ---> MnCl2 +Cl2+2 H2O (3)
khí thu được là Cl2
Cl2+ Cu-->CuCl2 (4)
3Cl2+2 Fe---> 2FeCl3 (5)
gọi số mol CuCl2 là x (x>0 ;mol)
--> mCucl2= 135x (g)
gọi số mol FeCl3 là y (y>0 ;mol)
---> n FeCl3=162,5 (g)
theo bài ra ta có 135x+162,5y=75,75( ** )
theo phương trình (4) ta có
nCu= nCuCl2=x(mol)
--> mCu= 64x (g)
theo phương trình (5) ta có
nFe=nFeCl3=y (mol )
--> mFe=56y (g)
theo bài ra ta có
64x+56y= 29,6 ( ** )
từ ( * ) và ( ** ) ta có hệ phương trình
\(\hept{\begin{cases}135x+162,5y=75,75\\64x+56y=29,6\end{cases}}\)
=> \(\hept{\begin{cases}x=0,2\\y=0,3\end{cases}}\)
=> mCuCl2= 0,2 x 135=27(g)
mFeCl3= 0,3 x 162,5= 48,75 (g)
LƯU Ý: bạn ghi ngoặc ở phép tính cuối và bạn tự giải phương trình hoặc liên hệ với mình
Nung 43,3 gam hỗn hợp gồm KMnO4 và KClO3. Sau một thời gian thu được khí X và chất rắn Y. Nguyên tố Mn chiếm 24,103% khối lượng chất rắn Y. Tính khối lượng của KMnO4 và KClO3 trong hỗn hợp ban đầu. Biết hiệu suất các phản ứng đều đạt 90%.
Gọi n KMnO4 = a
n KClO3 = b ( mol )
--> 158a + 122,5 b = 43,3
PTHH :
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\uparrow\)
0,9b 1,35b
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
0,9a 0,45a
\(\%Mn=\dfrac{55a}{43,3-32\left(0,45a+1,35b\right)}=24,103\%\)
\(\rightarrow a=0,15\)
\(b=0,16\)
\(m_{KMnO_4}=0,15.158=23,7\left(g\right)\)
\(m_{KClO_3}=0,16.122,5=19,6\left(g\right)\)
Đúng 3
Bình luận (0)
Hỗn hợp X gồm Al, Fe2O3 có khối lượng 27,3 gam. Tiến hành phản ứng nhiệt nhôm hỗn hợp X trong điều kiện không có không khí. Hòa tan hỗn hợp chất rắn sau phản ứng bằng dd NaOH dư thu được 4,032 lít H2 (đktc) và 14,88 gam chất rắn không tan. Hiệu suất của phản ứng nhiệt nhôm là: A. 60%. B. 80%. C. 75%. D. 71,43%.
Đọc tiếp
Hỗn hợp X gồm Al, Fe2O3 có khối lượng 27,3 gam. Tiến hành phản ứng nhiệt nhôm hỗn hợp X trong điều kiện không có không khí. Hòa tan hỗn hợp chất rắn sau phản ứng bằng dd NaOH dư thu được 4,032 lít H2 (đktc) và 14,88 gam chất rắn không tan. Hiệu suất của phản ứng nhiệt nhôm là:
A. 60%.
B. 80%.
C. 75%.
D. 71,43%.
Nhiệt phân hoàn toàn 99,95 gam hỗn hợp KMnO4 và KClO3 sau phản ứng thu đc 14,56 lít khí O2 ở đktc
a) Tính % theo khối lượng mỗi chất có trong hỗn hợp trước phản ứng
b) Tính % khối lượng mỗi chất rắn có trong hỗn hợp sau phản ứng
\(a)n_{KMnO_4} = a; n_{KClO_3} = b\Rightarrow 158a + 122,5b = 99,95(1)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ n_{O_2} = 0,5a +1,5b = \dfrac{14,56}{22,4}=0,65(2)\\ (1)(2)\Rightarrow a = 0,4 ; b = 0,3\\ \%m_{KMnO_4} = \dfrac{0,4.158}{99,95}.100\% = 63,23\%\\ \%m_{KClO_3} = 100\%-63,23\% = 36,77\%\)
\(n_{K_2MnO_4} = n_{MnO_2} = 0,5a = 0,2(mol)\\ n_{KClO_3} = b = 0,3(mol)\\ m_{hh\ sau\ pư} = 99,95 - 0,65.32 = 79,15(gam)\\ \%m_{K_2MnO_4} = \dfrac{0,2.197}{79,15}.100\% = 49,78\%\\ \%m_{MnO_2} = \dfrac{0,2.87}{79,15},100\% = 21,98\%\\ \%m_{KCl} = 28,24\%\)
Đúng 1
Bình luận (0)
![]() ko khó lém bn ơi có câu nèo easy hơm ko
ko khó lém bn ơi có câu nèo easy hơm ko![]()
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Al, Fe2O3 có khối lượng 21,67 gam. Tiến hành phản ứng nhiệt nhôm hỗn hợp X trong điều kiện không có không khí. Hòa tan hoàn toàn hỗn hợp chất rắn sau phản ứng bằng dung dịch NaOH dư thu được 2,016 lít H2 (đktc) và 12,4 gam chất rắn không tan. Hiệu suất của phản ứng nhiệt nhôm là: A. 60% B. 71,43% C. 80% D. 75%
Đọc tiếp
Hỗn hợp X gồm Al, Fe2O3 có khối lượng 21,67 gam. Tiến hành phản ứng nhiệt nhôm hỗn hợp X trong điều kiện không có không khí. Hòa tan hoàn toàn hỗn hợp chất rắn sau phản ứng bằng dung dịch NaOH dư thu được 2,016 lít H2 (đktc) và 12,4 gam chất rắn không tan. Hiệu suất của phản ứng nhiệt nhôm là:
A. 60%
B. 71,43%
C. 80%
D. 75%
Đáp án D
2 Al + Fe 2 O 3 → t o Al 2 O 3 + 2 Fe
Hỗn hợp sau phản ứng gồm A12O3, Fe, Al và Fe2O3.
Khi cho hỗn hợp vào dung dịch NaOH dư thì chỉ có Al và A12O3 tan, chất rắn còn lại gồm Fe và Fe2O3

Đúng 0
Bình luận (0)
Hỗn hợp X gồm Al,
Fe
2
O
3
có khối lượng 40,1 gam. Tiến hành phản ứng nhiệt nhôm hỗn hợp X trong điều kiện không có không khí. Hòa tan hoàn toàn hỗn hợp chất rắn sau phản ứng bằng dung dịch NaOH dư thu được 4,032 lít
H
2
(đktc) và 27,68 gam chất rắn không tan. Hiệu suất của phản ứng nhiệt nhôm là: A. 80% B. 75% C. 60% D. 71,43%
Đọc tiếp
Hỗn hợp X gồm Al, Fe 2 O 3 có khối lượng 40,1 gam. Tiến hành phản ứng nhiệt nhôm hỗn hợp X trong điều kiện không có không khí. Hòa tan hoàn toàn hỗn hợp chất rắn sau phản ứng bằng dung dịch NaOH dư thu được 4,032 lít H 2 (đktc) và 27,68 gam chất rắn không tan. Hiệu suất của phản ứng nhiệt nhôm là:
A. 80%
B. 75%
C. 60%
D. 71,43%