Cho 20g một oxit sắt phản ứng với dd HCl,sau phản ứng thu đc 40,625g muối clorua .Xác định CTHH của oxit

Những câu hỏi liên quan
Cho 20g một oxit sắt phản ứng với dd HCl,sau phản ứng thu đc 40,625g muối clorua .Xác định CTHH của oxit
Gọi CTHH là FexOy
56x + 16y = 20 (1)
PTHH: FexOy + 2yHCl -> xFeCl2y/x + yH2O
=> 56x + 71y = 40,625 (2)
(1)(2) => x = 0,25; y = 0,375
=> x/y = 0,25/0,375 = 2/3
Vậy CTHH là Fe2O3
Đúng 2
Bình luận (0)
Cho 20g một oxit sắt phản ứng hết với dung dịch HCl dư, sau phản ứng thu được 40,625g muối clorua. Xác định công thức phân tử của oxit sắt.
Gọi công thức hóa học của oxit sắt là F e x O y
PTHH của phản ứng là:
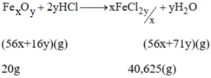
Theo PTHH ta có:
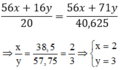
Vậy công thức hóa học của oxit sắt là F e 2 O 3
Đúng 0
Bình luận (0)
cho 20g 1 oxit sắt phản ứng với dung dịch HCl sau phản ứng thu được 40,625g muối clorua . Xác định CTPT của Oxit sắt
cho 20g 1 oxit sắt phản ứng với dung dịch HCl sau phản ứng thu được 40,625g muối clorua . Xác định CTPT của Oxit sắt
Cho 1 lượng oxit kim loại tác dụng vừa đủ với 100g dd HCl 21,9%, sau phản ứng thu được dd muối clorua có nồng độ 24,23%. Xác định CTHH của oxit kim loại.
Giải giúp em 3 bài này với ạ!1. Cho 1,625g muối sắt clorua tác dụng hết với dd AgNO3 thu được 4,035 kết tủa. Xác định CTHH của muối sắt clorua2. Đun nóng a gam 1 oxit sắt trong ống chưa khí CO,sau phản ứng thu được 3,36l.a) Tính VCOb) Tìm ac) Xác định CTHH của oxit sắt3. Xác định CTHH của oxit sắt Biết rằng khi hòa tan 7,2g oxit phải cần 69,52l dd HCl 10%, có khối lượn riêng là 1,05g
Đọc tiếp
Giải giúp em 3 bài này với ạ!
1. Cho 1,625g muối sắt clorua tác dụng hết với dd AgNO3 thu được 4,035 kết tủa. Xác định CTHH của muối sắt clorua
2. Đun nóng a gam 1 oxit sắt trong ống chưa khí CO,sau phản ứng thu được 3,36l.
a) Tính VCO
b) Tìm a
c) Xác định CTHH của oxit sắt
3. Xác định CTHH của oxit sắt Biết rằng khi hòa tan 7,2g oxit phải cần 69,52l dd HCl 10%, có khối lượn riêng là 1,05g
Bài 3: Khối lượng dung dịch HCl là: 69,52 . 1,05 = 73 gam
Khối lượng chất tan HCl là: 73 . 10% = 7,3 gam
Gọi CTHH của ôxit sắt là: FexOy
PTHH: FexOy + 2yHCl → xFeCl\(\frac{2y}{x}\) + yH2O
Số mol của FexOy là: 7,2 : (56x+16y) mol
Số mol của HCl là: 7,3 : 36,5 = 0,2 mol
Số mol của FexOy tính theo HCl là: 0,2:2y = 0,1:y mol
=> 7,2:(56x+16y) = 0,1y <=> 7,2y = 5,6x + 1,6y
<=> 5,6y = 5,6x => x:y = 1:1
Vậy CTHH của ôxit sắt là: FeO
Đúng 0
Bình luận (0)
Hòa tan hết 10,8 g một oxit sắt vào dd HCl .Sau phản ứng ta thu dc 19 05 g muối sắt clorua .Xác định CTHH của oxit sắt
PTPU : FexOy + HCl -> muối sắt clorua + H2O
gọi a là số mol HCl => số mol H2O = a/2
m(muối) - m(oxit) = m(HCl) - m(H2O)
<=>19,05 - 10,8 = 36,5a - 9a
=> a = 0,3
từ đó suy ra số mol nguyên tử O có trong nước =a/2 = số mol nguyên tử O có trong oxit = 0,15
=> m(O) = 2,4 g
m (Fe) có trong oxit = 10,8 - 2,4 = 8,4 (g)
nFe = 8,4/56 = 0.15 (mol )
lập tỉ lệ số mol
\(\dfrac{Fe}{O}=\dfrac{0,15}{0,15}=\dfrac{1}{1}\)
vậy oxit là FeO
Đúng 0
Bình luận (0)
Gọi CTHH oxit sắt là FexOy
gọi a là số mol HCl
FexOy + 2yHCl -> xFeCl\(\dfrac{2y}{x}\) + yH2O
(mol) a/2y a a/2
Áp dụng định luật bảo toàn khối lượng
mFexOy + mHCl = mFeCl\(\dfrac{2y}{x}\)+ mH2
10.8+ 36,5a = 19.05 + 9a
27.5a = 8.25
a = 0.3
nFexOy = a/2y = 0.3/2y = 0.15/y
mFexOy = n.M
10.8 = 0.15/y(56x + 16y)
10.8=8.4x/y + 2.4
8.4 = 8.4x/y
x/y = 1/1
CTHH của oxit sắt FeO
Đúng 0
Bình luận (0)
dùng 2,106 lít h2 để phản ứng vừa đủ vs 5,6g hh X gồm đồng(2) oxit và 1 oxit sắt. sau phản ứng thu được m gam chất rắn y. cho 3/4 lượng y vào dd hcl thì thu đc 672 ml khí(đktc). xác định CTHH của oxit sắt ban đầu
Cho 9,4 gam oxit kim loại A có hóa trị I phản ứng hết với dung dịch axit clohidđric HCl, sau phản ứng thu được nước và 14,9 gam muối clorua (tạo bởi kim loại liên kết với clo). Xác định CTHH của oxit kim loại A
\(n_{A_2O}=\dfrac{9,4}{2M_A+16}\left(mol\right)\)
PTHH: A2O + 2HCl --> 2ACl + H2O
\(\dfrac{9,4}{2M_A+16}\)-->\(\dfrac{9,4}{M_A+8}\)
=> \(\dfrac{9,4}{M_A+8}\left(M_A+35,5\right)=14,9\Rightarrow M_A=39\left(g/mol\right)\)
=> A là K
CTHH: K2O
Đúng 2
Bình luận (0)




















