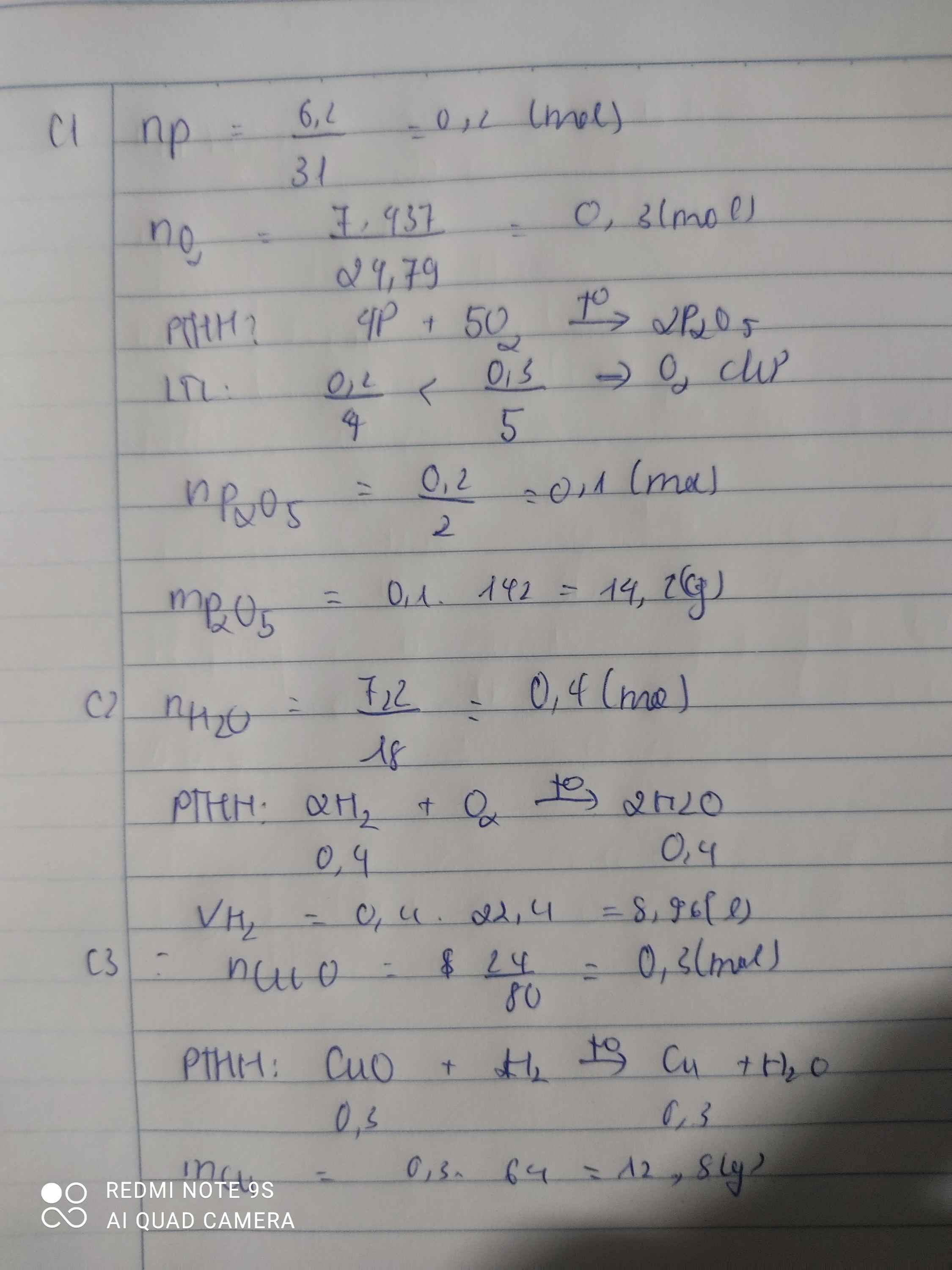Đốt cháy hoàn toàn Phosphorus trong bình chứa 2,479 lit Oxygen (đkc) thu được hơp chất có công thức P2O5. Tính khối lượng sản phẩm thu được.

Những câu hỏi liên quan
Bài 6 Đốt cháy 16,8 gam sắt trong bình chứa 6,72 lit oxi (đktc) thu được oxit sắt từ.a. Viết PTHH?b. Tính khối lượng sản phẩm thu được?Bài 7: Đốt cháy hoàn toàn Photpho trong bình chứa 1,12 lit oxi (dktc) thu được hợp chất có công thức P2O5.a. Viết phương trình hóa học? b. Tính khối lượng sản phẩm thu được?c. Tính khối lượng Kali clorat KC1O, cần dùng để điều chế được lượng oxi dùng cho phản ứng trên?
Đọc tiếp
<Bài 6 Đốt cháy 16,8 gam sắt trong bình chứa 6,72 lit oxi (đktc) thu được oxit sắt từ.
a. Viết PTHH?
b. Tính khối lượng sản phẩm thu được?
Bài 7: Đốt cháy hoàn toàn Photpho trong bình chứa 1,12 lit oxi (dktc) thu được hợp chất có công thức P2O5.
a. Viết phương trình hóa học? b. Tính khối lượng sản phẩm thu được?
c. Tính khối lượng Kali clorat KC1O, cần dùng để điều chế được lượng oxi dùng cho phản ứng trên?
Xem thêm câu trả lời
Bài 1 : Đốt cháy 6,2 gam phosphorus trong bình chứa 7,437lít (đkc) khí oxygen, thu được diphosphorus pentaoxide (P2O5). Tính khối lượng P2O5 tạo thành.
Bài 2: Khí H2 cháy trong khí O2 tạo nước. Tính thể tích khí H2 (đkc) cần dùng để thu được 7,2 gam nước.
Bài 3: Cho 24 gam CuO tác dụng hoàn toàn với khí H2 đun nóng, thu được m gam đồng (Cu). Tính giá trị của m.
Đốt cháy hoàn toàn 6,2g Phosphorus (P) trong khí Oxygen (O2) thu được điphosphorus pentoxide (P2O5).
a, tính khối lượng P2O5
b, Biết rằng trong thực tế khi đốt cháy lượng Phosphorus trên chỉ thu được 12,75g điPhosphorus pentoxide (P2O5) tính hiệu suất phản ứng trên
-Giúp mình với ạ, mình sắp thi rồi-
\(a,n_P=\dfrac{6,2}{31}=0,2mol\\ 4P+5O_2\xrightarrow[]{t^0}2P_2O_5\\ n_{P_2O_5}=\dfrac{0,2.2}{4}=0,1mol\\ m_{P_2O_5\left(lt\right)}=0,1.142=14,2g\\ b,H=\dfrac{12,75}{14,2}\cdot100\%\approx89,79\%\)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 12,4 gam phosphorus P trong bình chứa khí Oxygen O2 tạo thành diphosphorus pentaoxide P2O5. a)tính khối lượng diphosphorus pentaoxide thu được
b) Tính thể tích oxygen(đktc) đã tham gia phản ứng
Ta có: \(n_P=\dfrac{12,4}{31}=0,4\left(mol\right)\)
PT: \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
_____0,4____0,5_____0,2 (mol)
a, \(m_{P_2O_5}=0,2.142=28,4\left(g\right)\)
b, \(V_{O_2}=0,5.22,4=11,2\left(l\right)\)
Đúng 4
Bình luận (4)
Đốt cháy hoàn toàn 6,2 gam phosphorous trong bình đựng khí oxygen. Hãy: a. Tính khối lượng sản phẩm thu được. b. Tính thể tích khí oxygen (đkc) cần dùng. Biết P=31; O=16
4P+5O2-to>2P2O5
0,2-----0,25----0,1
n P=\(\dfrac{6,2}{31}\)=0,2 mol
=>VO2=0,25.24,79=6,1975l
=>m P2O5=0,1.142=14,2g
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 6,2 gam phosphorus trong không khí, ta thu đc 14,2 gam hợp chất P2O5
a) viết phương trình hóa học của phản ứng
b) viết công thức về khối lượng cho phản ứng trên
c) tính khối lượng khí oxygen đã tham gia phản ứng
a) PTHH: 4P + 5O2 -> 2P2O5
b,c) ĐLBTKL
\(m_P+m_{O_2}=m_{P_2O_5}\\ m_{O_2}=14,2-6,2=8\left(g\right)\)
Đúng 1
Bình luận (0)
a, 4P + 5O2 \(\underrightarrow{t^o}\) 2P2O5
b, Theo ĐLBTKL, ta có:
mP + mO\(_2\) = m\(P_2O_5\)
c, \(\Rightarrow m_{O_2}=14,2-6,2=8g\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 12,4 gam Photpho trong bình chứa khí oxi, thu được hợp chất điphotpho pentaoxit P2O5
a. Viết chương trình hóa học
B. Tính khối lượng sản phẩm thu được
C. Tính thể tích oxi cần dùng (đktc)
D. Tính khối lượng KClO3 cần dùng để khi phân hủy thì thu được một thể tích khí O2 (ở đktc) bằng với thể tích khí O2 đã sử dụng ở phản ứng trên
giúp mình bài này với mình cảm ơn
Đọc tiếp
Đốt cháy hoàn toàn 12,4 gam Photpho trong bình chứa khí oxi, thu được hợp chất điphotpho pentaoxit P2O5 a. Viết chương trình hóa học B. Tính khối lượng sản phẩm thu được C. Tính thể tích oxi cần dùng (đktc) D. Tính khối lượng KClO3 cần dùng để khi phân hủy thì thu được một thể tích khí O2 (ở đktc) bằng với thể tích khí O2 đã sử dụng ở phản ứng trên giúp mình bài này với mình cảm ơn
a, \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
b, \(n_P=\dfrac{12,4}{31}=0,4\left(mol\right)\)
Theo PT: \(n_{P_2O_5}=\dfrac{1}{2}n_P=0,2\left(mol\right)\Rightarrow m_{P_2O_5}=0,2.142=28,4\left(g\right)\)
c, \(n_{O_2}=\dfrac{5}{4}n_P=0,5\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,5.22,4=11,2\left(l\right)\)
d, \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
Theo PT: \(n_{KClO_3}=\dfrac{2}{3}n_{O_2}=\dfrac{1}{3}\left(mol\right)\Rightarrow m_{KClO_3}=\dfrac{1}{3}.122,5=\dfrac{245}{6}\left(g\right)\)
Đúng 3
Bình luận (1)
Đốt cháy hoàn toàn hợp chất hữu cơ Y cần dùng 16,8(lit) O2 thu được CO2, H2O ,N2 . Cho hoàn toàn sản phẩm thu được qua dung dịch Ca(OH)2 dư thu được 60g kết tủa đồng thời khối lượng bình giảm 21g và có 2,24(lit) khí thoát ra khỏi bình (đktc).
Tìm công thức phân tử của Y biết công thức phân tử trùng với công thức đơn giản nhất.
\(Đăt:n_{CO_2}=a\left(mol\right),n_{H_2O}=b\left(mol\right)\)
\(BTNTO:\\ 2n_{O_2}=2n_{CO_2}+n_{H_2O}\\ \Leftrightarrow2a+b=0.75\left(1\right)\)
\(m_{bìnhgiảm}=m_{CaCO_3}-\left(m_{CO_2}+m_{H_2O}\right)=21\left(g\right)\)
\(\Leftrightarrow44a+18b=60-21=39\left(g\right)\left(2\right)\)
Bạn xem lại đề nha
Đúng 1
Bình luận (0)
\(n_{CO_2} = n_{CaCO_3} = 0,6(mol)\)
\(m_{tăng} = n_{CO_2} + m_{H_2O} - m_{CaCO_3}\\ \Rightarrow n_{H_2O} = \dfrac{60-21-0,6.44}{18} = 0,7(mol)\)
\(n_{N_2} = n_{khí\ thoát\ ra} = 0,1(mol)\)
\(n_{O_2} =0,75(mol)\)
BTNT với C,H,O và N :
\(n_C = n_{CO_2} = 0,6\\ n_H = 2n_{H_2O} = 0,7.2 = 1,4(mol)\\ n_N = 2n_{N_2} = 0,2(mol)\\ n_O = 2n_{CO_2} + n_{H_2O} -2n_{O_2}= 0,4(mol)\)
Ta có :
\(n_C : n_H : n_O : n_N = 0,6 : 1,4 : 0,4 : 0,2 = 3 : 7 :2 : 1\)
Vậy CTPT của Y :C3H7O2N
Đúng 1
Bình luận (0)
Người ta đun nóng hết 47,4 gam KMnO4 để thu khí oxygen.
a) Tính thể tích khí oxygen thu được (đkc).
b) Dùng toàn bộ lượng oxygen trên đốt cháy hoàn toàn m gam Al. Tính khối lượng Al tham gia phản ứng và khối lượng sản phẩm thu được. K = 39, Mn = 55, O = 16, Al = 27.
a. \(n_{KMnO_4}=\dfrac{47.4}{158}=0,3\left(mol\right)\)
PTHH : 2KMnO4 ---to----> K2MnO4 + MnO2 + O2
0,3 0,15
\(V_{O_2}=0,15.22,4=3,36\left(l\right)\)
b. PTHH : 4Al + 3O2 -> 2Al2O3
0,2 0,15
\(m_{Al}=0,2.27=5,4\left(g\right)\)
Đúng 5
Bình luận (1)