Tìm công thức hóa học đơn giản nhất của hợp chất A biết rằng trong A có 7 g sắt kết hợp với 3 g oxi.

Những câu hỏi liên quan
Hãy tìm công thức hóa học đơn giản nhất của một loại oxit của lưu huỳnh, biết rằng trong oxit này có 2 g lưu huỳnh kết hợp với 3 g oxi.
\(\frac{n_S}{n_O}=\frac{\frac{2}{32}}{\frac{3}{16}}=\frac{1}{3}\Rightarrow SO_3\)
Đúng 0
Bình luận (1)
Giả sử CTHH là SxOy , ta có tỉ lệ:
\(\dfrac{x}{y}\)=\(\dfrac{2}{32}\):\(\dfrac{3}{16}\)=\(\dfrac{1}{3}\)⇒CTHH là SO3
Đúng 0
Bình luận (1)
Giả sử CTHH là SxOy , ta có tỉ lệ:
xyxy=232232:316316=1313⇒CTHH là SO3
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Hãy tìm công thức hóa học đơn giản nhất của một loại oxit của lưu huỳnh, biết rằng trong oxit này có 2g lưu huỳnh kết hợp với 3g oxi.
Số mol của nguyên tử lưu huỳnh là: 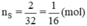
Số mol của nguyên tử oxi là: 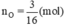
Ta có: 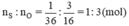
⇒ Trong một phân tử lưu huỳnh trioxit có 1 nguyên tử S và có 3 nguyên tử O.
Vậy công thức hóa học đơn giản nhất của oxit lưu huỳnh là SO3.
Đúng 0
Bình luận (0)
Tìm công thức hóa học của một oxit sắt biết trong hợp chất, cứ 7 phần khối lượng sắt kết hợp với 2 phần khối lượng oxi
Ta có: \(\dfrac{m_{Fe}}{m_O}=\dfrac{7}{2}\Rightarrow\dfrac{56n_{Fe}}{16n_O}=\dfrac{7}{2}\Rightarrow\dfrac{n_{Fe}}{n_O}=\dfrac{1}{1}\)
Vậy: CTHH của oxit sắt là FeO.
Đúng 1
Bình luận (0)
Công thức hoá học đơn giản nhất của một loại oxit của sắt, biết rằng trong oxit này có 7 gam sắt kết hợp với 2 gam oxi.
A. FeO B. Fe2O3 C. Fe3O4 D. Không có.
Gỉai bài này hộ mình với:hãy tìm công thức hóa học đơn giản nhất của 1 loại oxit sắt ,bít trong oxit này có 7 phần khối lượng của Fe kết hợp với 2 phần khối lượng oxit
Gọi công thức oxit sắt là FexOy
Do Fe chiếm 7 phần trong Oxit , Oxi chiếm 2 phần , Suy ra :
=> (56x/7)*2 = 16x = 16y
<=> x=y => x = y chỉ có thể bằng 1
Được rồi nhé bạn !!
Đúng 0
Bình luận (1)
Đốt cháy hoàn toàn 2,3 g hợp chất A thu được 4,4 g CO2 và 2,7 g hơi nước công thức hóa học của a là gì viết công thức hóa học của A trùng với công thức đơn giản
CTHH của A gồm C và H và có thể có O
\(n_C=n_{CO_2}=\dfrac{4,4}{44}=0,1mol\)
\(n_H=2.n_{H_2O}=2.\dfrac{2,7}{18}=0,3mol\)
\(n_O=\dfrac{2,3-\left(0,1.12+0,3.1\right)}{16}=0,05mol\)
\(CTHH:C_xH_yO_z\)
\(x:y:z=0,1:0,3:0,05=2:6:1\)
\(\Rightarrow CTHH:C_2H_6O\)
Đúng 1
Bình luận (0)
Một loại oxi sắt có thành phần là: 7 phần khối lượng sắt kết hợp với 3 phần khối lượng oxi. Em hãy cho biết: Công thức phân tử của oxit sắt, biết công thức phân tử cũng chính là công thức đơn giản.
Giả sử khối lượng oxit là 10g ⇒ m F e = 7g ; m O = 3g
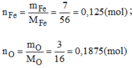
Vậy: 0,125 mol nguyên tử Fe kết hợp với 0,1875 mol nguyên tử O.
Suy ra 2 mol nguyên tử Fe kết hợp với 3 mol nguyên tử O (vì số nguyên tử luôn là số nguyên).
→ Công thức hóa học đơn giản của oxit sắt là: F e 2 O 3
Đúng 0
Bình luận (0)
Hãy tìm công thức hóa học đơn giản nhất của một loại oxit của lưu huỳnh, biết rằng trong oxit này có 2 g lưu huỳnh kết hợp với 3 g oxi.
Số mol của nguyên tử lưu huỳnh là: nS = (mol)
Số mol của nguyên tử oxi là: =
mol
Ta có: =
:
=
Vậy công thức hóa học đơn giản nhất của oxit lưu huỳnh là SO3
Đúng 0
Bình luận (1)
Số mol của nguyên tử lưu huỳnh là: nS = (mol)
Số mol của nguyên tử oxi là: =
mol
Ta có: =
:
=
Vậy công thức hóa học đơn giản nhất của oxit lưu huỳnh là SO3
Đúng 1
Bình luận (1)
Gọi công thức lưu huỳnh oxi là: SxOy
Ta có tỉ lệ:
x ÷ y = 2/32÷3/16=0,0625:0,1825=1:3
-> Công thức hóa học là: SO3
Đúng 1
Bình luận (2)
Xem thêm câu trả lời
Khi đốt cháy P trong khí oxi người ta thấy cứ 1 gam P kết hợp đủ với khoảng 1,29 gam khí oxi tạo ra một hợp chất A duy nhất . Xác định công thức hóa học của A và hóa trị của P trong hợp chất , biết rằng phân tử A có 2 nguyên tử P
( ko dùng mol tại em chưa học ạ )
$n_P = \dfrac{1}{31}(mol)$
$n_{O_2} = \dfrac{1,29}{32} \Rightarrow n_O = 2n_{O_2} = \dfrac{2,58}{32}(mol)$
Suy ra :
$n_P : n_O = \dfrac{1}{31} : \dfrac{2,58}{32} = 2 :5$
Vậy A là $P_2O_5$
hóa trị của P : hóa tri V
Đúng 5
Bình luận (3)

























