axit clohidric ( HCL ) tác dụng với Magie cacbonat ( MgCO3 ) theo sơ đồ phản ứng sau :
HCL + MgCO3 ---> MgCl2 + CO2 + H2O
tính nồng độ % chất tan có trong dung dịch sau phản ứng khi có 100g dung dịch HCl 14,6% tác dụng với 50 g MgCO3
Cho 4,8 gam kim loại magie tác dụng với 250ml dung dịch axit clohidric (HCl) 2M thì thu được magie clorua (MgCl2) và khí hidro. Tính nồng độ mol của các chất có trong dung dịch thu được sau phản ứng? Cho rằng thể tích dung dịch thay đổi không đáng kể.
A. MgCl2: 0,8M B. MgCl2: 0,8M; HCl: 0,4M
C. HCl: 0,4M D. MgCl2: 0,4M; HCl: 0,8M
Giúp e với ạ, e đang cần gấp ạ. Em cảm ơn ạ
Cho một lượng bột CaCO3 tác dụng hoàn toàn với dung dịch HCl 32,85%. Sau phản ứng thu được dung dịch X trong đó nồng độ HCl còn lại 24,2%. Thêm vào X một lượng bột MgCO3, khuấy đều cho phản ứng xảy ra hoàn toàn thu được dung dịch Y trong đó nồng độ dung dịch HCl bằng 21,10%. Nồng độ % của dung dịch CaCl2 và MgCl2 lần lượt là:
A. 11,35% và 3,54%
B. 11,35% và 4,54%
C. 10,35% và 3,04%
D. 10,35% và 3,54%
Đáp án D
Giả sử có 100 gam dung dịch HCl 32,85% thì khối lượng HCl là 32,85 gam.
nHCl= 32 , 85 36 , 5 = 0,90 mol
- Gọi số mol của CaCO3 là x (mol). Phản ứng:
CaCO3 + 2HCl → CaCl2 + H2O + CO2 (1)
x 2x x x
Từ (1) và đề ra: nHCldư = (0,90 - 2x) mol
Khối lượng dung dịch X sau phản ứng (1): 100 + 100x – 44x = (100 + 56x) gam
Theo đề ra: C%HCl = ( 0 , 90 - 2 x ) . 36 , 5 100 + 56 x . 100 % = 24,195% => x = 0,1 mol
Vậy sau p/ư (1) nHCl còn lại = 0,7mol
- Cho MgCO3 vào dung dịch X, có p/ư:
MgCO3 + 2HCl → MgCl2 + H2O + CO2 (2)
y 2y y y
Sau p/ư (2) nHCl dư = 0,7-2y
Khối lượng dung dịch Y là: (105,6 + 84y - 44y) gam hay (105,6 + 40y) gam
Từ (2) và đề ra: C%HCl trong Y = ( 0 , 7 - 2 y ) . 36 , 5 105 , 6 + 40 y . 100% = 21,11% => y = 0,04 mol
Dung dịch Y chứa 2 muối CaCl2, MgCl2 và HCl dư:
C%(CaCl2) = 0 , 1 . 111 107 , 2 . 100 % = 10 , 35 %
C%(MgCl2) = 0 , 04 . 95 107 , 2 . 100 % = 3 , 54 %
Hòa tan m(g) Magie Cacbonat MgCO3 và dung dịch HCL dư. Sau phản ứng thu được 1,12(l) khí Oxi ở đktc, muối MgCl2 và nước. Dẫn khí CO2 sinh ra qua dung dịch Ca(OH)2 thu được kết tủa CaCO3 và H2O
a) Viết các phản ứng xảy ra
b) Tính m.
c) Tính khối lượng kết tủa CaCO3
Sau phản ứng thu được O2?
hòa tan magie trang dung dịch axit clohidric HCL thu được 4,48 lít khí: a) tính khối axit clohidric HCL đã tham gia phản ứng. b) cô cạn dung dịch sau phản ứng thu được m gam chất rắn màu trắng là magie clrua MgCL2. Tính m
\(n_{H_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(...........0.4.....0.2...0.2\)
\(m_{HCl}=0.4\cdot36.5=14.6\left(g\right)\)
\(m_{MgCl_2}=0.2\cdot111=22.2\left(g\right)\)
Cho một lượng tinh bột CaCO3 tác dụng hoàn toàn với dung dịch HCl 32,85%. Sau phản ứng thu được dung dịch X trong đó nồng độ HCl còn lại là 24,20%. Thêm vào X một lượng bột MgCO3 khuấy đều cho phản ứng xảy ra hoàn toàn thu được dung dịch Y trong đó nồng độ HCl còn lại là 21,10%. Nồng độ phần trăm MgCl2 trong dung dịch Y là:
A. 12,35%
B. 3,54%
C. 10,35%
D. 8,54%
Đáp án B
Chọn 1 mol HCl ban đầu. Gọi n C a C O 3 = x
Có phản ứng: C a C O 3 + 2 H C l → C a C l 2 + C O 2 + H 2 O (1)
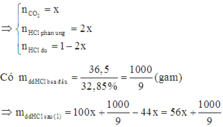
Do đó nồng độ phần trăm của HCl sau phản ứng (1) là:
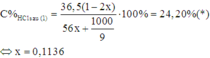
Do đó sau phản ứng (1) dung dịch X có mx = 117,47; nHCl dư = 0,7728
Gọi n M g C O 3 = y . Có phản ứng:
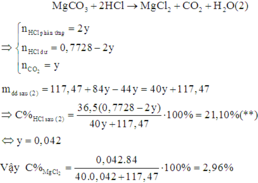
Do trong quá trình tính toán, ta có nhiều bước làm tròn nên dẫn đến sai số.
Khi đó ta sẽ chọn đáp án gần với kết quả tính được nhất.
Có pt 2Hcl+MgCO3→MgCl2+Co2+H2O
Tính mMgCl2 thu được khi cho 8,4g MgCO3 tác dụng với HCL dư
Tính V CO2 thu được ở dktc nếu có 7,3g HCL tham gia phản ứng
Thu Khí CO2 bằng cách đặt đứng bình hay ngược binh?Vì Sao
PTHH: MgCO3 +2 HCl -> MgCl2 + CO2 + H2O
a) nMgCO3=8,4/84=0,1(mol)
=> nMgCl2=nMgCO3=0,1(mol) => mMgCl2=0,1.95=9,5(g)
b) nHCl=7,3/36,5=0,2(mol)
=> nCO2= 1/2. nHCl=1/2. 0,2=0,1(mol) => V(CO2,đktc)=0,1.22,4=2,24(l)
c) Thu khí CO2 ta thu bằng cách đặt đứng bình vì khí CO2 là khí nặng hơn không khí (44>29)
Cho một lượng bột CaCO3 tác dụng hoàn toàn với dung dịch HCl 25,55%. Sau phản ứng thu được dung dịch X trong đó nồng độ HCl còn lại là 17,28%. Thêm vào dung dịch X một lượng bột MgCO3 khuấy đều cho phản ứng xảy ra hoàn toàn thu được dung dịch Y trong đó nồng độ HCl còn lại là 13,56%. Nồng độ phần trăm của MgCl2 trong dung dịch Y gần nhất với:
A. 5,2%.
B. 4,2%.
C. 5,0%.
D. 4,5%.
câu 1: cho 2,4 magie tác dụng với dung dịch axit clohdric HCL , sau phản ứng thu được 9,5g magie clorua MgCl2 và 0,2g khí hidro
a) Viết phương trình phản ứng trên
b) Áp dụng định luật bảo toàn khối lượng, hãy tính khối lượng axit clohidric HCL đã phản ứng
câu 2 : cho 13g kẽm tác dụng hoàn toàn với 14,6g axit clohidric (HCL) sau phản ứng thu được muối kẽm clorua (ZnCl2) và 0,4 khí hidro
a. Viết phương trình hóa học
b. tính khối lượng muối kẽm clorua (ZnCl2) thu được
Mọi người giải giúp mình với
Câu 1:
\(a,PTHH:Mg+2HCl\to MgCl_2+H_2\\ b,m_{Mg}+m_{HCl}=m_{MgCl_2}+m_{H_2}\\ \Rightarrow m_{HCl}=9,5+0,2-2,4=7,3(g)\)
Câu 2:
\(a,PTHH:Zn+2HCl\to ZnCl_2+H_2\\ b,m_{Zn}+m_{HCl}=m_{ZnCl_2}+m_{H_2}\\ \Rightarrow m_{ZnCl_2}=13+14,6-0,4=27,2(g)\)
cho một lượng muối magie cacbonat tác dụng vừa đủ với 200ml dung dịch HCl 0,5M.Hãy tính nồng độ mol của các chất trong dung dịch khi phản ứng kết thúc