| stt | tên thí nghiệm | cách tiến hành | hiện tượng | giải thích | chú thích |
|---|---|---|---|---|---|
| 1 | cacbon khử đồng(2) oxit ở nhiệt độ cao | ||||
2 | nhiệt phân muối NaHCO3 | ||||
| 3 | phân biệt muối cacbonat và muối clrua |
cách tiến hành vẽ hình nha
mn giúp mình với
Viết các phương trình hóa học cho mỗi hiện tượng hóa học sau ghi rõ điều kiện nếu có a. phân biệt muối kali pemanganat b. Oxi hóa kim loại đồng ở nhiệt độ cao c. Khử sắt từ oxit bằng khí hidro ở nhiệt độ cao
a, Muối kali pemanganat có màu tím
b, $Cu+O_2\rightarrow CuO$ (Kim loại chuyển từ màu đỏ thành màu đen)
$Fe_3O_4+H_2\rightarrow Fe+H_2O$ (Oxit màu đen nóng đỏ chuyển dần thành chất rắn màu xám có ánh kim)
a) Xuất hiện khí không màu không mùi
$2KMnO_4 \xrightarrow{t^o}K_2MnO_4 + MnO_2 + O_2$
b) Chất rắn chuyển từ màu nâu đỏ sang màu đen
$2Cu + O_2 \xrightarrow{t^o} 2CuO$
c) Chất rắn chuyển từ màu đen sáng màu đen xám
$Fe_3O_4 + 4H_2 \xrightarrow{t^o} 3Fe + 4H_2O$
: Trong phòng thí nghiệm, người ta tiến hành điều chế khí oxi bằng cách nhiệt phân muối kaliclorat KClO3 thu được muối kaliclorua và oxi.
a. Viết PTHH xảy ra? (0.5đ)
b. Tính khối lượng KClO3 cần dùng để điều chế được 9.6 g khí oxi? (1.0đ)
c. Nếu cho 32.5g kẽm phản ứng với lượng oxi ở phản ứng trên thì thu được kẽm oxit có khối lượng la bao nhiêu? (1.5đ)
giải thích hiện tượng xảy ra khi nhiệt phân muối NaHCO3 bằng lời.
\(2NaHCO_3\rightarrow\left(t^o\right)Na_2CO_3+CO_2+H_2O\)
Hiện tượng: Trên thành bình (ống) có những giọt nước đọng lại. Thấy có sủi bọt khí.
Giải thích: Muối axit không bền với nhiệt (cụ thể ở đây là NaHCO3)
Tham khảo:
Sau khi thực hiện thí nghiệm nhiệt phân NaHCO3 bằng ống nghiệp ta sẽ thu được kết quả bằng các hiện tượng như sau:
-Thành của ống nghiệm có xuất hiện nhiều giọt nước đọng lại.
-Ống nghiệm có hiện tượng vẩn đục.
Hãy gải thích hiện tượng hoá học xảy ra và viết các phương trình phản ứng khi tiến hành các thí nghiệm sau: a; Cho mẫu bari kim loại vào dung dịch muối Đồng (II) clorua b; Cho mẫu đoòng vào H2So4 đậm đặc nóng.
a. Hiện tượng: Bari chạy trên mặt nước, có khí không màu thoát ra, sau đó có kết tủa xanh tạo thành.
\(PTHH:\)
\(Ba+2H_2O--->Ba\left(OH\right)_2+H_2\)
\(Ba\left(OH\right)_2+CuCl_2--->Cu\left(OH\right)_2\downarrow+BaCl_2\)
b. Hiện tượng: Đường từ màu trắng dần chuyển sang màu đen, sau đó phần màu đen dần phồng lên.
PTHH:
\(C_{12}H_{22}O_{11}\overset{H_2SO_{4_{đặc}}}{--->}12C+11H_2O\)
\(C+2H_2SO_{4_đ}--->CO_2+2SO_2+2H_2O\)
cách tiến hành thí nghiệm đun muối
Tiến hành các thí nghiệm sau:
(a) Thổi luồng khí CO dư qua ống sứ đựng MgO nung nóng.
(b) Đốt FeS2 trong không khí.
(c) Nung hỗn hợp bột gồm Al và Fe2O3 (tỉ lệ mol 2 : 1) trong khí trơ, ở nhiệt độ cao.
(d) Điện phân dung dịch CuCl2 (điện cực trơ, màng ngăn xốp).
(e) Nhiệt phân muối bạc nitrat.
Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm thu được kim loại là
A. 2
B. 3
C. 4
D. 5
Tiến hành các thí nghiệm sau:
(a) Thổi luồng khí CO dư qua ống sứ đựng MgO nung nóng.
(b) Đốt FeS2 trong không khí.
(c) Nung hỗn hợp bột gồm Al và Fe2O3 (tỉ lệ mol 2 : 1) trong khí trơ, ở nhiệt độ cao.
(d) Điện phân dung dịch CuCl2 (điện cực trơ, màng ngăn xốp).
(e) Nhiệt phân muối bạc nitrat.
Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm thu được kim loại là
A. 2
B. 3
C. 4
D. 5
Đáp án B
(a) Không xảy ra phản ứng khử oxit kim loại (CO chỉ khử được oxit kim loại từ Zn trở về sau).
(b) 4FeS2+ 11O2 → t o 2Fe2O3+ 8SO2
(c) 2Al+ Fe2O3 → t o Al2O3+2Fe
(d) Điện phân dung dịch CuCl2, (điện cực trơ, màng ngăn xốp)
→ Thu được đồng kim loại ở catot (-).
AgNO3 → t o Ag+NO2+ 1 2 O2
Tiến hành thí nghiệm (A, B, C) ở điều kiện thường về phenol (C6H5OH) và muối C6H5ONa như hình vẽ sau đây:
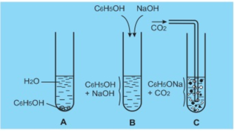
Thông qua các thí nghiệm cho biết điều khẳng định nào sau đây là chính xác?
A. Phenol ít tan trong nước nóng, tan nhiều trong dung dịch kiềm, có lực axit mạnh hơn axit cacbonic
B. Phenol tan nhiều trong nước nóng, tan nhiều trong dung dịch kiềm, có lực axit mạnh hơn axit cacbonic
C. Phenol ít tan trong nước lạnh, nhưng tan nhiều trong dung dịch kiềm, có lực axit yếu hơn cả axit cacbonic
D. Phenol ít tan trong nước lạnh, tan ít trong dung dịch kiềm, có lực axit yếu hơn cả axit cacbonic